元素锶广泛分布于环境、水、食物和几乎所有的生物体中,锶对人体健康具有重要意义,其参与多种生理功能。由于锶与钙化学性质相似,所以锶与钙在生理过程中起到的作用具有高度相似性,锶对骨骼成骨机制以及骨骼疾病,尤其骨质疏松症有着重要作用[1-3];对口腔疾病[4-6]、心血管疾病[7-9]、心脏病[10-12]具有良好的预防作用;对精液的积极作用有助于维持生殖健康[13-15];同时锶为防治非酒精性脂肪肝作出贡献[14-16];与妊娠期高血压、子痫前期等疾病的相关性以及对胎儿早产、胎儿疾病的相关性也备受关注[17-19]。在世界上大多数地区,锶的每日总摄入量约为4 mg,其中0.7~2.0 mg来自饮用水,1.2~2.3 mg来自食品[18]。 因为锶不易被人体吸收,吸收水平约为25%~30%[20],所以单纯从水中摄取锶元素,还不能满足人体需求。目前我国富锶食品类型较少,富锶饮用水、富锶茶叶、富锶苹果等产品相继面市,《中国居民膳食指南(2022年)》推荐每人每天摄入300~500 g乳及乳制品,乳制品在人们的饮食中占比较大,所以富锶乳制品的开发具有巨大发展前景。根据国家食品安全风险评估中心“十四五”规划工作中新提到的锶元素的重要性,对于富锶食品的评价和风险控制工作具有重要意义。研究表明过量摄入锶存在提高心血管疾病发生率的风险[21],长期饮用锶浓度相对较高的水会影响骨骼矿化[22],动物试验结果表明过量锶会导致胎鼠骨骼和眼睛发育异常[23],所以在开发富锶乳制品的过程中对锶含量的监测是重要的风险控制点。
本研究建立乳及乳制品中锶的检测方法,为富锶乳制品的开发研究奠定基础。目前我国对于锶元素含量的检测方法主要有溶液阴极辉光放电-原子发射光谱法(solution cathode glow discharge-atomic emission spectrometry,SCGDAES)[24]、电感耦合等离子体原子发射光谱法(inductively coupled plasma-atomic emission spectroscopy,ICP-AES)[25-26]、电感耦合等离子体质谱法(inductively coupled plasma-mass spectrometer,ICP-MS)[27-28]、离子色谱法(ion chromatography,IC)[29]、原子吸收色谱法(atomic absorption spectrome try,AAS)[30],具体应用在乳及其制品中锶的检测方法报道较少。AAS法不能多元素同时检测[31];SCGD-AES法仅适合水中相关元素的检测,在乳制品检测中的实际应用性并不强;IC法简单快速,更适合企业对矿泉水中常规阳离子的检测要求;ICP-AES和ICP-MS法可以满足多元素同时检测,并具有灵敏度高,检出限低,干扰少的优点。本研究采用电感耦合等离子体质谱法对不同乳制品中锶的含量进行检测,优化内标元素、锶同位素、赶酸方式和氦气流量,从而提高仪器工作效率,实现乳制品中锶含量的准确测定,以期为富锶乳及其制品的研发以及风险监控提供关键检测技术和科学依据。
1 材料与方法
1.1 材料与试剂
乳及乳制品(包括液态乳、发酵乳、乳粉和奶酪):市售。
含锶的标准奶粉:北京微标标物科技有限公司,附标准样品检测证书。
硝酸(分析纯):上海安谱实验科技股份有限公司;锶元素标准储备液(1 000 μg/mL)、含锗元素的多元素(45Sc、72Ge、103Rh、115In、185Re、209Bi)内标标准储备液(100 μg/mL):钢研纳克检测技术股份有限公司;试验所用去离子水符合GB/T 6682—2008《分析实验室用水规格和试验方法》[32]规定。
1.2 仪器与设备
ICP-MS 8900电感耦合等离子体质谱仪:美国Agilent公司;MARS 6密闭微波消解仪:美国CEM公司;XPR 205 DU电子天平:梅特勒-托利多仪器(上海)有限公司;BFGS-24A赶酸仪:北京信和达科技有限公司;Synergy UV Remote超纯水机:美国默克密理博公司。
1.3 方法
1.3.1 样品前处理
分别称取乳粉0.3 g、奶酪0.3 g、液态乳1.0 g、发酵乳1.0 g于微波消解罐中,加入10 mL硝酸,旋紧罐盖预消解后,放入微波消解仪中,消解程序参考国标GB 5009.268—2016《食品安全国家标准食品中多元素的测定》[33]:功率1 600 W,120 ℃升温10 min,恒温5 min;170 ℃升温5 min,恒温5 min;190 ℃升温5 min,恒温25 min。 冷却后取出消解罐,缓慢打开罐盖排气,用少量水冲洗内盖,将消解罐放在可调式电热赶酸仪上赶酸后,用少量水洗涤消解罐2~3次,合并洗涤液于容量瓶中,用水定容混匀备用,同时在不加试样的情况下按照与样品处理相同的方法作空白试验对照组。
1.3.2 标准工作液制备
锶标准工作液:取适量锶标准储备液,用硝酸溶液稀释配制成质量浓度为10 ng/mL、50 ng/mL、100 ng/mL、200 ng/mL、500 ng/mL的系列标准工作液。
锗元素(内标)标准工作液:取适量含有锗元素的内标储备液,用硝酸溶液稀释配制成质量浓度为500 ng/mL的内标工作液。
1.3.3 ICP-MS仪器条件
按照仪器标准操作步骤调整参数:射频功率为1 550 W,雾化器为高盐/同心雾化器,等离子体气流量为15 L/min,采样锥/截取锥为镍/铂锥,采样深度10 mm,采样模式为跳峰扫描,载气流量为1.01 L/min,辅助气流量为0.90 L/min,氦气流量为4.0~5.5 mL/min,雾化室温度为2 ℃,自动检测,重复10次,样品提升速率为0.3 rps。
定性定量方法:通过检测样品中元素的特征质谱峰实现定性;采用标准曲线法与内标法结合的方法定量,通过配制不同浓度的标准溶液建立浓度与信号强度的线性关系,利用该曲线反推待测样品的浓度。 同时在样品和标准中在线加入已知浓度的内标元素,通过内标信号校正仪器波动和基体效应,提高定量准确性。
1.3.4 锶同位素及内标的选择
以线性回归方程、灵敏度、干扰因素为评价指标,考察锶元素的4个同位素84Sr、86Sr、87Sr、88Sr对锶元素检测结果的影响。
以灵敏度和回收率为评价指标,选择国标给定的内标103Rh、115In,另增加72Ge作为内标,考察3种元素对锶元素检测结果的影响。
1.3.5 赶酸处理优化
考察100 ℃、30 min赶走酸雾后定容上机(国标赶酸处理)[33]及160 ℃赶酸到剩余量约0.5 mL后定容上机(本试验赶酸处理)。两种赶酸方式对锶元素含量检测结果的影响[34]。
1.3.6 质谱条件优化
为了减小仪器噪声,使得信号最大化,首先在标准模式下利用1 μg/L的Li、Co、Mg、Y、TI、Ce调谐液对仪器工作参数进行调节,使氧化物CeO/Ce比率控制在<2%,双电荷<3%,否则会严重影响部分元素的准确度。 参考GB 5009.268—2016《食品安全国家标准食品中多元素的测定》进行选择优化,分别考察不同氦气流量(4.0 mL/min、4.5 mL/min、5.0 mL/min、5.5 mL/min)对锶元素检测的影响,用含锶的标准奶粉(标准样品证书给定中位值2.08 mg/kg,标准范围1.86~2.30 mg/kg)的检测结果为判断依据,进而确定最优氦气流量,获得更好的灵敏度。
1.3.7 方法学考察
(1)标准曲线的绘制及检出限、定量限的确定:按照上述仪器条件,依次测定含锗元素(内标)标准工作液的锶元素系列标准工作液、待测样品和空白对照的信号响应值,以锶元素的质量浓度(X)为横坐标,锶元素与锗元素信号响应值的比值(Y)为纵坐标,绘制标准曲线,得到标准曲线的线性范围、回归方程、相关系数,从而确定锶元素的含量。
(2)检出限和定量限:依据GB/T 27417—2017《合格评定化学分析方法确认和验证指南》[36],用样品空白平均值+3S(S,标准偏差值)的方法计算检出限,+10S(S,标准偏差值)的方法计算定量限。
(3)加标回收率和精密度试验:为了验证方法的正确性,以常见乳制品中的4种基质(液态乳、发酵乳、乳粉和奶酪)为本底样品,参考GB/T 27404—2008《实验室质量控制规范食品理化检测》[35],对样品进行定量限、2倍定量限、10倍定量限的3水平加标实验,重复测定7次,计算加标回收率和精密度试验结果的相对标准偏差(relative standard deviation,RSD)。
1.3.8 数据处理
使用软件Excel 2021和Minitab 16处理数据及制图。
2 结果与分析
2.1 锶同位素的选择
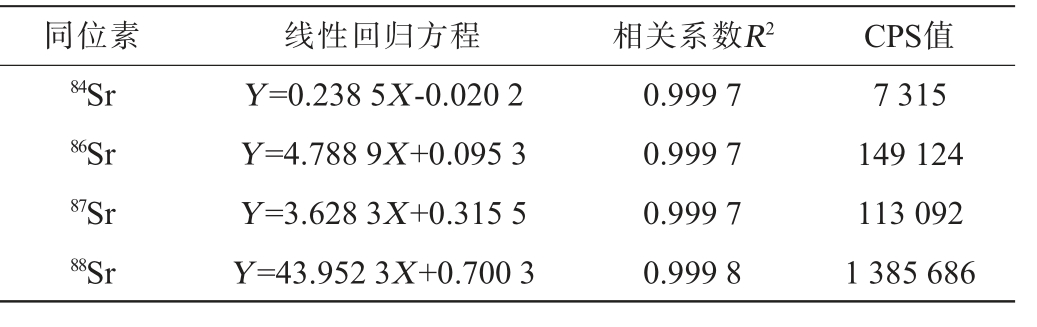
4种锶同位素线性回归方程及灵敏度分析结果见表1。由表1可知,84Sr、86Sr、87Sr、88Sr在0~500 ng/mL范围内呈良好线性关系,相关系数(R2)均>0.999。ICP-MS中利用每秒计数(counts per second,CPS)来表示元素检测信号的强度,通常认为CPS越高,灵敏度越高。由表1可知,88Sr的CPS值最高,84Sr、86Sr、87Sr的灵敏度均较低,对于一些低含量样品的检测结果影响较大。此外,部分乳制品样品中的87Sr易受到87Rb的干扰,而88Sr的丰度最高且无其他元素干扰,因此本实验选择线性好、灵敏度高、无干扰的88Sr进行下一步研究。
表1 不同锶同位素的线性方程及灵敏度分析
Table 1 Linear equations and sensitivity analysis of different strontium isotopes
同位素线性回归方程相关系数R2CPS值84Sr 86Sr 87Sr 88Sr Y=0.238 5X-0.020 2 Y=4.788 9X+0.095 3 Y=3.628 3X+0.315 5 Y=43.952 3X+0.700 3 0.999 7 0.999 7 0.999 7 0.999 8 7 315 149 124 113 092 1 385 686
2.2 内标的选择
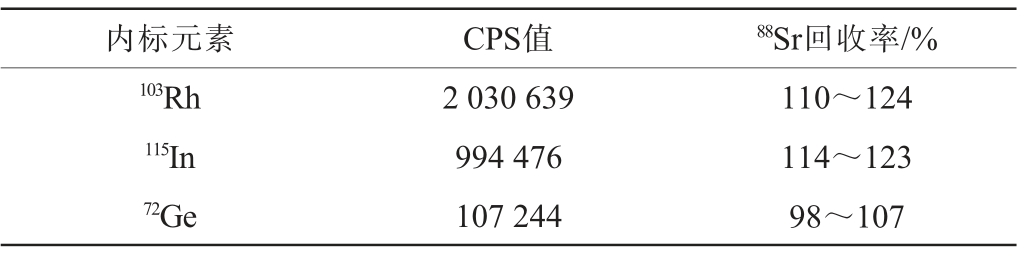
由于雾化过程、气溶胶传输过程导致的物理性干扰以及受到等离子体电离效应和空间电荷效应的基体性干扰的影响,如果待测元素的信号受到抑制作用,那么内标也会受到同样的影响,所以选择内标对每个待测元素信号进行校正,内标元素质量数应与待测元素相近,基于电离势能的匹配性进行选择。 3种内标的灵敏度分析和定量限、2倍定量限、10倍定量限的加标回收率结果见表2。 由表2可知,103Rh的CPS值最高,115In次之,72Ge最低。 但103Rh、115In作为内标的回收率偏高,起不到校正的作用,72Ge的质量数与88Sr的质量数相近,电离能相似,且72Ge作为内标的回收率良好,为98%~107%,满足GB 27404—2008《实验室质量控制规范食品理化检测》[35]的要求,因此选择72Ge作为内标。
表2 不同内标对锶含量检测的灵敏度分析及回收率结果比较
Table 2 Sensitivity analysis and recovery comparison of different internal standards for strontium content detection
内标元素CPS值88Sr回收率/%103Rh 115In 72Ge 2 030 639 994 476 107 244 110~124 114~123 98~107
2.3 赶酸方式的选择
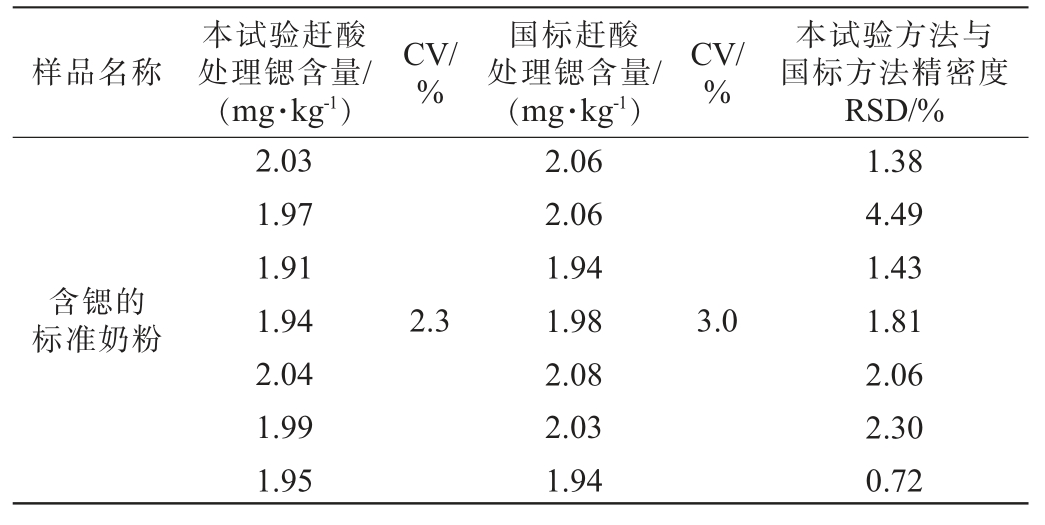
不同赶酸方式对锶含量检测结果的影响结果见表3。由表3可知,本试验与国标两种赶酸处理方法的变异系数(coefficient of variation,CV)分别为2.3%与3.0%,满足GB/T 27404—2008《实验室质量控制规范食品理化检测》[35]中被测组分含量在10 mg/kg,实验室变异系数<7.5%的要求。通过方差分析得到本方法和国标方法的P=0.231>0.05,说明本方法与国标方法对锶元素的检测结果无显著影响。与国标仅赶酸雾的方式相比,本实验方法减少酸气对人体、设备、环境的危害,有效降低样品溶液中的酸度,使得样品溶液的酸度与标准溶液的酸度更加匹配,所以选择160 ℃赶酸到剩余量约0.5 mL的赶酸方式。
表3 不同赶酸方式对锶含量检测结果的影响
Table 3 Effects of different acid extraction methods on the detection results of strontium content
样品名称含锶的标准奶粉本试验赶酸处理锶含量/(mg·kg-1)2.03 1.97 1.91 1.94 2.04 1.99 1.95 CV/%2.3国标赶酸处理锶含量/(mg·kg-1)2.06 2.06 1.94 1.98 2.08 2.03 1.94 CV/%3.0本试验方法与国标方法精密度RSD/%1.38 4.49 1.43 1.81 2.06 2.30 0.72
2.4 氦气流量优化
氦气通过碰撞模式可以消除多原子离子结合产生的质谱干扰,氦气碰撞程度直接影响仪器的灵敏度,流量过低可能导致碰撞不足,无法有效消除干扰,流量过高会导致灵敏度下降。 不同氦气流量对锶元素检测结果的影响见图1。由图1可知,在均值95%的置信区间内,氦气流量为4.5 mL/min、5.0 mL/min时检测结果偏高,氦气流量为5.5mL/min时检测结果较分散,当氦气流量为4.0 mL/min比较集中在中位值,满足要求,因此选择氦气流量为4.0 mL/min。
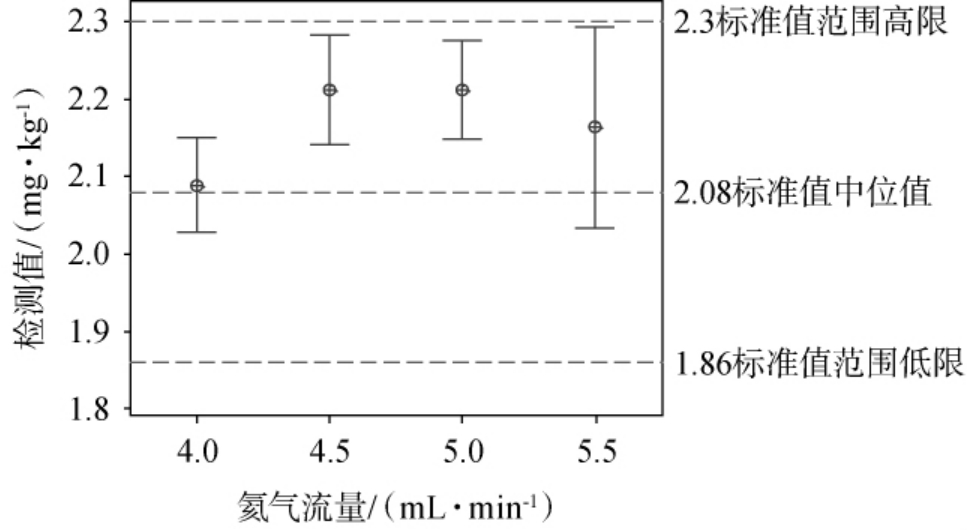
图1 不同氦气流量对锶含量检测结果的影响
Fig.1 Effects of different He flow rates on the detection results of strontium content
2.5 方法学考察
2.5.1 线性范围、线性回归方程、相关系数、检出限与定量限结果见表4,锶元素在0~500 ng/mL范围内呈良好的线性关系,相关系数(R2)>0.999,检出限和定量限分别为2.21 μg/kg和6.27 μg/kg,满足国标《食品安全国家标准食品中多元素的测定》[33]的要求。
表4 锶元素的线性范围、线性回归方程、相关系数、检出限与定量限
Table 4 Linear range, linear regression equation, correlation coefficient,detection limit and quantification limit of strontium

元素 线性范围/(ng·mL-1)线性回归方程相关系数R2定量限/(μg·kg-1)锶0~500 Y=43.952 3X+0.700 3 0.999 82.216.27检出限/(μg·kg-1)
2.5.2 加标回收率与精密度试验
锶的加标回收率与精密度试验结果见表5。
表5 不同乳制品中锶的加标回收率及精密度实验结果
Table 5 Experimental results of the spiked recovery rate and precision of strontium in different dairy products
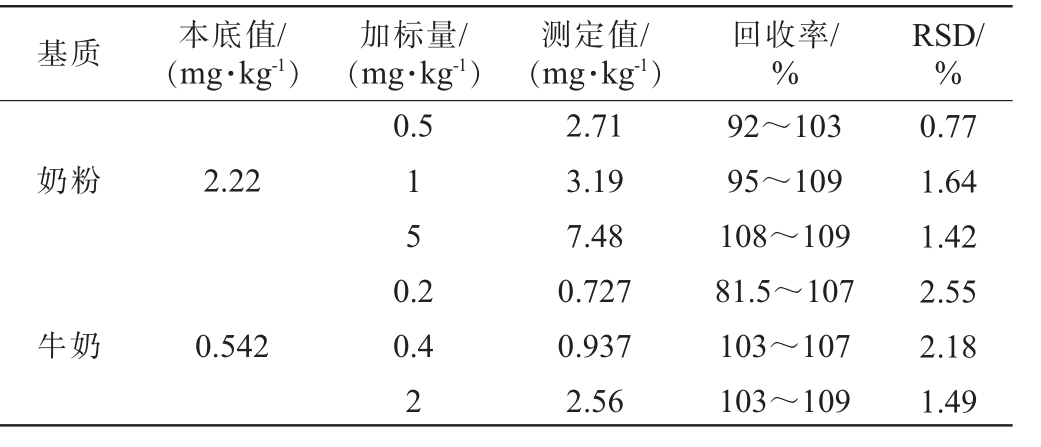
基质本底值/(mg·kg-1)加标量/(mg·kg-1)测定值/(mg·kg-1)回收率/%RSD/%0.5奶粉2.22 1 5牛奶0.542 0.2 0.4 2 2.71 3.19 7.48 0.727 0.937 2.56 92~103 95~109 108~109 81.5~107 103~107 103~109 0.77 1.64 1.42 2.55 2.18 1.49
续表
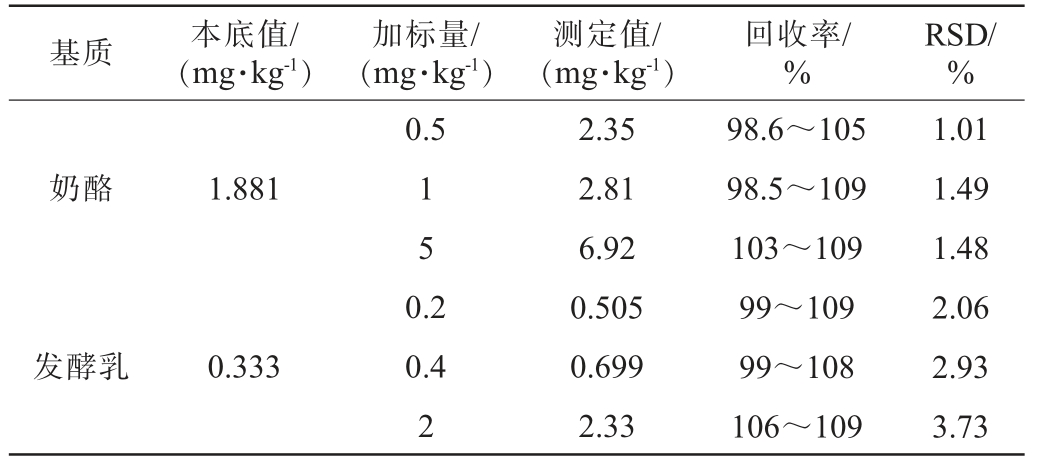
基质本底值/(mg·kg-1)加标量/(mg·kg-1)测定值/(mg·kg-1)回收率/%RSD/%0.5奶酪1.881 1 5发酵乳0.333 0.2 0.4 2 2.35 2.81 6.92 0.505 0.699 2.33 98.6~105 98.5~109 103~109 99~109 99~108 106~109 1.01 1.49 1.48 2.06 2.93 3.73
由表5可知,不同乳制品中锶元素的加标回收率为81.5%~109%,精密度试验结果的RSD为0.77%~3.73%,结果满足GB/T 27404—2008《实验室质量控制规范食品理化检测》[35]要求,说明该方法准确性与重复性良好。
2.5.3 实际奶粉样品中锶含量的测定
应用本研究建立的电感耦合等离子体质谱法检测含锶标准奶粉样品中锶元素含量,检测值为2.03 mg/kg,该奶粉样品锶元素含量实际中位值为2.08 mg/kg,标准值区间为1.86~2.30 mg/kg,对检测值和实际中位值进行单样本t检验,P=0.133>0.05,二者无显著差异,且检测值在标准值区间内,说明该方法可用于实际样品中锶元素的检测。
3 结论
本研究建立了电感耦合等离子体质谱测定不同乳制品中锶元素的方法,在国标基础上进行优化,选择赶酸方式为160 ℃赶酸到剩余量约0.5 mL,氦气流量为4.0 mL/min,用内标元素72Ge校正,对同位素88Sr进行检测。结果表明,该方法在锶元素0~500 ng/mL质量浓度范围内线性关系良好,相关系数(R2)>0.999,方法检出限为2.21 μg/kg,定量限为6.27 μg/kg,对4种乳制品的加标回收率为81.5%~109%,精密度试验结果RSD为0.77%~3.73%。该方法线性范围宽,干扰小,灵敏度高,精密度和准确度良好,可为后期对富锶乳的资源开发和食品安全风险评估等方面提供有效的技术参考。
[1]席雪瑶,高亚男,王加启,等.锶的成骨机制及富锶食品的研发现状[J].现代食品科技,2023,39(9):381-386.
[2]KOODZIEJSKA B S, KOLMAS J.The influence of strontium on bone tissue metabolism and its application in osteoporosis treatment[J].Int J Mol Sci,2021,22(12):6564.
[3]LI D Z, CHEN K, DUAN L, et al.Strontium ranelate incorporated enzyme-cross-linked gelatin nanoparticle/silk fibroin aerogel for osteogenesis in OVX-induced osteoporosis[J].ACS Biomater Sci Eng,2019,5(3):1440-1451.
[4]董昕玥,张晓明,刘念,等.锶元素促成骨机制及在口腔再生医学中的应用研究进展[J].中国医药科学,2024,14(3):38-39.
[5]曲静,卢冰铃,刘瑜瑜,等.含锶脱敏牙膏对牙本质过敏症脱敏作用的Meta分析[J].深圳中西医结合杂志,2024,34(1):11-13.
[6]MARX D,RAHIMNEJAD YAZDI A,PAPINI M,et al.A review of the latest insights into the mechanism of action of strontium in bone[J].Bone Rep,2020,12:100273.
[7]黄胥莱,高亚男,张养东,等.食品中锶功能的研究进展[J].食品科学,2023,44(15):401.
[8]李牧,杨佳琳,杨庭树,等.微量元素锶对幼年自发性高血压大鼠血压升高的预防作用及其作用机制探讨[J].现代生物医学进展,2012,12(12):2259-2264.
[9]李牧,杨佳琳,杨庭树,等.微量元素锶对实验性兔动脉粥样硬化斑块形成的影响[J].中国医药导报,2012,12(9):17-19.
[10]王娟,贺攀红,杨珍.在线双毛细管火焰原子吸收法测定海带中的微量锶[J].食品科学,2014,35 (10):192-194.
[11]刘婧婷,周亚威,王文第,等.孕期重金属元素和微量元素水平与子代先天性心脏病相关性的前瞻性队列研究[J].中国当代儿科杂志,2022,24(2):148-152.
[12]林妤浈,辛志明,夏瑜鸿,等.饮水锶对高血压小鼠抗氧化功能的影响[J].营养学报,2023,45(5):460-464.
[13]FAWZY M, ENAD M, MAHRAN A, et al.Artificial oocyte activation with SrCl2 or calcimycin after ICSI improves clinical and embryological outcomes compared with ICSI alone: Results of a randonmized clinical trial[J].Human Reprod,2018,33(9):1636-1644.
[14]杨继勇,张养东,郑楠,等.锶元素的生物学功能及其在人体内的代谢研究进展[J].中国食物与营养,2022,28(9):50-56.
[15]NOROZI-HAFSHEJANI M,TAVALAEE M,AZADI L,et al.Effects of assisted oocyte activation with calcium-ionophore and strontium chloride on in vitro ICSI outcomes[J].Ira J Basic Med Sci,2018,21(11):1109-1117.
[16]姜慧玲,关桥伟,龚林,等.微量元素锶改善大鼠非酒精性脂肪肝的机制研究[J].中国比较医学杂志,2017,27(2):9-12.
[17]TANG Y,XIA W,XU S Q,et al.Association of urinary strontium levels with pregnancy-induced hypertension[J].Curr Med Sci, 2021, 41(3):535-541.
[18]王瑞,李蕊,李运龙,等.锶与妊娠及妊娠期疾病的研究进展[J].基础医学与临床,2024,44(4):430-431.
[19]YIN S, WEI J, WANG C, et al.Alkali and alkaline earth elements in maternal serum and occurrence of orofacial clefts in offspring[J].Reprod Toxicol,2022,110:97-104.
[20]MARIE P J,AMMANN P,BOIVIN G,et al.Mechanisms of action and therapeutic potential of strontium in bone[J].Calcif Tissue Int, 2001,69(3):121-129.
[21]CURTIS E M, COOPER C, HARVEY N C.Cardiovascular safety of calcium,magnesium and strontium:What does the evidence say[J].Aging Clin Exp Res,2021,33:479-494.
[22]PORS NIELSEN S.The biological role of strontium[J].Bone,2004,35:583-588.
[23]CHIU C Y,CHIU H C,LIU S H,et al.Prenatal developmental toxicity study of strontium citrate in Sprague Dawley rats[J].Regul Toxicol Pharmacol,2019,101:196-200.
[24]郑培超,罗元江,王金梅,等.溶液阴极辉光放电-原子发射光谱法测定富锶矿泉水中的锶[J].光谱学与光谱分析,2022,42(1):273-275.
[25]潘钢,雷勇,李可及.电感耦合等离子体原子发射光谱法测定高钡光学玻璃中锶的含量[J].理化检验-化学分册,2022,58(9):1023-1024.
[26]王祝,李明礼,邵蓓,等.电感耦合等离子体发射光谱法测定西藏日多温泉地热水中11种主次量元素[J].岩矿测试,2015,34(3):303.
[27]崔艳梅,韩典峰,姜芳,等.电感耦合等离子体质谱(ICP-MS)法测定水产品中锶同位素比值[J].中国无机分析化学,2023,13(4):382-388.
[28]于丽,吴渺渺,刘美思,等.电感耦合等离子体质谱法测定新食品原料黑果腺肋花楸果中的20种营养元素[J].食品安全质量检测学报,2020,20(11):7289-7290.
[29]高翔,姜明洪,张明,等.离子色谱法检测矿泉水中钠、钾、镁、钙、锶[J].饮料工业,2013,16(10):32-34.
[30]张慧,白小鸣,张大强,等.火焰原子吸收分光光度法检测矿泉水中锶含量[J].现代食品,2018(10):132-136.
[31]黄晓燕,唐烁,刘丽君,等.乳及乳制品中元素检测技术研究进展[J].乳业科学与技术,2023,46(5):57.
[32]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 6682—2008 分析实验室用水规格和试验方法[S].北京:中国标准出版社,2008.
[33]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB 5009.268—2016 食品安全国家标准食品中多元素的测定[S].北京:中国标准出版社,2016.
[34]黄晓燕,宁月莲,刘丽君,等.前处理过程对电感耦合等离子体-质谱法测定乳粉中多种元素含量准确性的影响[J].乳业科学与技术,2022,45(2):14-16.
[35]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 27404—2008 实验室质量控制规范食品理化检测[S].北京:中国标准出版社,2008.
[36]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 27417—2017 合格评定化学分析方法确认和验证指南[S].北京:中国标准出版社,2017.