Determination of 12 methylsiloxanes residues in Baijiu contacting materials by GC-MS/MS
随着人们健康意识不断的提升,消费者对食品安全提出了更高的要求。由于乙醇具有较强的溶解性,白酒与不同材料接触后,包装材料中的有毒有害物质可能会迁移到酒体当中,给白酒品质安全带来较大风险隐患,因此,对白酒接触材料提出了较高的要求。白酒酒瓶包含了瓶底、瓶身、内塞、密封圈等部位,与酒体直接接触的部位在酒瓶内部和瓶盖内塞,其接触材料类型主要有玻璃、陶瓷和塑料、硅橡胶等,而塑料制品凭借优良的性能、低廉的成本和优美的外观,成为了白酒瓶盖内塞难以替代的物品。在聚合过程中,由于硫化不完全等原因易发生甲基硅氧烷残留,瓶盖内塞与酒体长时间接触易导致残留化合物浸入酒体当中,造成白酒出现异杂味、“塑化剂”等食品安全问题[1]。
甲基硅氧烷是主链为Si—O—Si键、侧链为Si—C键形成的有机化合物,其主链结构可分为线型甲基硅氧烷(用Ln表示,n为硅原子数)和环型甲基硅氧烷(用Dn表示)。因为甲基硅氧烷中硅和氧连接键不仅键能较大,而且键长较长,可自由旋转,导致其化学性质比较稳定,具有耐老化、耐高温、电绝缘性良好、疏水性强、耐紫外辐射等特点[2-3],在食品、纺织品、化妆品和药品包装材料等领域应用广泛。
随着对甲基硅氧烷的研究和应用日益深入,人们逐渐认识到某些甲基硅氧烷类化合物不仅难以降解,而且可通过多种途径进入人体内,可能对人体引发较大的健康风险和生态问题[4-7],因此,甲基硅氧烷类化合物成为了新一类污染物[8-10]。研究表明,将大鼠长期暴露于八甲基环四硅氧烷(D4)和十甲基环五硅氧烷(D5)中,会加快大鼠衰老速度[11-12]。由于甲基硅氧烷及其衍生物在多种介质或环境中被广泛检测到[13-16],甲基硅氧烷类化合物产生的食品安全风险引起了越来越多的关注。因此,加强对白酒接触材料中甲基硅氧烷类化合物的监测是十分必要的。
当前,甲基硅氧烷类化合物的检测主要集中在硅橡胶产品[17]、纺织品[18-19]、药用产品[20-22]、化妆品[23]、皮革[24]和水体[25]等领域,而在白酒接触材料中的报道较少。由于甲基硅氧烷多具有挥发性,研究人员多选择气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)或结合静态顶空和热裂解/热脱附法、气相色谱法等用于研究分析。气相色谱-串联质谱(gas chromatography-tandem mass spectrometry,GC-MS/MS)法具有分离效率高、检测灵敏度高、操作便捷等优点,广泛应用于检测多种挥发性化合物,如硫化物、磷化物、硅氧烷类化合物等。本研究以白酒瓶盖内塞为主要研究对象,利用GC-MS/MS法建立了12种甲基硅氧烷类化合物(环型甲基硅氧烷:六甲基环三硅氧烷(D3)、八甲基环四硅氧烷(D4)、十甲基环五硅氧烷(D5)、十二甲基环六硅氧烷(D6)、十四甲基环七硅氧烷(D7)、十六甲基环八硅氧烷(D8);线型甲基硅氧烷:八甲基三硅氧烷(L3)、十甲基四硅氧烷(L4)、十二甲基五硅氧烷(L5)、十四甲基六硅氧烷(L6)、十六甲基七硅氧烷(L7)、十八甲基八硅氧烷(L8))残留量的检测方法,并对该检测方法进行方法学考察,旨在为白酒品质安全监测和评估提供方法参考和借鉴。
1.1.1 材料
白酒瓶盖内塞:市售。
1.1.2 化学试剂
正己烷(色谱纯):安徽天地高纯溶剂有限公司;六甲基环三硅氧烷至十六甲基环八硅氧烷(编号为D3~D8)、八甲基三硅氧烷至十八甲基八硅氧烷(编号为L3~L8)(纯度95.0%~99.0%):上海梯希爱化成工业发展有限公司。
M8800H-C超声波清洗机:美国Branson公司;A3S0505CE超纯水机:美国Milli-pore公司;8890-7000D气相色谱-串联质谱(GC-MS/MS)仪:美国Agilent公司;QT-2旋涡混合器:北京鑫骉腾达仪器设备有限公司;ME203E电子天平:美国Mettler Toledo公司。
1.3.1 标准溶液的配制
甲基硅氧烷标准储备液:取洁净的10 mL容量瓶12个,称取各甲基硅氧烷标准品10 mg分别加入其中,用正己烷定容并混匀,所得各甲基硅氧烷标准储备液的质量浓度为1 000 mg/L,转移至-18 ℃冰箱保存。
甲基硅氧烷混标中间液:分别吸取各甲基硅氧烷标准储备液于同一容量瓶中,用正己烷将其稀释100倍,所得混标中间液中各甲基硅氧烷化合物的质量浓度为10 mg/L,保存备用。
甲基硅氧烷标准工作系列溶液:在6个容量瓶中,各取适量的甲基硅氧烷混标中间液,经正己烷定容后,所得标准工作系列溶液的质量浓度分别为0.05 mg/L、0.10 mg/L、0.20 mg/L、0.50 mg/L、1.00 mg/L、2.00 mg/L。
1.3.2 仪器条件
气相色谱条件:载气为高纯氦气(He);流速1 mL/min;进样口温度270 ℃;分流比5∶1;HP-5MS UI毛细管色谱柱(30 m×0.25 mm,0.25 μm);进样体积1 μL;升温程序为起始温度50 ℃,保持2 min,以10 ℃/min升至220 ℃;再以20 ℃/min升至270 ℃,不保持。
质谱条件:电子电离(electronic ionization,EI)源;质量扫描范围50~650 m/z;电子能量70 eV;离子源温度230 ℃;MSD传输线温度270 ℃;四极杆温度150 ℃;多反应监测(multiple response monitoring,MRM)模式;后运行时间:4 min;溶剂延迟3.6 min。
定性定量方法:根据环型甲基硅氧烷(D3~D8)和线型甲基硅氧烷(L3~L8)标准品的保留时间进行定性,采用外标法进行定量分析。甲基硅氧烷含量计算公式如下:
式中:X为甲基硅氧烷含量,mg/kg;m为称取样品的质量,g;ρ为进样溶液中测得的甲基硅氧烷在标准曲线上的质量浓度,mg/L;10为提取液体积,mL。
1.3.3 甲基硅氧烷类化合物的质谱参数
将12种甲基硅氧烷标准溶液进行一级质谱扫描,将响应强度较大的离子确定其母离子;激化母离子使其产生子离子,再通过优化设置获得各离子的最佳碰撞能量。12种硅氧烷化合物保留时间、定量与定性离子及碰撞能量等质谱分析相关参数见表1。
表1 多反应监测条件下12种甲基硅氧烷类化合物参数信息
Table 1 Parameter information of 12 methylsiloxane compounds under multiple reaction monitoring
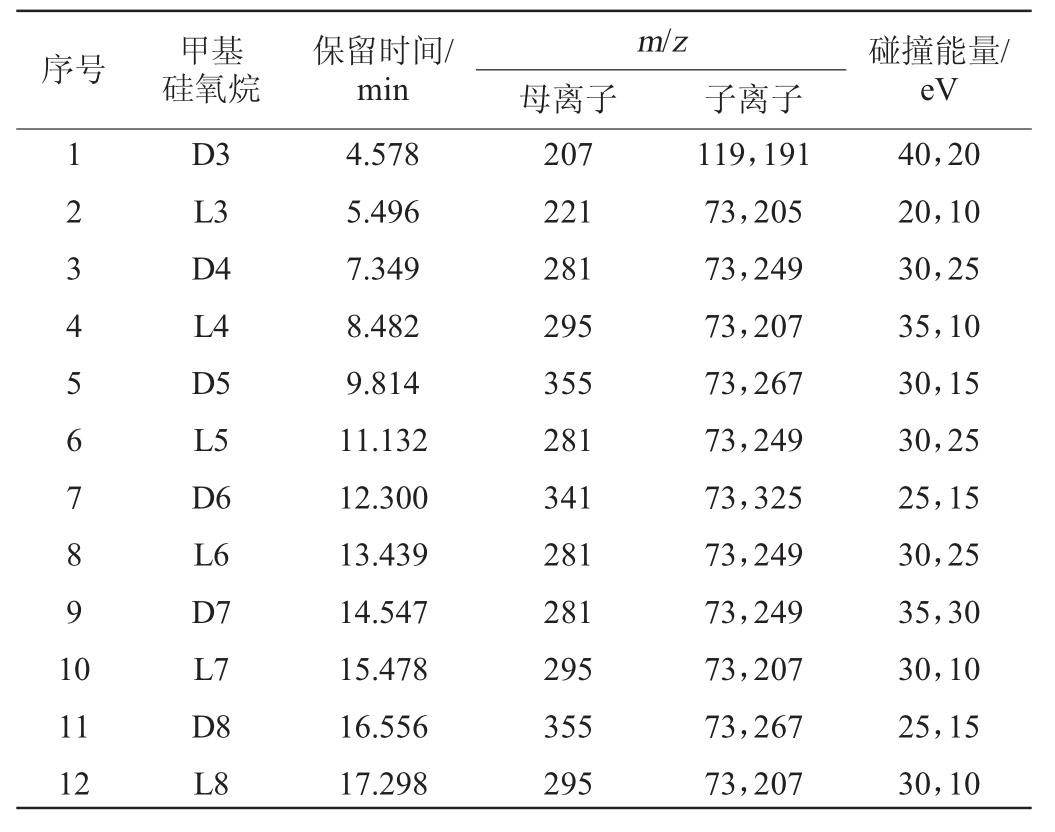
序号 甲基硅氧烷保留时间/min m/z母离子 子离子碰撞能量/eV 123456 7891 0 11 12 D3 L3 D4 L4 D5 L5 D6 L6 D7 L7 D8 L8 4.578 5.496 7.349 8.482 9.814 11.132 12.300 13.439 14.547 15.478 16.556 17.298 207 221 281 295 355 281 341 281 281 295 355 295 119,191 73,205 73,249 73,207 73,267 73,249 73,325 73,249 73,249 73,207 73,267 73,207 40,20 20,10 30,25 35,10 30,15 30,25 25,15 30,25 35,30 30,10 25,15 30,10
1.3.4 样品前处理
将白酒瓶盖内塞样品洗净晾干,用剪刀剪成约3 mm×3 mm的小块;称取已处理好的白酒瓶盖内塞样品0.5 g(精确至0.001 g),将其转移至25 mL具塞玻璃试管中,加入正己烷10 mL,盖上塞子,在功率为280 W条件下超声萃取40 min,静置10 min,取1 mL萃取溶液经滤膜过滤后上机分析,按照上述操作过程处理的正己烷溶液为空白溶液。
1.3.5 方法学考察
(1)标准曲线回归方程、线性范围、检出限及定量限
将12种甲基硅氧烷混合标准溶液稀释为6个不同浓度的标准工作系列溶液,采用1.3.2气相色谱、质谱条件进行分析检测,以色谱峰面积(Y)对物质质量浓度(X)进行线性回归分析,建立回归方程,得到线性关系和范围。配制一定浓度的甲基硅氧烷混合标准溶液,以3倍信噪比(signal to noise ratio,S/N)条件下的质量浓度作为检出限(limit of detection,LOD),10倍信噪比条件下的质量浓度作为定量限(limit of quantitation,LOQ)。
(2)精密度试验
取已知含量的瓶盖内塞样品,洗净剪碎后,称取0.50 g样品于玻璃试管中,添加一定质量浓度的甲基硅氧烷混合标准溶液,再加入正己烷溶液,按1.3.4的方法处理得到供试品,在1.3.2色谱质谱条件下连续进样检测6次,记录每次检测结果,并计算精密度试验结果的相对标准偏差(relative standard deviation,RSD)。
(3)加标回收率试验
取已知含量的瓶盖内塞样品,经洗净、剪碎、称量后,分别加入高、中、低三个水平的混合标准溶液适量,再加入正己烷溶液,按照1.3.4的方法处理样品,在1.3.2色谱质谱条件下进行分析检测,通过检测结果计算各成分加标回收率。
(4)重复性试验
取同一批次瓶盖内塞样品6个,经洗净、剪碎、称量后,分别加入质量浓度为1 mg/L的混合标准溶液,再加入正己烷提取,按1.3.4方法制作成供试品6份,在1.3.2色谱质谱条件下分析检测,记录其结果并计算其相对标准偏差。
1.3.6 数据处理与统计分析
使用Microsoft Excel 2010 进行统计分析,使用Origin 2022软件作图。
甲基硅氧烷类化合物可溶于多种有机试剂,如正己烷、二氯甲烷、乙酸乙酯、丙酮等,不同有机试剂对甲基硅氧烷类化合物具有不同的提取效果[26]。乙酸乙酯和丙酮均与乙醇互溶,不利于白酒中甲基硅氧烷类化合物的提取;二氯甲烷对甲基硅氧烷类化合物有熔融分解作用,溶解出的硅氧烷片段会对目标物产生干扰[2]。正己烷既能够有效提取甲基硅氧烷类化合物,又能在萃取后形成良好的分层。因此,本研究选择正己烷作为提取溶剂。
选用材质为硅橡胶的白酒瓶盖内塞,经洗净剪碎处理后置于25 mL具塞玻璃试管中,加入10 mL正己烷,在超声功率280 W条件下萃取,分别考察萃取时间为20 min、30 min、40 min、50 min条件下四种甲基硅氧烷类化合物的响应强度,结果见图1。由于在利用实际样品进行实验时,D5、D6、D7和D8色谱峰响应值较高,而其余8种甲基硅氧烷色谱峰响应值较低,因此,选择D5、D6、D7和D8四种甲基硅氧烷为考察对象。由图1可知,随着萃取时间在20~40 min范围内的延长,各甲基硅氧烷类化合物响应强度逐渐增加,当提取时间≥40 min之后,样品中各甲基硅氧烷类化合物响应趋于稳定。因此,选择超声萃取时间为40 min。
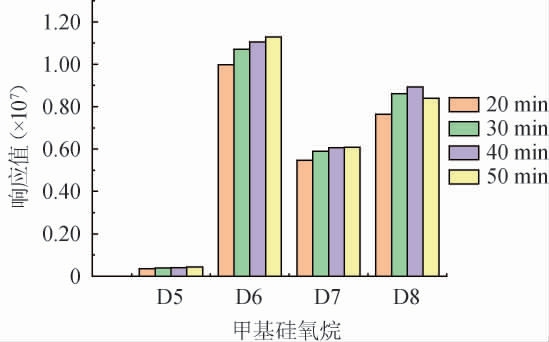
图1 四种甲基硅氧烷类化合物在不同超声萃取时间的提取效果
Fig.1 Extraction effect of four methylsiloxane compounds at different ultrasonic extraction times
为实现甲基硅氧烷类化合物的有效分离,比较了HPINNOWAX、DB-WAX UI和HP-5MS UI三种色谱柱(规格均为30 m×0.25 mm,0.25 μm)对甲基硅氧烷的分离效果,结果见图2。由图2可知,HP-INNOWAX和DB-WAX UI色谱柱均只能检测到10种甲基硅氧烷,未检测到D3和L3;而HP-5MS UI色谱柱能够检测出12种甲基硅氧烷并具有良好分离效果。因此,本研究选择HP-5MS UI色谱柱进行分离。
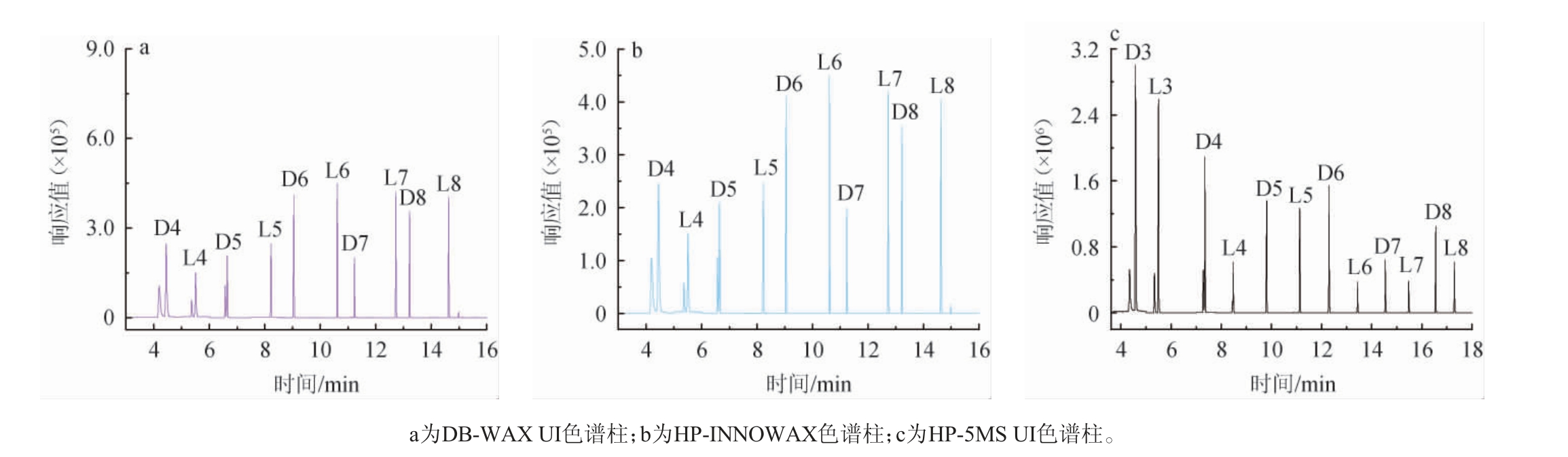
图2 三种不同色谱柱甲基硅氧烷类化合物分离效果
Fig.2 Separation effect of methylsiloxane compounds with three different chromatographic columns
在仪器检测方法运行过程中,除了质谱条件、升温程序、分流衬管等对目标物色谱峰响应值产生影响外,后运行温度和时间的设置也可能会对色谱峰响应值产生较大的影响。实验表明,当后运行温度分别设置在270 ℃、280 ℃、290 ℃和300 ℃时,色谱峰响应值变化均较小,选择后运行温度为270 ℃。在270 ℃条件下,为了考察样品在不同后运行时间下色谱峰响应值稳定性,分别设置后运行时间为1 min、2 min、3 min、4 min、5 min,不同后运行时间条件下四种甲基硅氧烷响应值见表2。由表2可知,随着后运行时间的增加,色谱峰响应值逐渐降低;当后运行时间为4 min和5 min时,四种甲基硅氧烷色谱峰响应值变化较小,相对稳定。因此,选择后运行时间为4 min。
表2 不同后运行时间条件下四种甲基硅氧烷类化合物响应值
Table 2 Four methylsiloxane compounds response values under
different post running time conditions
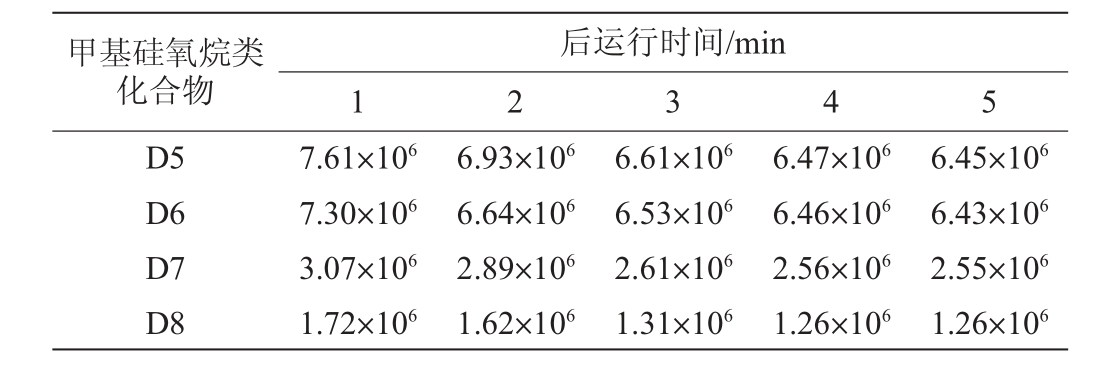
甲基硅氧烷类化合物D5 D6 D7 D8后运行时间/min 1 2 5 3 4 7.61×106 7.30×106 3.07×106 1.72×106 6.93×106 6.64×106 2.89×106 1.62×106 6.61×106 6.53×106 2.61×106 1.31×106 6.47×106 6.46×106 2.56×106 1.26×106 6.45×106 6.43×106 2.55×106 1.26×106
2.5.1 标准工作曲线的线性范围、回归方程、相关系数、检出限及定量限
按照优化后的条件,对甲基硅氧烷标准工作溶液进行检测,以甲基硅氧烷峰面积(Y)对质量浓度(X)进行回归分析,得到标准工作曲线回归方程及相关系数R2。以最低浓度点3倍信噪比计算检出限,10倍信噪比计算定量限,结果见表3。
表3 甲基硅氧烷类化合物标准曲线线性范围,回归方程,相关系数,检出限及定量限
Table 3 Standard curves linear range, regression equation, correlation coefficient, limits of detection and limits of quantitation of methylsiloxane compounds

甲基硅氧烷类化合物 线性方程 相关系数R2 线性范围/(mg·kg-1) 检出限/(mg·kg-1) 定量限/(mg·kg-1)D3 L3 D4 L4 D5 L5 D6 L6 D7 L7 D8 L8 Y=1 000.91X+266 439.77 Y=999.37X+186 493.51 Y=440.50X+85 132.72 Y=198.09X+4 732.42 Y=375.29X+77 348.25 Y=302.80X-8 340.33 Y=521.01X+87 056.76 Y=93.25X-16 960.86 Y=189.13X+13 896.20 Y=128.19X-38 559.46 Y=345.77X-32 948.17 Y=172.87X-86 794.65 0.999 3 0.999 5 0.999 4 0.999 1 0.999 5 0.999 1 0.999 4 0.998 1 0.998 9 0.996 5 0.997 9 0.995 3 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.05~2.00 0.066 0.007 4 0.040 0.004 2 0.026 0.048 0.008 6 0.150 0.074 0.019 0.028 0.052 0.220 0.024 0.140 0.014 0.090 0.160 0.028 0.500 0.240 0.062 0.094 0.170
由表3可知,12种甲基硅氧烷在0.05~2.00 mg/kg范围内线性关系较好,相关系数R2为0.995 3~0.999 5,检出限为0.004 2~0.15 mg/kg,定量限为0.014~0.50 mg/kg,表明该方法能够较好地满足检测需求。
2.5.2 加标回收率与精密度试验
按照优化后的条件,将高、中、低3个浓度水平的甲基硅氧烷类化合物标准溶液分别添加至已知含量的样品溶液中,进行加标回收率和精密度试验,每个水平加标样品重复测定6次,结果见表4。由表4可知,该方法测定12种甲基硅氧烷类化合物加标回收率为85.00%~98.44%,精密度试验结果RSD为2.65%~6.86%,回收率与精密度较好,表明该检测方法精密度良好,准确度较高,能满足检测需求。
表4 甲基硅氧烷类化合物加标回收率与精密度试验结果
Table 4 Results of spiked recovery rates and precision tests of methylsiloxane compounds

甲基硅氧烷类化合物本底值/(mg·kg-1)加标量/(mg·kg-1)测定值/(mg·kg-1)1 2 3 4 5 6平均回收率/%RSD/%D3 0 L3 0 D4 0 L4 0 D5 0 L5 0 D6 0 L6 0 D7 0 L7 0 D8 0 L8 0 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 4.00 16.00 30.00 3.80 15.20 29.40 3.80 16.40 29.00 3.80 15.20 31.20 4.00 16.40 29.20 3.80 14.80 30.60 4.00 15.00 29.20 3.60 15.60 30.80 3.60 15.40 28.80 3.60 15.40 27.40 3.80 16.60 29.20 3.60 15.20 28.20 3.80 15.00 28.60 3.80 15.80 30.40 3.80 15.40 30.00 3.60 15.60 29.80 3.80 16.60 28.40 3.40 15.40 29.80 3.80 15.60 28.40 3.80 15.80 30.20 4.00 15.40 28.40 3.40 14.80 28.20 3.80 15.60 28.40 3.80 15.40 28.60 3.80 15.40 27.60 4.00 15.40 30.00 3.60 15.20 29.20 3.40 14.80 30.00 3.60 15.40 28.00 3.40 15.00 29.60 3.60 14.80 28.80 3.40 15.20 29.20 4.00 14.80 27.80 3.40 13.80 27.80 3.40 15.20 26.60 3.40 14.80 27.60 3.40 14.40 27.20 3.60 16.20 29.60 3.40 15.00 28.20 3.60 14.40 28.80 3.60 15.60 27.80 3.20 14.60 28.80 3.60 15.40 29.00 3.40 14.40 28.40 3.80 13.80 27.20 3.20 14.20 27.60 3.60 15.40 27.20 3.20 14.60 27.40 3.60 14.80 27.00 3.60 15.00 28.40 3.60 15.40 27.60 3.20 14.60 28.40 3.80 14.80 27.40 3.60 13.80 28.40 3.80 14.60 27.80 3.60 13.80 28.00 3.60 14.60 27.40 3.60 14.00 26.40 3.40 14.80 27.40 3.20 15.00 27.00 3.20 14.40 26.40 3.40 14.60 28.60 3.60 14.40 26.80 3.40 14.00 29.00 3.40 14.60 26.60 3.20 14.20 27.80 3.60 14.00 27.20 3.20 13.60 27.40 3.80 14.20 26.40 3.20 13.20 25.60 3.60 14.60 26.40 3.40 14.20 25.80 3.40 14.00 25.80 93.33 96.04 98.00 92.50 95.63 94.89 87.50 92.29 98.44 92.50 97.29 93.00 85.83 91.46 97.22 93.33 93.13 94.67 87.50 92.08 96.67 95.00 91.88 92.22 85.00 88.96 90.56 90.00 96.04 91.78 85.83 92.92 91.44 88.33 91.67 90.33 5.53 3.72 2.65 5.67 4.27 4.09 5.99 3.87 3.44 5.67 5.23 3.16 6.81 3.91 3.51 4.37 3.86 2.71 5.99 6.35 4.53 4.71 4.37 3.12 5.26 5.44 3.59 4.97 4.61 3.92 6.81 2.90 3.58 6.86 3.41 3.57
2.5.3 重复性试验
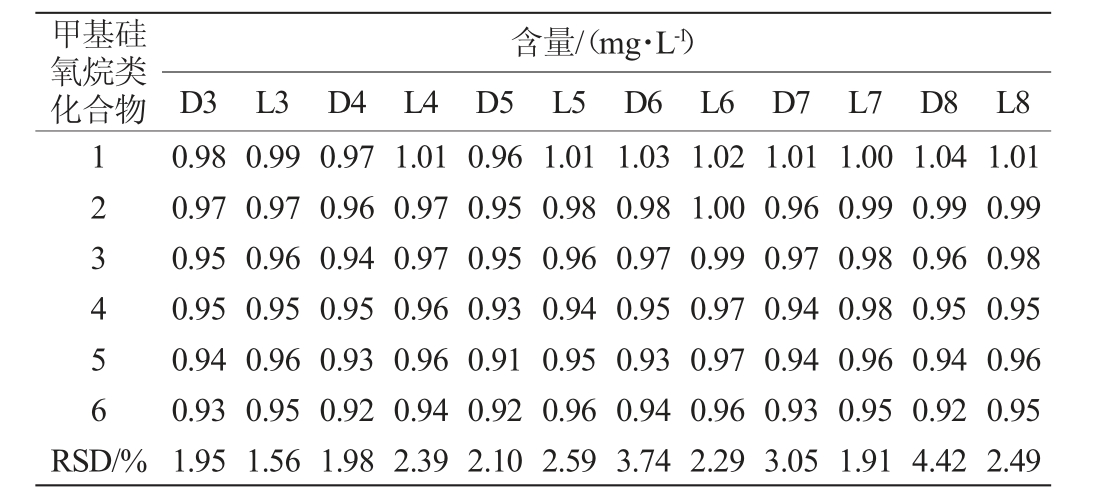
为考察检测方法的重复性,在已知含量的样品中,添加各甲基硅氧烷类化合物质量浓度为1.00 mg/L的混合标样溶液,经处理后得到供试样品,重复测定6次,结果见表5。由表5可知,各甲基硅氧烷类化合物重复性试验结果RSD为1.56%~4.42%,表明该检测方法重复性良好。
表5 甲基硅氧烷类化合物重复性试验结果
Table 5 Results of repeatability tests of methylsiloxane compounds
甲基硅氧烷类化合物含量/(mg·L-1)D3 L3 D4 L4 D5 L5 D6 L6 D7 L7 D8 L8 123456 RSD/%0.98 0.97 0.95 0.95 0.94 0.93 1.95 0.99 0.97 0.96 0.95 0.96 0.95 1.56 0.97 0.96 0.94 0.95 0.93 0.92 1.98 1.01 0.97 0.97 0.96 0.96 0.94 2.39 0.96 0.95 0.95 0.93 0.91 0.92 2.10 1.01 0.98 0.96 0.94 0.95 0.96 2.59 1.03 0.98 0.97 0.95 0.93 0.94 3.74 1.02 1.00 0.99 0.97 0.97 0.96 2.29 1.01 0.96 0.97 0.94 0.94 0.93 3.05 1.00 0.99 0.98 0.98 0.96 0.95 1.91 1.04 0.99 0.96 0.95 0.94 0.92 4.42 1.01 0.99 0.98 0.95 0.96 0.95 2.49
白酒瓶盖内塞中常用材料为聚对苯二甲酸乙二醇酯(polyethyleneglycolterephthalate,PET)、低密度聚乙烯(lowdensity polyethylene,LDPE)、高密度聚乙烯(high-density polyethylene,HDPE)和硅橡胶,利用该方法对四种材质的8个市售瓶盖内塞样品进行检测。结果表明,硅橡胶材质瓶盖内塞中检出D5、D6、D7和D8残留量,含量为8.56~34.74mg/kg,PET、LDPE、HDPE材质瓶盖内塞中均未检测出12种甲基硅氧烷类化合物。
本研究利用GC-MS/MS法建立了白酒接触材料中12种甲基硅氧烷类化合物残留量的分析检测方法,通过优化溶剂、色谱柱、超声提取时间和后运行温度等因素,确定了最佳运行条件。结果表明,12种甲基硅氧烷类化合物在0.05~2.00 mg/kg质量浓度范围内线性关系良好,相关系数R2为0.995 3~0.999 5,加标回收率为85.00%~98.44%,精密度试验结果相对标准偏差(RSD)为2.65%~6.86%,重复性试验结果RSD为1.56%~4.42%,检出限为0.004 2~0.15 mg/kg,定量限为0.014~0.50 mg/kg,表明该方法精密度良好,准确度、重复性较高,能够较好地满足检测需求。采用该方法对市售白酒的多种类型接触材料进行检测,对PET、LDPE、HDPE和硅橡胶四种材质的8个市售瓶盖内塞样品进行检测结果表明,仅硅橡胶材质瓶盖内塞样品中检出D5、D6、D7和D8,含量为8.56~34.74 mg/kg,其余材质瓶盖内塞样品中均未检出12种甲基硅氧烷类化合物。该方法操作简单、灵敏度和准确度高,适用于白酒接触材料中甲基硅氧烷类化合物残留量的检测和监控,为白酒接触材料中食品安全监测提供技术支撑和理论参考。后期还应加强对白酒接触材料中风险物质的迁移含量研究,逐步完善和提升白酒食品安全监测水平。
[1]刁波,吴月,高天容,等.白酒生产全过程接触材料应用研究[J].酿酒科技,2023(8):56-60.
[2]董犇,张子豪,曾莹,等.气相色谱-串联质谱法同时测定硅橡胶餐具中21 种硅氧烷类化合物的残留量[J].食品科学,2021,42(22):311-317.
[3]XUE X H, JIA H L, XUE J C.Bioaccumulation of methyl siloxanes in common carp(Cyprinus carpio)and in an estuarine food web in northeastern China[J].Arch Environ Contam Toxicol,2019,76(3):496-507.
[4]BERNARDO F,ALVES A,HOMEM V.A review of bioaccumulation of volatile methylsiloxanes in aquatic ecosystems[J].Sei Total Environ,2022,824:153821.
[5]JIANG Y,GUO J Y,ZHOU Y,et al.Occurrence and behavior of methylsiloxanes in urban environment in four cities of China[J].Int J Environ Res Public Health,2022,19(21):13869.
[6]CHENG J L, TANG Z W, MA Y, et al.Methyl siloxanes in road dust from a large silicone manufacturing site in China:Implications of human exposure[J].Environ Sci Pollut Res,2021,28(13):16054-16064.
[7]CHENG J L,TANG Z W,MA Y,et al.Methyl siloxanes in soils from a large silicone-manufacturing site,China:Concentrations,distributions and potential human exposure[J].Environ Geochem Health,2021,43(10):3871-3881.
[8]鲍珊,顾雯,邱天,等.硅氧烷及其衍生物分析方法研究进展[J].环境卫生学杂志,2023,13(11):853-863.
[9]HAN W J,SUN H Y,ZHANG S Y,et al.Hydroxyl radical oxidation of cyclic methylsiloxanes D4-D6 in aqueous phase[J].Chemosphere,2020,242:1-8.
[10]FENG D,ZHANG X R,WANG W J,et al.Development validation and comparison of three detection methods for 9 volatile methylsiloxanes in food contact silicone rubber products[J].Polym Test,2019,73:94-103.
[11]葛丹阳,刘桂华,姜欢,等.GC-MS/MS法测定食品接触用硅橡胶制品中6种环硅氧烷迁移量[J].分析测试学报,2022,41(10):1486-1493.
[12]QUINN A L, DALU A, MEEKER L S, et al.Effects of octamethylcyclotetrasiloxane(D4) on the luteinizing hormone(LH) surge and levels of various reproductive hormones in female Sprague Dawley rats[J].Reprod Toxicol,2007,23(4):532-540.
[13]GUO J Y,ZHOU Y,WANG Y F,et al.Assessment of internal exposure to methylsiloxanes in children and associated nondietary exposure risk[J].Environ Int,2021,154:1-10.
[14]XU S H,WARNER N,BOHLIN-NIZZETTO P,et al.Long-range transport potential and atmospheric persistence of cyclic volatile methylsiloxanes based on global measurements[J].Chemosphere,2019,228:460-468.
[15]HE Y, SU S, CHENG J L, et al.Bioaccumulation and trophodynamics of cyclic methylsiloxanes in the food web of a large subtropical lake in China[J].J Hazard Mater,2021,413:1-9.
[16]XU L,SHI Y L,LIU N N,et al.Methyl siloxanes in environmental matrices and human plasma/fat from both general industries and residential areas in China[J].Sei Total Environ,2015,505:454-463.
[17]刘宜奇,胡长鹰,商贵芹,等.食品接触用硅橡胶中3种环硅氧烷的测定及迁移规律[J].食品工业科技,2020,41(11):245-250.
[18]梁鸣,邹哲祥,唐熙,等.气相色谱-质谱联用法测定纺织品中甲基环硅氧烷残留[J].中国口岸科学技术,2020(12):33-42.
[19]赵海浪,尹喆,谭玉静.Py/TD-GC-MS法快速测定纺织品中的甲基环硅氧烷[J].印染,2022(7):70-74.
[20]吴红洋.药用胶塞中二甲基环体硅氧烷残留量及在药品中迁移量的测定[J].药物分析杂志,2022,42(11):1972-1979.
[21]冯霞兰,邱怡婷,王刚,等.气相色谱法测定药用硅橡胶管、硅橡胶垫片中挥发性甲基环硅氧烷的残留量[J].药物分析杂志,2022,42(3):441-448.
[22]张晓芸,孙星宇,丁逸梅.气相色谱法测定注射用雷替曲塞中甲基环硅氧烷[J].海峡药学,2024,36(1):48-52.
[23]李思源,陈安丽,赵思雯,等.气相色谱-串联质谱法测定化妆品中7种二甲基环硅氧烷[J].分析测试学报,2023,42(12):1607-1614.
[24]杜英英,李海燕,别红梅,等.GC-MS 法测定皮革中甲基环硅氧烷的检测方法研究[J].皮革与化工,2022,39(4):16-19.
[25]张伟,范德玲,王蕾,等.气相色谱-质谱联用法测定水体和土壤中3种环状挥发性甲基硅氧烷[J].化学研究与应用,2023,35(6):1423-1432.
[26]卢科,许义,黄飞.HS-GC法测定八甲基环四硅氧烷、十甲基环五硅氧烷和十二甲基环六硅氧烷[J].印染助剂,2022,39(11):55-59.