普洱茶(Pu-erh tea)是以云南大叶种茶树(Camellia sinensis var.assamica)晒青茶为原料,在地理标志保护范围内采用特定加工工艺制成的茶叶[1-2]。根据加工工艺和品质特征,分为普洱茶(生茶)和普洱茶(熟茶)两种类型[3]。其中,普洱熟茶是以大叶种茶树晒青茶为原料,通过潮水、后发酵等工艺制成,具有汤色红褐、滋味醇厚(和)、陈香显著等品质特征[4],具有抗氧化、抗菌、抗突变、抗肿瘤等多种生理活性[5],而临床研究也证实,普洱熟茶能够改善血脂和血糖代谢,有助于预防和控制肥胖、代谢综合征及糖尿病[6]。
后发酵是形成普洱熟茶独特风味的关键,其实质上是以晒青茶为基质的固态发酵过程,发酵过程中发生转化、异构、降解、聚合、偶联等以茶多酚转化为主导的复杂而剧烈的化学反应[7]。由于采用传统自然发酵的方式,发酵微生物菌群与代谢物变化受到发酵原料、工艺以及环境的影响。研究表明,在发酵过程中,黄酮苷类物质(如黄酮苷和奎尼酸衍生物)的含量呈现显著降低趋势;而生物碱类物质(如咖啡碱和可可碱)的含量呈现显著增加趋势[8]。SHI J等[9]研究表明,在普洱熟茶发酵过程中,原儿茶酸、龙胆酸、短叶苏木酚酸和香豆酰奎宁酸等化合物含量逐渐增加,绿原酸、咖啡酸和没食子酸[10]的含量逐渐降低。LI J等[11]研究表明,普洱熟茶在发酵过程中,氨基酸、游离糖以及儿茶素和黄酮醇糖苷的含量呈现减少趋势。然而,普洱熟茶发酵过程中部分功能性物质的代谢机制仍不明确,工业化生产中的代谢物变化规律更有待深入探究。代谢组学是一种定量测量生命系统对病理生理刺激或基因修饰的动态代谢反应技术,有助于在植物学中更好的探测植物生理及其在各种条件下的代谢扰动或反应[12]。近年来,代谢组学已发展成为研究茶叶生理特性的重要工具[13],在普洱熟茶发酵机制、功能性成分转化及健康功效等方面取得诸多进展,为深入研究普洱熟茶工业化发酵过程中的代谢规律奠定了方法学基础。目前,关于普洱熟茶发酵过程中代谢物研究报道较少。
本研究以普洱熟茶为研究对象,对其发酵过程中感官品质及理化指标进行分析,结合超高效液相色谱-串联质谱(ultra-high performance liquid chromatography-tandem mass spectrometry,UHPLC-MS/MS)技术测定普洱熟茶发酵过程中的代谢物,并对其进行正交偏最小二乘-判别分析(orthogonal partial least squares-discriminant analysis,OPLSDA),并基于变量重要性投影(variables importance projection,VIP)值、方差分析P值及差异倍数(fold change,FC)筛选显著差异代谢物。以期揭示普洱熟茶发酵过程中特征成分的转化规律,为深入解析普洱熟茶发酵过程中物质代谢机制提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
晒青毛茶:云南下关沱茶股份集团有限公司。
1.1.2 试剂
葡萄糖(分析纯):西陇科学股份有限公司;乙酸乙酯(分析纯):天津市大茂化学试剂厂;蒽酮、硫酸亚铁、酒石酸钾钠(均为分析纯):国药集团化学试剂有限公司;茚三酮(分析纯):广州科檬生物科技有限公司;L-谷氨酸(分析纯):上海埃博商贸有限公司;儿茶素类8种标准品包括儿茶素(catechin,C)、表儿茶素(epicatechin,EC)、没食子儿茶素(gallic catechin,GC)、儿茶素没食子酸酯(catechin gallate,CG)、表没食子酸儿茶素(epigallocatechin,EGC)、表儿茶素没食子酸酯(epicatechin-3-gallate,ECG)、表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)、没食子儿茶素没食子酸酯(gallocatechin gallate,GCG);黄酮类6种标准品包括槲皮素(quercetin)、杨梅素(myricetin)、木犀草素(luteolin)、山奈酚(kaempferol)、芦丁(rutin)、花旗松素(taxifolin);酚酸类2种标准品包括没食子酸(gallic acid,GA)、鞣花酸(ellagic acid);生物碱类2种标准品包括茶碱(theophylline)和咖啡碱(caffeine,CA)标准品(纯度均>99%):成都曼思特生物科技有限公司;甲醇、甲酸、醋酸铵(均为色谱纯):德国Thermo Fisher公司。
1.2 仪器与设备
1200型高效液相色谱仪:美国Agilent公司;超高效液相色谱-串联质谱系统(Q ExactiveTMHF-X型质谱仪、Vanquish UHPLC型色谱仪):德国Thermo Fisher公司;K6600全波长酶标仪:北京凯奥科技发展有限公司;MOC63U 240V EXP水分快速测定仪:日本Shimadzu公司;101-2AB型电热鼓风干燥箱:天津市泰斯特仪器有限公司。
1.3 方法
1.3.1 普洱熟茶发酵过程中样品的制备
将晒青毛茶原料喷洒潮水至含水率约40%,堆高约1 m,每7 d翻堆一次,共翻8次。每次翻堆后5点取样混合,于室温(20~25 ℃)发酵56 d后出堆,分别在普洱熟茶发酵0、7 d、14 d、21 d、28 d、35 d、42 d、49 d、56 d取样,样品编号分别为F0、F7、F14、F21、F28、F35、F42、F49、F56。
1.3.2 茶叶感官审评方法
按国标GB/T 23776—2018《茶叶感官审评方法》对茶样进行感官审评[14],实验中,准确称取每份茶叶样品3.0 g,按照茶水比(质量体积比)1∶50的比例,将茶叶样品分别置于标准审评杯中,随后注入沸水至满,加盖浸泡。浸泡完成后,迅速将茶汤与叶底分离,以便对茶样的感官特征进行详细观察与评估。感官审评主要依据八项因子进行评价,包括外形(嫩度、条索、色泽、净度)、香气、汤色、滋味和叶底。
1.3.3 理化指标及活性成分的测定
含水量:采用水分快速测定仪测定;水浸出物、茶多酚、可溶性糖和游离氨基酸的含量:分别采用恒重法[15]、酒石酸亚铁比色法[16]、蒽酮-硫酸法[17]、茚三酮法[18]测定;儿茶素、黄酮与生物碱含量:采用高效液相色谱法[19]测定;茶色素(茶黄素、茶红素和茶褐素)含量:参照NYT3675—2020《红茶中茶红素和茶褐素含量的测定方法》[20]测定。
1.3.4 代谢物分析
样品前处理:液氮研磨茶样至粉末状后,称取0.1 g茶粉加入0.5 mL体积分数为80%甲醇水溶液,低速涡旋振荡30 s、冰浴静置5 min。离心(4 ℃、15 000×g)20 min取上清液后加水(质谱级)稀释至甲醇体积分数为53%,重复离心操作2次,取上清液待测。同时,从各提取的茶样中混合制备质量控制(quality control,QC)样品,并使用体积分数53%的甲醇水溶液代替实验样本作为空白样本进行LC-MS分析。
UHPLC条件:Hypesil Gold column C18色谱柱(100×2.1 mm,1.9 μm),流动相正离子模式A为0.1%甲酸,B为甲醇;流动相负离子模式A为5 mmol/L醋酸铵(pH 9.0),B为甲醇。洗脱梯度为0~1.5 min(2%B);12~14 min(100%B);14.1~17 min(2%B),柱温40 ℃,流速0.2 mL/min。MS条件:采用正负离子模式检测,喷雾电压3.2 kV,毛细管温度320℃,鞘层气体流速40 arb,辅助气体流速10 arb。
鉴定:利用基迪奥生物科技有限公司自建数据库资源,采用Compound Discoverer 3.1软件根据保留时间、质荷比等参数对代谢物的数据进行采集;通过整合目标离子,与mzCloud(https://www.mzcloud.org/)、mzVault和Masslist数据库中物质的分子离子峰和碎片离子的分子式进行比对,使用空白样本去除背景离子后对结果进行归一化处理后进行鉴定。
1.3.5 数据处理
使用Excel 2019进行数据的计算、分析和整理;SPSS 25.0软件进行显著性分析;Tbtool 2.0绘制热图;采用在线网站MetaboAnalyst 6.0(https://www.metaboanalyst.ca/)平台上进行正交偏最小二乘判别分析(OPLS-DA),根据VIP值>1.0、P<0.05和差异倍数(FC)>2或<0.5筛选差异代谢物。
2 结果与分析
2.1 普洱熟茶发酵过程中感官特征的变化
发酵过程中普洱熟茶样品的感官特征变化见图1。由图1可知,随着发酵时间延长,样品感官品质呈现明显变化,具体表现为4个关键转折节点:在发酵21 d后,发酵茶样的香气逐渐由清香转变为发酵味或酸味;在发酵28 d后,茶样的干茶色泽、茶汤颜色逐渐由黄绿色转变为红褐色;在发酵42 d后,茶样外形、汤色色泽逐渐加深,汤色逐渐由红色转为褐色。在发酵49 d后,普洱熟茶独特的陈香逐渐显现,滋味由浓醇转变为醇和。感官审评结果与蒋睿等[21]研究结论相同,发酵中茶叶色泽与汤色逐渐由黄绿变为红褐,滋味由浓醇变为醇和,香气由清香、烟香变为陈香。
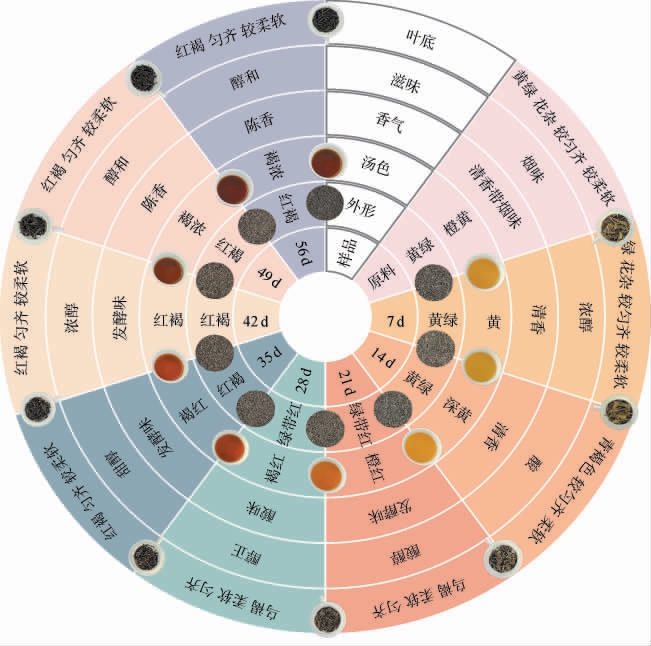
图1 发酵过程中普洱熟茶样品的感官特征变化
Fig.1 Changes of sensory characteristics of ripened Pu-erh tea samples during fermentation process
2.2 普洱熟茶发酵过程中理化指标及活性成分含量变化
普洱熟茶发酵过程中理化指标及活性成分测定结果见图2。由图2可知,发酵0~14 d时,水浸出物含量呈升高趋势;当发酵时间>14 d时,其含量呈下降趋势。发酵0~56 d时,茶多酚、茶黄素、茶红素以及游离氨基酸的含量显著降低,而茶褐素含量显著升高(P<0.05)。该结果与韩肋撒等[22]研究发现普洱发酵中游离氨基酸、茶多酚含量降低,而茶褐素的含量提高相符[6]。在发酵28 d时,可溶性糖的含量达到最高(10.66%),发酵时间>28 d时,含量则逐渐降低,发酵结束时,可溶性糖含量为6.74%。
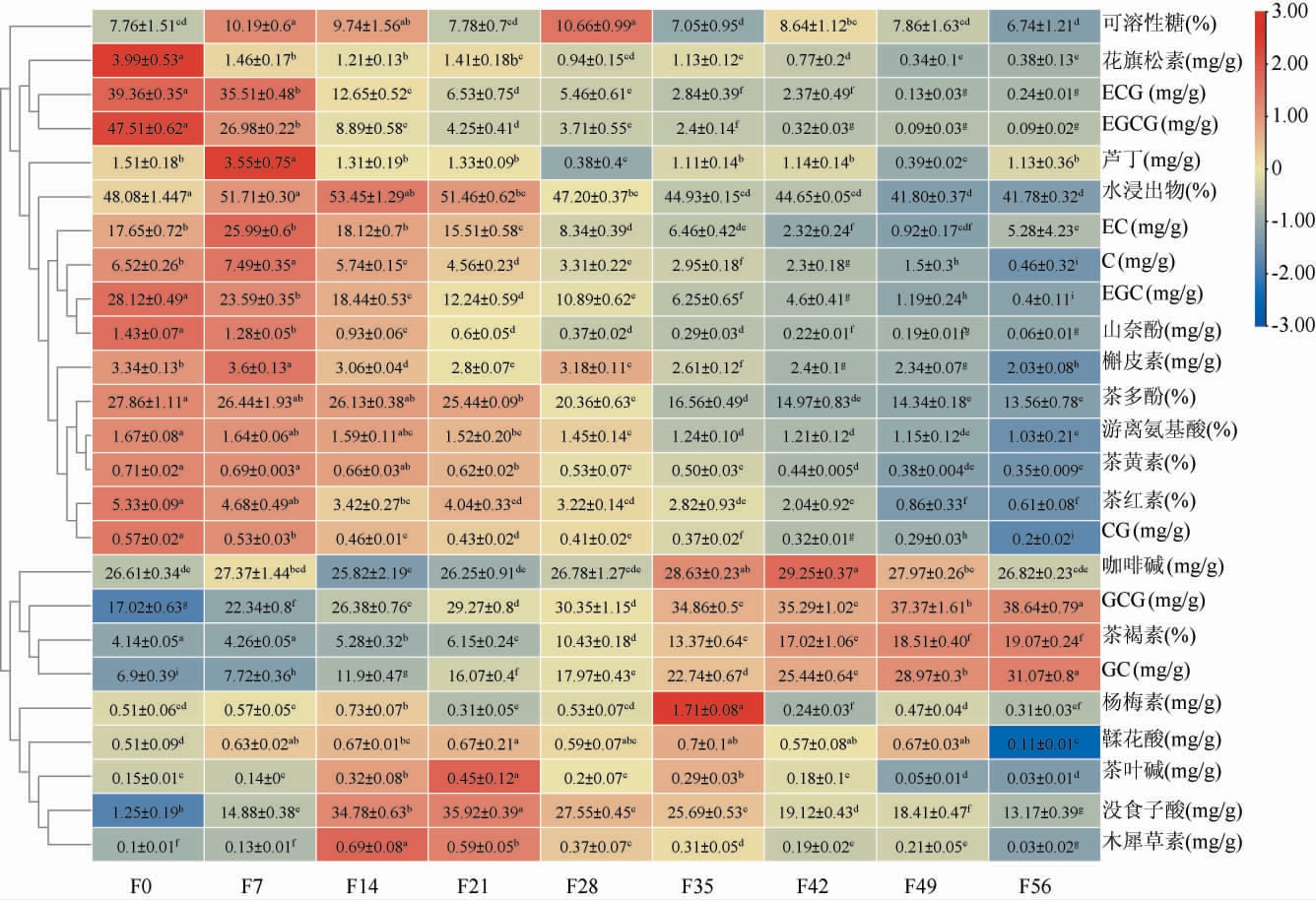
图2 普洱熟茶发酵过程中理化指标及活性成分的聚类分析热图
Fig.2 Heat map of cluster analysis of physicochemical indicators and active components during the fermentation process of ripened Pu-erh tea
同行不同小写字母表示差异显著(P<0.05)。下同。
发酵0~56d时,儿茶素(C)、表儿茶素没食子酸酯(ECG)、表没食子儿茶素没食子酸酯(EGCG)、表没食子酸儿茶素(EGC)、儿茶素没食子酸酯(CG)、表儿茶素(EC),芦丁、杨梅素、花旗松素、山奈酚的含量显著降低(P<0.05),而少数的儿茶素类化合物(没食子儿茶素(GC)、没食子儿茶素没食子酸酯(GCG))的含量增加。这与ZHU Y C等[23]研究结果相一致,发酵结束后儿茶素含量显著降低。发酵21 d时,木犀草素、茶碱、没食子酸(GA)和鞣花酸四种成分量呈现逐渐上升趋势;然而,当发酵56 d时,这些成分的含量显著降低。发酵28 d时,槲皮素的含量最高,随后显著降低,与MA C Q等[24]研究结果中的槲皮素含量在发酵初始时急剧增加,后明显减少结果相似。发酵0~35 d时,咖啡碱的含量持续上升,直至发酵42 d时达到最高值29.25 mg/g,此后在发酵49~56 d时逐渐降低。这一发现与ZHANG L等[4]的研究结果中咖啡碱的含量在发酵后降低结果相吻合。LONG P P等[8]研究表明,槲皮素、杨梅素和山奈酚是茶黄酮醇的主要苷元,黄酮类化合物,包括黄酮醇苷,会影响到茶汤的颜色。普洱茶至少需要3轮堆发酵(21 d)才能降低普洱茶中黄酮醇苷的含量。此外,儿茶素类化合物、黄酮类化合物和黄酮苷类化合物的减少改善了普洱茶的苦味和涩味,茶褐素的增加赋予了普洱熟茶特有的棕色茶汤[25-26]。总体而言,在发酵进行0~56 d的过程中,发酵样品的总儿茶素(包括C、EC、EGC、GC和ECG、EGCG、CG、GCG)与总黄酮(包括槲皮素、花旗松素、芦丁、木犀草素、山奈酚和杨梅素)含量显著降低(P<0.05),总儿茶素含量由163.65 mg/g下降到76.38 mg/g,总黄酮含量由10.88 mg/g下降到3.94 mg/g。即发酵后,普洱熟茶的苦涩味显著减少,醇和度增加,汤色逐渐转变为红褐色,与上述感官品质描述相一致。
2.3 普洱熟茶发酵前后代谢物变化
2.3.1 普洱熟茶代谢物类别
为进一步研究普洱熟茶发酵前后的代谢物的变化,采用UHPLC-MS/MS技术对发酵前后样品进行非靶向代谢组学检测分析发现,发酵前后普洱熟茶样品中共鉴定出460个化合物,其中正离子模式下化合物231个,负离子模式下化合物229个,将这些代谢物进行分类,结果见图3。由图3可知,普洱熟茶样品代谢物主要包括羧酸及其衍生物类(67个)、脂肪酰基类(56个)和有机氧化合物(51个)等27种代谢物类别。
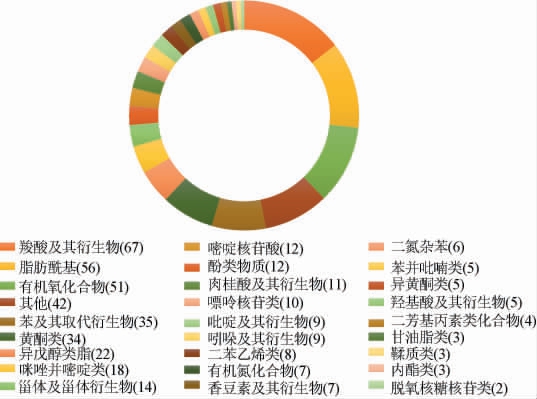
图3 普洱熟茶样品中代谢物的类别
Fig.3 Categories of metabolites in ripened Pu-erh samples
2.3.2 正交偏最小二乘-判别分析
基于正负离子模式检测的峰信号,使用正交偏最小二乘判别分析(OPLS-DA)模型对发酵茶样进行分析,结果见图4。由图4可知,OPLS-DA的前两个主成分解释了总变异的70.3%(PC1=63.1%,PC2=7.2%),模型的自变量拟合指数(T score)分别为63.1%和7.2%。发酵前样品位于置信区间的左侧,而发酵后样品位于置信区间的右侧,表明发酵可导致普洱熟茶样品中代谢物差异。因此,OPLS-DA可有效区分发酵前后普洱熟茶样品。
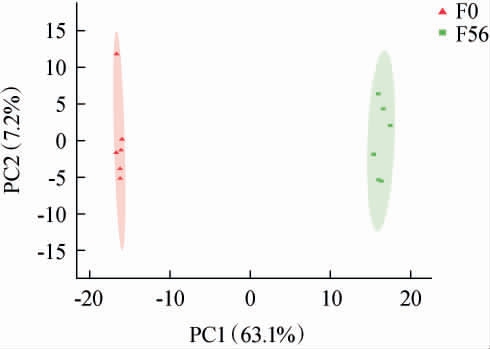
图4 普洱熟茶发酵前后样品的正交偏最小二乘法判别分析得分图
Fig.4 Orthogonal partial least squares-discriminant analysis score plot of ripened Pu-erh tea samples before and after the fermentation
2.3.3 普洱熟茶发酵前后差异代谢物变化
基于OPLS-DA模型根据VIP>1.0,P<0.05且FC>2或FC<0.5共筛选得到238个显著差异代谢物,主要包括羧酸及其衍生物(45个)、脂肪酰基(34个)、有机氧化合物(27个)和黄酮类(20个)等。并基于log2(FC)值对排名前20的代谢物进行可视化,结果见图5。
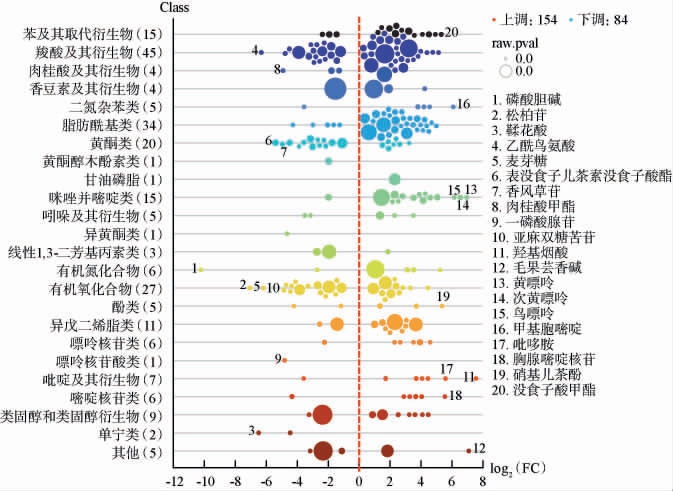
图5 普洱熟茶发酵前后样品排名前20的显著差异代谢物分析
Fig.5 Analysis of top 20 ranked significantly differential metabolites in ripened Pu-erh tea samples before and after the fermentation
由图5可知,基于VIP>1.0,P<0.05且FC>2发现,发酵后普洱熟茶中有154个显著差异代谢物含量升高,包括羧酸及其衍生物(27个)、咪唑并嘧啶类(14个)、脂肪酰基(29个)、有机氧化合物(11个)、苯和取代衍生物(12个)等。其中没食子酸甲酯、硝基儿茶酚、胸腺嘧啶核苷、吡哆胺、甲基胞嘧啶、鸟嘌呤、次黄嘌呤、黄嘌呤、毛果芸香碱、羟基烟酸10种化合物的含量提高58倍以上。没食子酸甲酯作为没食子酸的甲酯衍生物,是一种独具活性的多酚类化合物,具有抗氧化、抗癌、抗炎以及抗糖基化等多种生物活性[27-28],发酵后没食子酸甲酯含量的显著升高,值得进一步研究。茶叶生物碱主要含有嘌呤碱,以及少量的嘧啶碱类化合物,包括尿嘧啶、胸腺嘧啶、胞嘧啶及5-甲基胞嘧啶等[29]。发酵过程中,茶叶生物碱类化合物的相互代谢转化,可能是导致普洱熟茶中胸腺嘧啶核苷、吡哆胺、甲基胞嘧啶、鸟嘌呤、次黄嘌呤、黄嘌呤等物质含量升高的原因。发酵结束后,甜菜碱、L-胱氨酸、缬氨酸等羧酸及其衍生物的含量升高,这一发现与LI T H等[30]发现发酵结束后熟茶中鸟氨酸、甘氨酸和胱氨酸等氨基酸含量增加的结果不同。此外,发酵后原儿茶酸、龙胆酸等物质含量显著上升,与其他学者观察结果一致[9]。部分脂类物质如雷公藤红素、柠檬醛、栀子苷与脂肪酰基类化合物2-羟基肉豆蔻酸、二氢茉莉酮酸甲酯;黄酮类化合物如槲皮素7-鼠李糖苷、柚皮素、芹菜素、异鼠李素等具有多种生理活性的代谢物在发酵后含量也显著升高(VIP>1.0,P<0.05且FC>2)。
基于VIP>1.0,P<0.05且FC<0.5发现,84个代谢物含量呈现下降趋势,包括羧酸和衍生物(18个)、有机氧化合物(16个)、黄酮类(13个)等。其中,磷酸胆碱、松柏苷、鞣花酸、乙酰鸟氨酸、麦芽糖、表没食子儿茶素没食子酸酯、香风草苷、肉桂酸甲酯、5'-一磷酸腺苷、亚麻双糖苦苷等10种化合物含量降低超过18倍。黄酮类化合物中儿茶素、表没食子儿茶素、儿茶素没食子酸酯、原花青素A2、原花青素B2、原花青素B1、花旗松素、杨梅素、山奈酚、三叶草素、柚皮苷二氢查尔酮含量在发酵后显著下降,与龙飘飘[31]得出发酵后儿茶素类物质的含量降低、EGCG和ECG的含量大幅度下降的研究结果相符。LI J等[25-32]研究发现,黄烷-3-醇和原花青素B3导致了茶汤的苦味和涩味的产生[25-32],发酵中,黄酮醇苷和大部分原花青素迅速减少[25],为普洱熟茶的醇厚口感的提供了物质基础[26-33]。高精氨酸、天冬氨酸、谷氨酸、苯丙氨酸、丝氨酸、酪氨酸、苏氨酸、天冬酰胺、组氨酸、谷氨酰胺等氨基酸含量在发酵后含量显著下降,与游离氨基酸测定结果相符,可能是氨基酸被微生物利用而含量降低[32]。氨基酸是茶叶鲜味物质的主要来源[34],其中谷氨酸、天冬氨酸具有鲜味特征,苏氨酸具甜味,而组氨酸和苯丙氨酸呈苦味[35]。ZHANG L等[36]研究结果表明,谷氨酸的缺失会导致茶叶鲜味的大幅降低。发酵过程中氨基酸含量的不断降低,削弱了发酵茶的鲜爽味与苦味,逐步形成普洱熟茶的醇和风味,与感官审评结果相应。1-磷酸葡萄糖、蔗糖、麦芽四糖、异绿原酸C以及绿原酸等发酵含量下降,这一发现与SHI J等[9]研究结果一致。
总体而言,普洱熟茶后发酵后的代谢物含量发生显著变化,其中没食子酸甲酯、黄嘌呤和次黄嘌呤等代谢物含量在发酵后显著上升(VIP>1.0,P<0.05且FC>2);氨基酸类化合物(如天冬氨酸、谷氨酸、苏氨酸、苯丙氨酸、组氨酸)、鞣花酸、麦芽糖、表没食子儿茶素没食子酸酯、香风草苷和肉桂酸甲酯等代谢物含量在发酵后显著下降(VIP>1.0,P<0.05且FC<0.5)。发酵过程中茶多酚类化合物、生物碱类化合物与氨基酸类化合物生物相互代谢转化,含量不断降低,进一步降低了发酵茶的鲜爽味与苦涩味,醇和度显著增加,与感官品质特征结果相一致。
对普洱熟茶发酵前后样品中通过UHPLC-MS/MS、HPLC两种方法均检出的化合物进行分析,并计算化合物的log2(FC)值,筛选出物质含量变化趋势相同的化合物,其含量变化结果见图6。由图6可知,两种方法共检出9个含量变化趋势相同的化合物,包括EGC、EGCG、C、CG、花旗松素、山奈酚、杨梅素、鞣花酸和咖啡碱。其中,咖啡碱分布在右上象限,log2(FC)>0表明咖啡碱的含量增加,其余8个化合物分布在左下象限,log2(FC)<0表明其含量均下降。结果表明,普洱熟茶发酵过程中这9个化合物的变化与普洱茶品质密切相关。
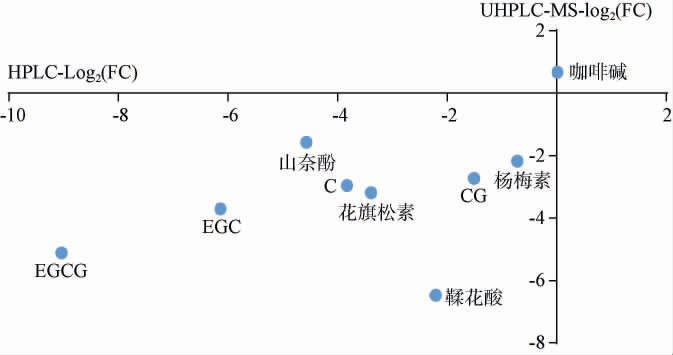
图6 普洱熟茶发酵前后HPLC与UHPLC-MS/MS共同检出化合物的含量变化
Fig.6 Content change of compounds in ripened Pu-erh tea samples before and after fermentation detected by HPLC and UHPLCMS/MS techniques
3 结论
本研究通过代谢组学与化学计量方法对普洱熟茶发酵过程中感官品质、理化指标及活性成分、非挥发性物质变化进行分析。结果表明,在发酵过程中,茶汤滋味由浓强、稍涩逐渐转为醇和,这与茶多酚、儿茶素(EGC、EGCG、C、CG)、黄酮(花旗松素、山奈酚、杨梅素、原花青素)、氨基酸(天冬氨酸、谷氨酸、苏氨酸、苯丙氨酸、组氨酸)及鞣花酸等化合物含量的显著下降有关;汤色由绿黄逐渐变为红褐,则与茶黄素与茶红素含量下降以及茶褐素含量增加有关。发酵结束后,普洱熟茶呈现出汤色红褐、滋味醇和及典型的陈香气味;总儿茶素含量、总黄酮含量分别从163.65 mg/g、10.88 mg/g下降至76.38 mg/g、3.94 mg/g。普洱熟茶发酵前后样品中筛选获得238个显著差异代谢化合物(VIP>1.0,P<0.05),其中,没食子酸甲酯、黄嘌呤和次黄嘌呤等显著差异代谢物(VIP>1.0,P<0.05,FC>2)含量显著上调;而鞣花酸、麦芽糖、香风草苷和肉桂酸甲酯等显著差异代谢物(VIP>1.0,P<0.05,FC<0.5)含量显著下调。高效液相色谱(HPLC)及UHPLC-MS/MS同时检出9个含量变化趋势相同的化合物,其中,咖啡碱含量上升,而儿茶素等8种化合物含量均下降。结果表明,普洱熟茶发酵过程中这9个化合物的变化与普洱茶品质密切相关。普洱熟茶的发酵过程涉及多种物质的协同作用,后续研究将进一步聚焦挥发性成分变化与香气变化的关系,以完善普洱熟茶品质形成的理论体系。
[1]MA B S,WANG J,XU C C,et al.Interrelation analysis between phenolic compounds and in vitro antioxidant activities in Pu-erh tea[J].LWT-Food Sci Technol,2022,158:113117.
[2]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 22111—2008 地理标志产品普洱茶[S].北京:中国标准出版社,2008.
[3]ZHU J Y, CHEN L, CHEN Y, et al.Effect of geographical origins and pile-fermentation on the multi-element profiles of ripen Pu-erh tea revealed by comprehensive elemental fingerprinting[J].Food Control,2023,154:109978.
[4]ZHANG L,LI N,MA Z Z,et al.Comparison of the chemical constituents of aged Pu-erh tea,ripened pu-erh tea,and other teas using HPLC-DADESI-MSn[J].J Agr Food Chem,2011,59(16):8754-8760.
[5]PEREZ-VIZCAINO F,DUARTE J.Flavonols and cardiovascular disease[J].Mol Aspect Med,2010,31(6):478-494.
[6]HUANG F J,ZHENG X J,MA X H,et al.Theabrownin from Pu-erh tea attenuates hypercholesterolemia via modulation of gut microbiota and bile acid metabolism[J].Nat Communi,2019,10(1):4971.
[7]冯玲然.普洱茶中功能性微生物的筛选及风味物质的初步研究[D].无锡:江南大学,2014.
[8]LONG P P, WEN M C, GRANATO D, et al.Untargeted and targeted metabolomics reveal the chemical characteristic of Pu-erh tea (Camellia assamica)during pile-fermentation[J].Food Chem,2020,311:125895.
[9]SHI J,MA W J,WANG C P,et al.Impact of various microbial-fermented methods on the chemical profile of dark tea using a single raw tea material[J].J Agr Food Chem,2021,69(14):4210-4222.
[10]VILLARREAL-SOTO S A,BEAUFORT S,BOUAJILA J,et al.Impact of fermentation conditions on the production of bioactive compounds with anticancer, anti-inflammatory and antioxidant properties in kombucha tea extracts[J].Proc Biochem,2019,83:44-54.
[11]LI J,WU S M,YU Q Y,et al.Chemical profile of a novel ripened Pu-erh tea and its metabolic conversion during pile fermentation[J].Food Chem,2022,378:132126.
[12]GAI Z S, WANG Y, JIANG J T, et al.The quality evaluation of tea(Camellia sinensis) varieties based on the metabolomics[J].Hort Sci,2019,54(3):409-415.
[13]HONG Y S.Tea's metabolomics[J].Comprehensive Foodomics,2021,2:129-135.
[14]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 23776—2018 茶叶感官审评方法[S].北京:中国标准出版社,2018.
[15]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 8305—2013 茶 水浸出物测定[S].北京:中国标准出版社,2013.
[16]张妙芬.茶叶中茶多酚含量测定方法的研究[J].化学工程与装备,2012(5):152-155.
[17]傅博强,谢明勇,聂少平,等.茶叶中多糖含量的测定[J].食品科学,2001,22(11):69-73.
[18]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 8314—2013 茶游离氨基酸总量的测定[S].北京:中国标准出版社,2013.
[19]NIAN B,CHEN L J,YI C,et al.A high performance liquid chromatography method for simultaneous detection of 20 bioactive components in tea extracts[J].Electrophoresis,2019,40(21):2837-2844.
[20]中华人民共和国农业农村部.NY/T 3675—2020 红茶中茶红素和茶褐素含量的测定 分光光度法[S].北京:中国农业出版社,2020.
[21]蒋睿,罗理勇,常睿,等.普洱生茶和熟茶的品质化学成分分析比较[J].西南大学学报(自然科学版),2018,40(6):38-47.
[22]韩肋撒,张会敏,张文芳,等.发酵程度与原料对普洱茶菌群结构与品质影响[J].食品与发酵工业,2025,51(9):186-195.
[23]ZHU Y C,LUO Y H,WANG P P,et al.Simultaneous determination of free amino acids in Pu-erh tea and their changes during fermentation[J].Food Chem,2016,194:643-649.
[24]MA C Q, MA B S, ZHOU B X, et al.Pile-fermentation mechanism of ripened Pu-erh tea: Omics approach, chemical variation and microbial effect[J].Trends Food Sci Tech,2024,146:104379.
[25]LI J,WU J,XU N F,et al.Dynamic evolution and correlation between microorganisms and metabolites during manufacturing process and storage of Pu-erh tea[J].LWT-Food Sci Technol,2022,158:113128.
[26]CHEN G H,YANG C Y,LEE S J,et al.Catechin content and the degree of its galloylation in oolong tea are inversely correlated with cultivation altitude[J].J Food Drug Anal,2014,22(3):303-309.
[27]SEOUNGWOO S,JEESUN L,HYUN Y S,et al.Anti-glycation activities of methyl gallate in vitro and in human explants[J].J Cosmet Dermatol,2021,21(6):2602-2609.
[28]陈思铭,谢佳丽,阎续,等.基于拉曼光谱的没食子酸甲酯化反应在线监控方法[J].高校化学工程学报,2023,37(3):492-497.
[29]谢果,何蓉蓉,栗原博.茶叶生物碱的生物合成与代谢的研究进展[J].中国天然药物,2010,8(2):153-160.
[30]LI T H,WEI Y M,FENG W Z,et al.Exploring the mysterious effect of piling fermentation on Pu-erh tea quality formation: Microbial action and moist-heat action[J].LWT-Food Sci Technol,2023,185:115132.
[31]龙飘飘.LC-MS非靶标和靶标代谢组学分析普洱茶渥堆过程中关键标记物[D].合肥:安徽农业大学,2019.
[32]YANG C,HU Z Y,LU M L,et al.Application of metabolomics profiling in the analysis of metabolites and taste quality in different subtypes of white tea[J].Food Res Int,2018,106:909-919.
[33]ELSA B,SUSANA S,NUNO M,et al.In vivo interactions between procyanidins and human saliva proteins: Effect of repeated exposures to procyanidins solution[J].J Agr Food Chem,2014,62(39):9562-9568.
[34]CHEN Q C,SHI J,MU B,et al.Metabolomics combined with proteomics provides a novel interpretation of the changes in nonvolatile compounds during white tea processing[J].Food Chem,2020,332:127412.
[35]YE Y L,YAN J N,CUI J L,et al.Dynamic changes in amino acids,catechins,caffeine and gallic acid in green tea during withering[J].J Food Compos Anal,2018,66:98-108.
[36]ZHANG L,CAO Q Q,GRANATO D,et al.Association between chemistry and taste of tea:A review[J].Trends Food Sci Tech,2020,101:139-149.