蛋白酶是一类促进肽键断裂的酶,广泛用于食品、饲料、洗涤剂、皮革、生物修复和生物学基础研究等领域[1-3]。芽孢杆菌属(Bacillus)菌株发酵产蛋白酶是商业蛋白酶的重要来源,其分泌的碱性和中性蛋白酶不仅是改善饲料口感和质量的重要添加剂[4-6],更是生产功能性活性肽的关键酶。活性肽是一类由2~20个氨基酸组成的生物活性物质,具有抗氧化、抗癌、抑菌、降血压、免疫调节等多种生理功能[7-9],其制备方法主要包括酶解法、微生物发酵法和人工合成法[10],其中微生物发酵法具有成本低、安全性高、质量稳定、功能显著等优点[11]。然而,传统发酵工艺面临蛋白酶产量低、生产成本高、活性肽得率受限等瓶颈,制约了该技术的工业化应用。
周期性超声刺激是近年来出现的一种通过超声波技术辅助微生物发酵的方法,利用频率高于20 kHz的能量机械波,刺激发酵微生物,增强细胞通透性,加快细胞壁及细胞膜边界层的传质速率,改变细胞的生理代谢等[12-14]。王禹程[15]探究了超声处理解淀粉芽孢杆菌(Bacillus amyloliquefaciens)对豆粕固态发酵的影响,在最佳超声条件下,发酵豆粕中多肽含量较对照组提高15.57%,同时总蛋白酶活显著提升。LI Y等[16]采用超声辅助芽孢杆菌发酵酪蛋白,研究发现在最佳超声条件下,解淀粉芽孢杆菌发酵酪蛋白的蛋白酶活性和肽含量分别比对照提高了50%和45%。XIE M等[17]采用超声辅助枯草芽孢杆菌(B.subtilis)SNBS-3和解淀粉芽孢杆菌(B.amyloliquefaciens)10混合发酵豆渣制备抗氧化肽,结果表明,在最佳超声处理条件下,肽含量达到最大值(12.36±0.02)mg/mL。然而,由于超声波的快速衰减,周期性超声在固态发酵领域的研究应用较少。
本研究以豆粕为发酵底物,以耐盐芽孢杆菌(Bacillus halotolerans)为发酵菌种,对比不同发酵方式和周期性超声处理对耐盐芽孢杆菌固态发酵产物种蛋白酶活及活菌数的影响,并优化超声处理条件,同时利用转录组测序技术揭示周期性超声处理提高耐盐芽孢杆菌蛋白酶产量在分子层面的作用机理,并将周期性超声处理应用于耐盐芽孢杆菌固态发酵制备活性肽,以期提高豆粕等农副产物的高值化利用效率,为超声技术在蛋白酶及功能性肽工业化生产中的推广提供了技术支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株耐盐芽孢杆菌(Bacillus halotolerans):本实验室分离纯化、保藏。
1.1.2 试剂
福林试剂、碳酸钠、氢氧化钠、氯化钠、硫酸铜、琼脂粉、葡萄糖、三氯乙酸(trichloroacetic acid,TCA)、酒石酸钾钠、磷酸氢钠、磷酸二氢钠(均为分析纯):北京化工厂有限责任公司;胰蛋白胨、酵母提取物、酪蛋白(均为生化试剂):英国Oxoid有限公司;豆粕:内蒙古呼和浩特农贸市场。
1.1.3 培养基
LB固体培养基:胰蛋白胨10 g/L,酵母提取物5 g/L,NaCl 10 g/L,琼脂粉18 g/L,调节pH值至7.0~7.2,121 ℃灭菌20 min。LB液体培养基:配方同LB固体培养基,不添加琼脂粉,121 ℃灭菌20 min。
固体发酵培养基:豆粕粉20 g/瓶,以固液比1∶3(g∶mL),加入液体培养基(葡萄糖2 g/L,KH2PO4 1 g/L,pH值自然)。115 ℃灭菌30 min。
1.2 仪器与设备
SX-700高压蒸汽灭菌锅:日本Tomy Digital Biology公司;DL-CJ-1ND-Ⅱ超净工作台:北京东联哈尔仪器制造有限公司;HPX-Ⅱ-300生化培养箱:上海跃进医疗器械有限公司;ZHWY-2112B恒温培养摇床:常州金坛精达仪器制造有限公司;KQ-500E超声波清洗器:昆山市超声仪器有限公司;UV-1780紫外可见分光光度计:日本岛津公司;Heraeus Multifuge X3R离心机、NanoDrop2000超微量分光光度计:美国Thermo Scientific公司;llumina Nova Seq6000测序平台:北京奥维森基因科技有限公司;OmicShare云工具平台:广州基迪奥生物科技有限公司;Agilent 2100生物分析仪:美国安捷伦科技有限公司。
1.3 实验方法
1.3.1 菌株活化取4 ℃保存的耐盐芽孢杆菌(B.halotolerans)平板划线接种于LB固体培养基,37 ℃培养18 h。
1.3.2 种子液的制备
挑取活化的耐盐芽孢杆菌(B.halotolerans)单菌落接种至装液量为100 mL/250 mL LB液体培养基中,37 ℃、180 r/min恒温摇床培养18 h,即得种子液。
1.3.3 周期性超声处理对耐盐芽孢杆菌固态发酵的影响
以静置发酵组为对照,采用相同接种方式:将耐盐芽孢杆菌种子液按8%接种量均匀接种于固体培养基表面,37 ℃恒温培养,培养时间参考王禹程[15]方法稍作修改。
静置发酵组:接种后于37 ℃条件下恒温静置培养72 h。
周期性超声处理发酵组:培养72 h期间施加超声辅助发酵。在超声功率500 W,室温条件下,以发酵产物中蛋白酶活和活菌数作为评价指标,通过单因素试验分析不同周期性超声处理时间间隔(12 h、16 h、24 h)、不同周期性超声处理时间(30 min、60 min、90 min、120 min)对耐盐芽孢杆菌固态发酵的影响。
1.3.4 发酵产物分析检测
(1)耐盐芽孢杆菌活菌数:采用平板计数法测定。取发酵基质5 g,加50 mL无菌水,振荡混匀,取0.1 mL稀释液均匀涂布于LB固体培养基,37 ℃静置培养18 h后,统计LB平板上的耐盐芽孢杆菌(B.halotolerans)菌落数,根据稀释倍数和取样量计算耐盐芽孢杆菌活菌数。
(2)蛋白酶活力:采用GB/T 23527—2009《蛋白酶制剂》中的福林酚法测定。取发酵基质5 g,加50 mL磷酸氢钠(Na2HPO4)-磷酸二氢钠(NaH2PO4)缓冲溶液(pH 7.5),振荡混匀,于8 000 r/min条件下离心10 min,收集上清液检测蛋白酶活力。蛋白酶活力定义:1 g固体酶粉(或1 mL液体酶)在40 ℃、pH 7.5条件下,1 min产生1 μg酪氨酸定义为1个酶活单位(U/g)。
(3)多肽含量:采用双缩脲法测定。取上述上清液,加10%TCA溶液去除蛋白后,检测多肽含量,结果以干质量计。
(4)氨基酸含量:采用高效液相色谱法测定。分别称取周期性超声耐盐芽孢杆菌固态发酵第1~5天的样品各50 mg于离心管中,加入4 mL磷酸缓冲液充分溶解,取0.5 mL上述样品液于离心管中,在氮吹仪上60 ℃浓缩至近干,加入200 μL超纯水氮吹浓缩至近干,反复进行2次。用2.5 mL 0.02 mol/L盐酸溶液超声溶解,经0.22 μm滤膜过滤,进样测定氨基酸含量。
1.3.5 转录组测序
菌体收集:发酵结束后,向培养基中加无菌水,在无菌条件下用纱布过滤并收集滤液,于10 000 r/min条件下离心10 min,弃上清,沉淀于液氮速冻15 min。周期性超声处理固态发酵样品为处理组,静置固态发酵样品为对照组,每组设置3个重复。
核糖核酸(ribonucleic acid,RNA)提取、建库和测序:采用TRIzol法提取B.halotolerans的总RNA,并用RNase-free DNase I处理。通过1%琼脂糖凝胶电泳检测RNA的降解程度和污染情况,随后使用Agilent 2100生物分析仪进行定量,并利用NanoDrop分光光度计评估其纯度和完整性。使用NEBNext UltraTM RNA文库制备试剂盒(NEB,USA)构建cDNA文库,文库经质控合格后在Illumina Novaseq 6000平台上完成PE150双端测序。
差异表达基因(differentially expressed genes,DEGs)分析:对原始测序数据(raw reads)进行质控过滤,使用Perl脚本去除带有测序接头的、N(不确定碱基)含量比例>1%的以及低质量碱基(Q≤20)含量>50%的reads,获得高质量clean reads。使用Bowtie2(v2.2.6)软件将clean reads与Bacillus halodurans C-125参考基因组序列进行比对。利用HTSeq(v0.6.0)软件统计比对到每个基因的read counts,并采用FPKM(Fragments per kilobase of exon model per million mapped reads)法计算基因表达水平。基于表达量分析结果,使用DESeq(v1.22.1)软件对处理组和对照组进行差异表达分析,以Padj<0.05为标准,筛选差异表达基因(DEGs)。采用GOSeq(v1.22)、KOBAS(v2.0)软件对筛选到的DEGs进行基因本体(gene ontology,GO)、京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析。具体转录组学分析流程由北京奥维森基因科技有限公司和广州基迪奥生物科技有限公司完成[18]。
1.3.6 周期性超声处理应用于耐盐芽孢杆菌固态发酵制备活性肽
在超声功率500 W、超声处理间隔时间16 h、超声处理时间60 min条件下,对耐盐芽孢杆菌(B.halotolerans)豆粕固态发酵过程中的活菌数、蛋白酶活、多肽含量以及氨基酸含量进行监测。
2 结果与分析
2.1 周期性超声处理对耐盐芽孢杆菌固态发酵的影响
2.1.1 周期性超声处理对耐盐芽孢杆菌固态发酵蛋白酶活及活菌数的影响
由表1可知,在超声功率500 W,间隔时间12 h,每次30 min的条件下,经周期性超声处理发酵组的耐盐芽孢杆菌(B.halotolerans)固态发酵产物中蛋白酶活为(3371.40±101.03)U/g,较静置发酵组的蛋白酶活[(935.64±108.86)U/g]提高了约260.37%。周期性超声处理发酵组的活菌数为(95.3±2.62)×107 CFU/g,较静置发酵组活菌数[(80±1.34)×107 CFU/g]提高了约19.13%。结果表明,在耐盐芽孢杆菌(B.halotolerans)固态发酵过程中施加周期性超声处理,可显著提高蛋白酶产量,该结果与LI Y等[11]的研究一致。
表1 周期性超声处理对耐盐芽孢杆菌固态发酵中活菌数和蛋白酶活的影响
Table 1 Effects of periodic ultrasonic treatment on viable counts and protease activities during solid-state fermentation of Bacillus halotolerans

组别 蛋白酶活/(U·g-1)活菌数/(×107 CFU·g-1)静置发酵组周期性超声处理发酵组935.64±108.86 3 371.40±101.03 80.00±1.34 95.30±2.62
2.1.2 周期性超声处理间隔时间对耐盐芽孢杆菌固态发酵中蛋白酶活及活菌数的影响
在超声功率500 W,超声处理时间30 min条件下,探究周期性超声处理间隔时间对耐盐芽孢杆菌(B.halotolerans)固态发酵产物中活菌数和蛋白酶活的影响,结果见图1。
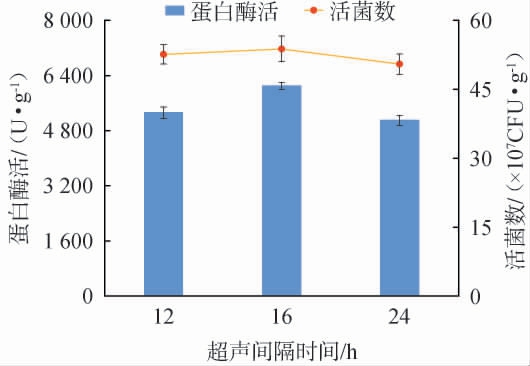
图1 不同周期性超声处理间隔时间对耐盐芽孢杆菌固态发酵中活菌数和蛋白酶活的影响
Fig.1 Effects of different time interval of periodic ultrasonic treatment on viable counts and protease activities during solid-state fermentation of Bacillus halotolerans
由图1可知,当周期性超声处理间隔时间为12 h时,蛋白酶活和活菌数分别为(5 325.39±159.85)U/g和(52.6±2.1)×107CFU/g,细胞来不及修复上一次空化作用造成的损伤,再次遭受刺激导致不可逆的损伤,甚至菌体死亡;当周期性超声处理间隔时间为16 h时,蛋白酶活和活菌数均达到最大值,分别为(6 102.29±104.66)U/g、(53.8±2.8)×107 CFU/g。当周期性超声处理间隔时间为24 h时,蛋白酶活和活菌数分别为(5 102.19±144.14)U/g、(50.5±2.2)×107 CFU/g,对菌体细胞壁和细胞膜的损伤效果小,加之自身的修复功能,导致细胞膜通透性变化不大[19]。因此,选择最佳超声处理间隔时间为16 h。
2.1.3 周期性超声处理时间对耐盐芽孢杆菌固态发酵中蛋白酶活及活菌数的影响
在超声功率500 W,超声处理间隔16 h的条件下,探究周期性超声处理时间对耐盐芽孢杆菌(B.halotolerans)固态发酵中蛋白酶活和活菌数的影响,结果见图2。由图2可知,随着周期性超声处理时间在30~120 min范围内的增加,蛋白酶活和活菌数均呈先增加后降低的趋势。当周期性超声处理时间为30~60 min时,蛋白酶活和活菌数随之增加;当周期性超声处理时间为60 min时,蛋白酶活和活菌数均达到最高,分别为(5151.78±137.69)U/g、(55.5±0.21)×107 CFU/g;当周期性超声处理时间>60 min之后,蛋白酶活与活菌数均有所下降。处理时间过长,过度的振动和空化效应会破坏细胞结构,造成永久性损伤[20]。PAWAR S V等[21]利用超声强化地衣芽孢杆菌产尿酸酶和碱性蛋白酶,发现当超声处理时间为15 min时,尿酸酶和碱性蛋白酶的产量最高,超声处理时间超过15 min时,由于细菌细胞的有害变化导致尿酸酶和碱性蛋白酶产量降低,与本实验结果基本一致。因此,选择最佳每次超声处理时间为60 min。
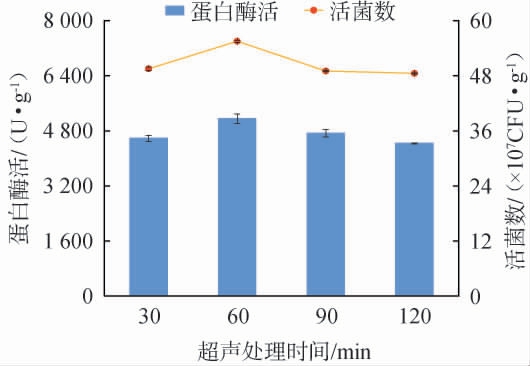
图2 不同周期性超声处理时间对耐盐芽孢杆菌固态发酵中活菌数和蛋白酶活的影响
Fig.2 Effects of different periodic ultrasonic treatment time on viable counts and protease activities in solid-state fermentation of Bacillus halotolerans
2.2 周期性超声对B.halotolerans转录组学的影响
2.2.1 差异表达基因筛选
以校正后的P值(Padj)<0.05为标准,筛选处理组和对照组之间的差异表达基因(DEGs),两组之间的差异表达基因(DEGs)火山图见图3。由图3可知,共筛选到2 557个DEGs,其中1 277个基因上调,1 280个基因下调。结果表明,当B.halotolerans受到周期性超声刺激时,其菌体细胞内的基因表达发生了显著变化。
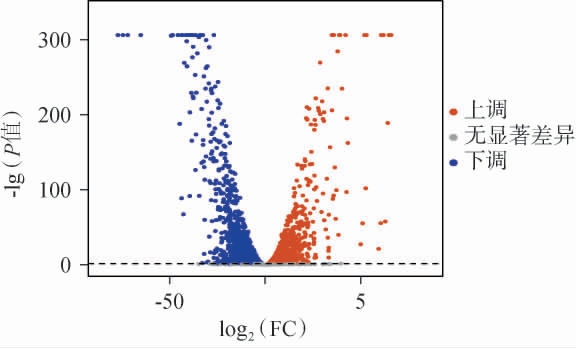
图3 处理组与对照组之间差异表达基因火山图
Fig.3 Volcano plot of differentially expressed genes between the treatment group and the control group
2.2.2 差异表达基因的GO注释和功能富集分析
对筛选到的2 557个差异表达基因(DEGs)进行GO数据库注释,并将其按功能归类为生物学过程(biological process,BP)、细胞组分(cellular component,CC)和分子功能(molecular function,MF)三大类。按Q值从小到大排序,选取前20个显著富集的GO条目进行展示,其中生物学过程类占11条,分子功能类占9条,细胞组分类无条目富集。对两组之间的差异表达基因进行显著性富集分析,结果见图4。
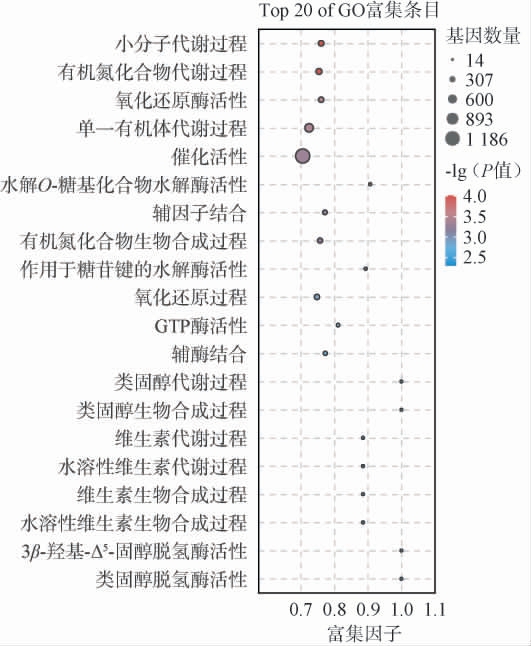
图4 处理组与对照组之间差异表达基因的基因本体富集分析
Fig.4 Gene ontology enrichment analysis of differentially expressed genes between the treatment group and control group
由图4可知,在生物学过程类别中,差异表达基因主要参与小分子代谢过程、有机氮化合物代谢过程、单一有机体代谢过程、有机氮化合物生物合成过程以及氧化还原过程。其中,单一有机体代谢过程富集的差异基因数量最多,共593个(上调299个,下调294个)。在分子功能类别中,差异表达基因主要富集于氧化还原酶活性、催化活性、水解酶活性及水解O-糖基化合物等功能。催化活性类别富集的差异基因数量最多,达1 186个(上调602个,下调584个)。结果表明,周期性超声处理通过调控B.halotolerans的多个代谢过程,对其菌体生长、代谢能力以及环境胁迫响应产生重要影响。
2.2.3 差异表达基因的KEGG通路富集分析
为进一步系统分析差异表达基因(DEGs)参与的代谢通路,将筛选出2 557个差异表达基因映射到KEGG数据库进行功能注释,并选取显著性最高的前20条通路见图5。由图5可知,差异表达基因(DEGs)显著富集于次级代谢产物生物合成、代谢通路、糖酵解/糖异生、淀粉和蔗糖代谢、三羧酸循环、碳代谢、甘氨酸/丝氨酸/苏氨酸代谢、半胱氨酸与甲硫氨酸代谢以及氨酰tRNA生物合成等通路,其中,代谢通路富集程度最高,其次为次级代谢产物生物合成通路。这些富集通路覆盖了糖类代谢(如糖酵解、淀粉蔗糖代谢、三羧酸循环)、氨基酸代谢(如甘氨酸/丝氨酸/苏氨酸代谢、半胱氨酸与甲硫氨酸代谢)及蛋白质合成(如氨酰tRNA生物合成)等过程,表明周期性超声处理通过调控B.halodurans的碳源利用、氨基酸供应及蛋白质合成网络,为其产生蛋白酶提供了充足的物质和能量基础。
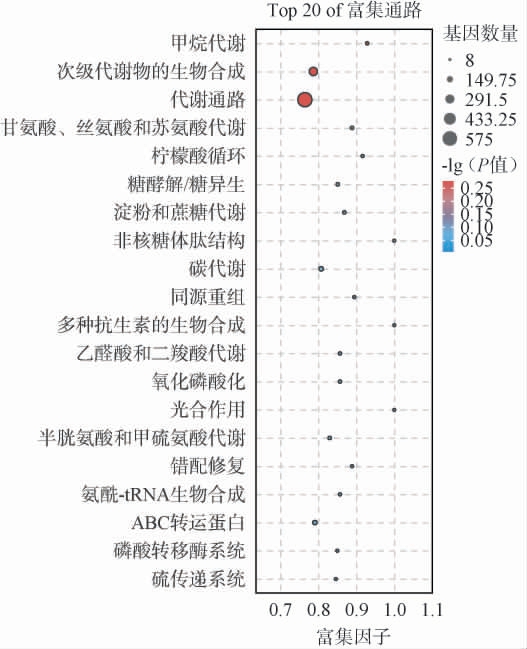
图5 处理组与对照组之间差异表达基因的京都基因与基因组百科全书代谢通路富集分析
Fig.5 Kyoto Encyclopedia of Genes and Genomes metabolic pathway enrichment analysis of differentially expressed genes between the treatment group and control group
尽管实验部分证明了周期性超声处理后可明显提高B.halotolerans固态发酵产物中蛋白酶产量,但是转录组数据显示编码胞外蛋白酶的基因aprE表达量显著下调(log2FC=-1.36),基因mprF表达量虽略有上调,但未达到显著水平(log2FC=-0.35),结果提示,周期性超声可能并非直接提高单个细胞的蛋白酶合成能力,而是通过其他途径实现的。研究表明,芽孢杆菌属(Bacillus)合成胞外蛋白酶与孢子形成起始阶段存在时间上的协同关系[22]。ZHOU C等[23]通过构建参与地衣芽孢杆菌孢子形成的主调控基因(spo0A、sigF和sigE)的缺失突变体,发现与孢子形成II期相关的突变能显著提升碱性蛋白酶产量。
现有研究揭示了超声处理对芽孢杆菌孢子存续的复杂影响。在嗜热地衣芽孢杆菌YYC4中,在超声时间0~1.5 h内,孢子数量从5.57×106 CFU/mL减少至4.37×106 CFU/mL,当超声处理时间进一步延长至3 h时,孢子数量又回升至7.27×106 CFU/mL,该现象被归因于低强度超声促进了孢子萌发,本实验的超声处理时间60 min正处于“促进萌发、减少孢子”的时间范围内[24]。与此同时,本研究的转录组数据揭示了超声处理的一个更为直接且持续的作用机制:周期性超声处理后耐盐芽孢杆菌的芽孢形成通路中多个关键基因表达发生显著变化:孢子启动相关基因spo0M(log2FC=-1.85)显著下调,该基因参与Spo0A调控网络,影响磷酸中继系统及芽孢启动信号的传递;前孢子特异性σ因子sigF(log2FC=-1.94)表达受到抑制,阻碍前孢子早期发育程序的启动;孢子形成Ⅱ期关键元件spoIIQ(log2FC=-2.45)、spoIIAA(log2FC=-2.33)、spoIIAB(log2FC=-1.77)均显著下调,这些基因负责前孢子与母细胞间的信号转导和σF因子的激活,其表达下降严重破坏了细胞不对称分裂后的区室化协调与孢子成熟进程。结果表明,周期性超声处理通过显著抑制B.halotolerans孢子形成通路中多个核心基因的表达,有效的阻断了菌体向休眠态转化,使其无法进入孢子形成程序,从而维持较高的代谢活性和营养生长状态。这一调控效应促使菌体持续进行蛋白酶合成与分泌,最终在发酵体系中整体提高了蛋白酶和多肽的产量。
2.3 周期性超声处理应用于耐盐芽孢杆菌豆粕固态发酵制备活性肽
在超声功率500 W、超声处理时间间隔16 h、超声处理时间60 min条件下,对耐盐芽孢杆菌(B.halotolerans)豆粕固态发酵过程中的活菌数、蛋白酶活、多肽含量以及氨基酸含量进行动态监测,结果见图6。由图6可知,B.halotolerans在该培养条件下,0~3 d为对数生长期,在第3天达到峰值,为(11.9±0.14)×108 CFU/g,3 d后进入稳定期,随后逐渐进入衰亡期,活菌数逐步下降。蛋白酶活在培养前3 d内随菌体生长迅速提高,于第3天达到峰值,为(5147.52±31.68)U/g;3 d后随着菌体进入衰亡期,耐盐芽孢杆菌活菌数减少,蛋白酶合成能力下降,酶活随之降低。多肽含量整体呈先上升后下降趋势,发酵前4 d内,蛋白酶持续水解豆粕蛋白生成多肽,多肽含量逐渐累积,第4天达到最大值,为(146.42±0.8)mg/g。氨基酸含量在发酵0~5 d内持续增加,第5天达到最高值,为(250.46±15.37)mg/g。这主要是由于蛋白酶持续水解蛋白质生成多肽,多肽进一步被肽酶水解为氨基酸,而且氨基酸作为菌体生长的直接氮源,在发酵后期平稳期仍可能被少量合成或从多肽中释放。值得注意的是,蛋白酶活在第3天达到峰值时,多肽含量并未同步达到最高,其峰值滞后于蛋白酶活峰值。该结果与WANG Y等[25]超声处理淀粉样芽孢杆菌提高豆粕固态发酵产物肽含量的报道基本一致。可能是因为蛋白酶活性最高时,蛋白质水解反应仍在持续进行并不断生成多肽;与此同时超声空化效应刺激菌体快速生长,基质中的营养物质被加速消耗。为满足生长所需的碳源和氮源,菌体可能转而利用已生成的多肽,从而推迟了多肽的净积累峰值。因此在超声功率500 W、超声处理间隔时间16 h、超声处理时间60 min条件下,耐盐芽孢杆菌(B.halotolerans)豆粕固态发酵制备活性肽,为实现多肽产量的最大化,应选择最适发酵时间为4 d。
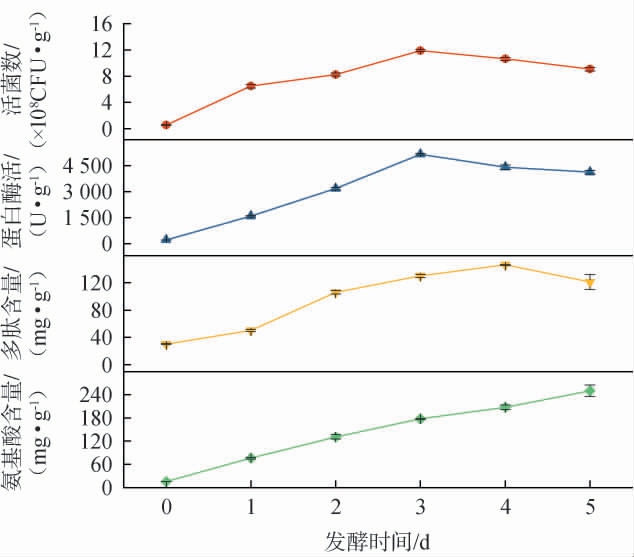
图6 耐盐芽孢杆菌固态发酵过程中活菌数、蛋白酶活、多肽和氨基酸含量的变化
Fig.6 Changes of viable counts, protease activities, polypeptide and amino acid contents during solid-state fermentation process of Bacillus halotolerans
3 结论
本研究以耐盐芽孢杆菌(B.halotolerans)为发酵菌种,考察发酵方式和周期性超声处理对固态发酵产物中蛋白酶活及活菌数的影响,利用转录组测序技术进一步阐明周期性超声强化耐盐芽孢杆菌固态发酵产蛋白酶的作用机理,并将优化的周期性超声条件应用于耐盐芽孢杆菌固态发酵制备活性肽。结果表明,最佳超声处理条件为超声功率500 W,超声处理时间间隔16 h,超声处理时间60 min。在此优化条件下,蛋白酶酶活为(5 151.78±137.69)U/g,较对照组(未超声处理)提高了约450.61%。以Padj<0.05为筛选条件,周期性超声组和对照组样品之间共筛选到2 577个差异表达基因,其中1 277个基因上调,1 280个基因下调。GO富集分析结果显示,差异基因在生物学过程类别中主要参与小分子代谢过程、有机氮化合物代谢过程、单一有机体代谢过程、有机氮化合物生物合成过程以及氧化还原过程。在分子功能的类别中主要富集于氧化还原酶活性、催化活性和水解酶活性。在KEGG富集分析中,差异表达基因(DEGs)显著富集在糖类代谢、氨基酸代谢和蛋白质合成等代谢通路。周期性超声下调了B.halotolerans中与芽孢形成相关基因spo0M、sigF、spoIIQ、spoIIAA、spoIIAB的表达,有效阻止了菌体形成休眠体,使其维持活性状态,进而能够持续产生蛋白酶。同时,优化周期性超声处理能够应用于B.halotolerans豆粕固态发酵制备活性肽。
[1]LIMKAR M B,PAWAR S V,RATHOD V K.Statistical optimization of xylanase and alkaline protease co-production by Bacillus spp using Box-Behnken design under submerged fermentation using wheat bran as a substrate[J].Biocatal Agr Biotechnol,2019,17:455-464.
[2]ZHANG Y, HU J, ZHANG Q, et al.Enhancement of alkaline protease production in recombinant Bacillus licheniformis by response surface methodology[J].Bioresour Bioproc,2023,10(1):27.
[3]SONG P,ZHANG X, WANG S, et al.Microbial proteases and their applications[J].Front Microbiol,2023,14:1236368.
[4]CHEN H,WU J,HUANG X,et al.Overexpression of Bacillus circulans alkaline protease in Bacillus subtilis and its potential application for recovery of protein from soybean dregs[J].Front Microbiol,2022,13:968439.
[5]CONTESINI F J,MELO R R,SATO H H.An overview of Bacillus proteases:from production to application[J].Crit Rev Biotechnol,2018,38(3):321-334.
[6]MATKAWALA F,NIGHOJKAR S,KUMAR A,et al.Microbial alkaline serine proteases:Production,properties and applications[J].World J Microbiol Biotechnol,2021,37(4):63.
[7]余楠楠,陈琛.生物活性肽功能及制备技术研究进展[J].中国酿造,2018,37(9):17-21.
[8]杨文清,黄秀芳,陈耀兵,等.植物源生物活性肽的研究进展[J].食品安全质量检测学报,2023,14(1):270-278.
[9]WEN Q M,ZHANG L,ZHAO F,et al.Production technology and functionality of bioactive peptides[J].Curr Pharm Des,2023,29(9):652-674.
[10]ZHU F,CAO J,SONG Y,et al.Plant protein-derived active peptides:a comprehensive review[J].J Agr Food Chem,2023,71(51):20479-20499.
[11]朱梦媛,李冲伟.植物源功能肽的制备、生理活性与应用研究进展[J].食品科学,2021,42(17):363-369.
[12]孙悦,夏蓉,陶汇源,等.超声波促进巴氏醋杆菌发酵生长的研究[J].中国酿造,2018,37(8):45-49.
[13]LIU Y, ZHU J X, ZHU C H.Effect of ultrasonic pretreatment on fermentation performance and quality of fermented hawthorn pulp by lactic acid bacteria[J].Food Chem,2024,446:138774.
[14]HAO J,XU H N,YAN P F,et al.Application of fixed-frequency ultrasound in the cultivation of Saccharomyces cerevisiae for rice wine fermentation[J].J Sci Food Agric,2024,104(11):6417-6430.
[15]王禹程.超声处理解淀粉芽孢杆菌对豆粕固态发酵产肽的影响及其作用机制[D].镇江:江苏大学,2021.
[16]LI Y,RUAN S,ZHOU A,et al.Ultrasonic modification on fermentation characteristics of Bacillus varieties:Impact on protease activity,peptide content and its correlation coefficient[J].LWT-Food Sci Technol,2022,154:112852.
[17]XIE M X,MA Y Y,AN F Y,et al.Ultrasound-assisted fermentation for antioxidant peptides preparation from okara: Optimization, stability,and functional analyses[J].Food Chem,2024,439:138078.
[18]MU H Y,CHEN J Z,HUANG W J,et al.OmicShare tools:A zero-code interactive online platform for biological data analysis and visualization[J].iMeta,2024,3(5):e228.
[19]户红通,徐达,徐庆阳,等.超声辅助细胞转型的谷氨酸发酵工艺[J].食品与发酵工业,2019,45(1):44-48.
[20]HU Y,LI K,BAI Y,et al.Effect of combined ultrasonic and enzymatic assisted treatment on the fermentation process of whole Lycium barbarum(goji berry)fruit[J].Food Biosci,2023,53:102550.
[21]PAWAR S V, RATHOD V K.Ultrasound assisted process intensification of uricase and alkaline protease enzyme co-production in Bacillus licheniformis[J].Ultrason Sonochem,2018,45:173-179.
[22]ZHOU C,ZHOU H,FANG H,et al.Spo0A can efficiently enhance the expression of the alkaline protease gene aprE in Bacillus licheniformis by specifically binding to its regulatory region[J].Int J Biol Macromol,2020,159:444-454.
[23]ZHOU C,ZHOU H,ZHANG H,et al.Optimization of alkaline protease production by rational deletion of sporulation related genes in Bacillus licheniformis[J].Microb Cell Fact,2019,18(1):127.
[24]DAI C H,SHU Z Z,XU X T,et al.Enhancing the growth of thermophilic Bacillus licheniformis YYC4 by low-intensity fixed-frequency continuous ultrasound[J].Ultrason Sonochem,2023,100:106611.
[25]WANG Y,XU K,LU F,et al.Increasing peptide yield of soybean meal solid-state fermentation of ultrasound-treated Bacillus amyloliquefaciens[J].Innov Food Sci Emerg,2021,72:102704.