库德毕赤酵母(Pichia kudriavzevii)是一种耐高温、耐酸的酵母菌,广泛应用于白酒、酱油等传统发酵食品的生产。然而,在发酵过程中,微生物常面临高温、高酸等胁迫环境,导致生长抑制和代谢效率下降[1]。因此,提高酵母的环境适应性对优化发酵工艺至关重要。通过工艺改进,不仅能够提高酵母菌株在高温环境下的存活率和代谢活性,更能确保发酵过程的稳定性和连续性,这对白酒工业化生产的质量控制与工艺优化具有重要的实践意义。
交叉保护是一种通过亚致死胁迫预处理增强微生物抗逆性的策略,在微生物抗逆性调控中具有重要应用价值[2]。如盐胁迫可提高库德毕赤酵母(P.kudriavzevii)的耐热性,并促进热休克蛋白HSP12和麦角固醇合成酶的表达[3]。乳酸胁迫能够优化碳源利用和代谢产物组成,促进P.kudriavzevii菌株固态发酵[4]。近年来,关于热应激预处理对微生物耐受性影响的研究逐渐增多。热应激预处理可以诱导微生物产生一系列生理和生化反应,如热休克蛋白的合成、膜脂肪酸组成的改变、抗氧化酶活性的提高等,从而增强微生物对高温和其他胁迫的耐受性[5-6]。陈家露等[7]研究发现,在热应激条件下,大肠杆菌(Escherichia coli)的ycjX基因表达水平显著上升,其表达可能受到σ32因子的调控。σ32因子能够与核糖核酸(ribonucleic acid,RNA)聚合酶相互作用,进而激活热休克基因的转录过程,促使热休克蛋白得以合成,从而赋予细菌抵御热应激的能力。庄若茹等[8]研究发现,热应激预处理可诱导乳酸菌产生相应的应激蛋白来修复或降解受损蛋白,从而提高乳酸菌在喷雾干燥过程中的存活率。相较之下,国外学者对于热休克蛋白等分子伴侣在热应激中所发挥的作用进行了更为深入的研究,研究证明热休克蛋白70、DnaK和FstH等分子伴侣可结合并降解未折叠蛋白,维持细胞内蛋白质的稳定[9-10]。然而,目前关于热应激预处理对酵母菌发酵性能的影响研究尚不充分,其交叉保护效应的调控机制仍不明确。
为了探究不同温度的预处理对库德毕赤酵母(P.kudriavzevii)PK8交叉保护效应的影响,本研究通过检测菌株存活率、胞内pH、活性氧簇(reactive oxygen species,ROS)、三磷酸腺苷(adenosine triphosphate,ATP)含量、挥发性代谢产物及细胞膜脂肪酸组成解析细胞生理特性和代谢产物的变化。旨在为工业发酵中酵母菌的抗逆性优化提供新策略,为揭示交叉保护提升酵母菌发酵性能的生理机制提供理论参考,同时为高温发酵工艺改进提供理论支持,有助于提高发酵效率和产品质量。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
库德毕赤酵母(P.kudriavzevii)PK8:分离自浓香型白酒糟醅,保存于黑龙江省科学院微生物研究所菌种保藏中心。
1.1.2 化学试剂
磷酸盐缓冲液:生工生物工程(上海)股份有限公司;甲醇钠、正己烷、4-(2-羟乙基)-1-哌嗪乙磺酸[4-(2-hydroxyethyl)piperazine-1-ethanesulfonic acid,HEPES]:上海麦克林生化科技股份有限公司;胞内pH检测试剂盒、ROS检测试剂盒、ATP检测试剂盒:上海碧云天生物科技有限公司;二喹啉甲酸(bicinchoninic acid,BCA)蛋白浓度检测试剂盒:南京建成生物科技有限公司;其他试剂均为国产分析纯。
1.1.3 培养基
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YEPD)固体培养基、YEPD液体培养基:青岛海博生物技术有限公司。
1.2 仪器与设备
Trace GC Ultra-DSQⅡ型气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)仪:美 国Thermo Fisher公司;Lzp930色谱柱(50 m×0.25 mm×0.25 μm):北京豫维科技有限公司;ZQLY-300V恒温摇床:上海知楚仪器有限公司;3K15高速冷冻离心机:德国Sigma公司;Infinite 200 PRO酶标仪:帝肯(上海)贸易有限公司;BPH-9082恒温培养箱:上海一恒科学仪器有限公司。
1.3 方法
1.3.1 菌株活化
采用平板划线法将保藏的菌株PK8甘油菌液接种于YEPD固体培养基,28 ℃静置培养48 h。挑取单菌落重复划线接种获得纯化菌株PK8,复接种于YEPD液体培养基中,28 ℃、180 r/min振荡培养24 h至对数生长期,用于后续实验。
1.3.2 热应激预处理对菌株PK8生长的影响
将活化至对数生长期的菌株PK8,分别置于不同温度(28 ℃、37 ℃、40 ℃、42 ℃、44 ℃、45 ℃、46 ℃)、180 r/min条件下振荡培养90 min。培养结束后,各组在4 ℃、8 000 r/min条件下离心10 min收集菌体,用无菌的磷酸盐缓冲液洗涤两次,进行酵母菌落计数。酵母PK8存活率计算公式如下:
式中:A1为在不同温度(37 ℃、40 ℃、42 ℃、44 ℃、45 ℃、46 ℃)、180 r/min条件下振荡培养90 min后的酵母菌数,个;A0为在28 ℃、180 r/min条件下振荡培养90 min后的酵母菌数,个。
1.3.3 热应激预处理对菌株PK8高温发酵特性的影响
将活化至对数生长期的菌株PK8,分别置于不同温度(28 ℃、37 ℃、40 ℃、42 ℃、44 ℃)、180 r/min条件下振荡培养90 min进行热应激预处理。预处理结束后,各组在4 ℃、8 000 r/min条件下离心10 min收集菌体,用无菌的磷酸盐缓冲液洗涤以去除培养基成分。将菌体重悬于新的YEPD液体培养基中,调整各组菌悬液浓度至3.0×108 CFU/mL,在45 ℃、180 r/min条件下振荡培养24 h。
培养结束后离心,菌体用无菌的磷酸盐缓冲液(phosphate buffer solution,PBS)洗涤两次,稀释成适当梯度后涂布平板法计数。以经28 ℃热应激预处理的样品细胞存活数为基准,根据存活倍数评估不同热应激预处理对酵母菌株高温特性的影响[11]。存活倍数计算公式如下:
式中:B1为不同温度(37 ℃、40 ℃、42 ℃、44 ℃)热应激预处理后,再以45 ℃、180 r/min条件下振荡培养24 h后的酵母菌数,个;B0为以28 ℃热应激预处理后,再以45 ℃、180 r/min条件下振荡培养24 h后的酵母菌数,个。
利用气相色谱法对上清液中的挥发性代谢产物进行检测,参照潘婉舒等[4]的方法稍作修改。气相色谱条件:Lzp930色谱柱(50 m×0.25 mm×0.25 μm),进样温度230 ℃,检测温度250 ℃,进样量0.3 μL,载气为高纯氮气(N2),流速1.0 mL/min,分流比10∶1,升温程序为40 ℃保持3 min;以5 ℃/min升温至100 ℃,保持1 min;以10 ℃/min升温至200 ℃,保持2 min;再以15 ℃/min升温至230 ℃,保持10 min。
1.3.4 热应激预处理对菌株PK8胞内pH的影响
参考吴重德[12]的方法稍作修改:取2 mL对数生长期的菌株PK8,经不同热应激预处理90 min后,离心收集菌体。用50 mmol/L HEPES缓冲液洗涤2次后重悬于等体积的相同缓冲液,加入1 μL胞内pH荧光探针,30 ℃水浴20 min。用磷酸盐缓冲液洗涤3次后重悬于等体积的缓冲液中。按照BREEUWER P等[13]的方法分别测定菌悬液的荧光强度It和上清的荧光强度If。激发波长为490 nm和440 nm,发射波长为525 nm,狭缝宽度均为5 nm。总荧光强度I计算公式如下:
式 中:I为 总 荧 光 强 度;(I490)t、(I490)f、(I440)t、(I440)f分 别 表 示490 nm激发波长条件下菌悬液荧光强度、490 nm激发波长条件下上清液荧光强度、440 nm激发波长下菌悬液荧光强度、440 nm激发波长条件下上清液荧光强度。
配制不同pH的标准缓冲体系,分别加入等量荧光探针,同时测定各pH条件下的荧光强度I。以荧光强度I的对数值(lgI值)为横坐标(x),对应的pH值(y)为纵坐标绘制荧光强度标准曲线,得到标准曲线回归方程为:y=3.818 7x+6.466 1,相关系数R2=0.992 4。根据标准曲线回归方程计算胞内pH值。
1.3.5 热应激预处理对菌株PK8胞内ROS的影响
参考ZHANG H等[14]的方法,取不同热应激预处理后的酵母菌细胞悬浮液1.0 mL,离心收集菌体。经磷酸盐缓冲液洗涤3次后,用10 μmol/L的2',7'-二氯二氢荧光素二乙酸酯进行处理,处理完成后置于暗处于37 ℃培养30 min,使用酶标仪测定样品在激发波长(488 nm)/发射波长(525 nm)处的荧光强度,以此确定酵母菌细胞内的ROS水平。
1.3.6 热应激预处理对菌株PK8胞内ATP的影响
取不同热应激预处理后的酵母菌细胞悬浮液1.0 mL,离心收集菌体。将磷酸盐缓冲液洗涤3次后的酵母菌细胞置于裂解液中裂解,于4 ℃、12 000×g离心10 min,获得菌体沉淀。ATP浓度(nmol)参照ATP检测试剂盒说明书进行测定。为了消除样品制备时由于蛋白量的差异而造成的误差,样品的蛋白浓度(mg)按照蛋白浓度检测试剂盒进行测定。将ATP浓度换算成nmol/mg蛋白形式。
1.3.7 热应激预处理对菌株PK8膜脂肪酸的影响
取20 mL对数生长期的菌株PK8,经不同热应激预处理90 min后,离心收集菌体。经去离子水洗涤3次,弃上清后向沉淀中加入1.5 mL 1 mol/L甲醇钠振荡90 s,置于4 ℃静置10 min。加入1 mL正已烷,振荡1 min,静置5 min,取上层有机相测定膜脂肪酸含量。膜脂肪酸含量的测定按ZHENG J等[15]的方法进行。以不饱和脂肪酸与饱和脂肪酸的比值反映膜脂肪酸不饱和度[11]。平均碳链长度计算公式如下:
平均碳链长度=(∑FAP×C)/100
式中:FAP为每种脂肪酸占比,%;C为脂肪酸碳原子数,个。
1.3.8 数据处理与统计分析
所有数据均为3次重复试验的平均值,采用SPSS 18.0进行显著性差异检验(P<0.05),用Origin 2024作图。
2 结果与分析
2.1 热应激预处理对菌株PK8存活率的影响
为筛选合适的热应激预处理条件,考察了对数生长期的酵母菌PK8在不同温度(28 ℃、37 ℃、40 ℃、42 ℃、44 ℃、45 ℃、46 ℃)条件下处理90 min后的存活率变化,结果见图1。由图1可知,热应激预处理显著影响对数生长期酵母菌的存活率(P<0.05)。随着处理温度从37 ℃升高至46 ℃,酵母菌PK8存活率由75.21%急剧下降至7.06%。当处理温度>44 ℃之后,酵母菌的存活率降至20%以下。过低的存活率可能导致菌体数量不足,难以满足工业化发酵需求。基于此,后续实验选择37 ℃、40 ℃、42 ℃和44 ℃作为热应激预处理的优化温度范围,以平衡存活率与热应激效应,确保菌株在保持较高活性的同时增强其耐高温特性。
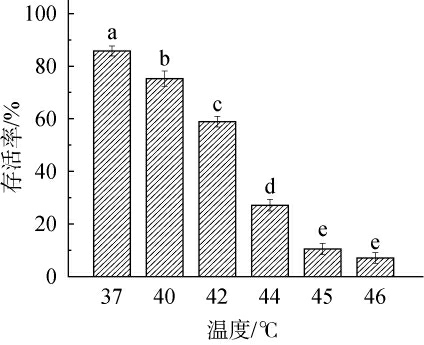
图1 热应激温度对菌株PK8存活率的影响
Fig.1 Effect of thermal stress temperature on the survival rates of strain PK8
不同字母表示差异显著(P<0.05)。下同。
2.2 热应激预处理对菌株PK8高温发酵特性的影响
白酒发酵工艺伴随着显著的产热效应,导致窖池内部温度呈现动态变化,对微生物群落构成严峻挑战,特别是对于参与发酵的关键微生物——酵母菌而言,其耐热性能直接影响发酵效率和产物品质[16]。因此提升菌株的高温耐受性对实际生产具有重要意义。实验以45 ℃模拟白酒发酵过程中糟醅温度,考察不同温度(37 ℃、40 ℃、42 ℃和44 ℃)预处理对酵母菌PK8高温胁迫下存活能力的影响,结果见图2。由图2可知,与28 ℃对照处理组(存活倍数设为1)相比,经过37 ℃、40 ℃、42 ℃和44 ℃预处理90 min的菌株,其高温胁迫下的存活倍数分别显著提升至1.34倍、1.72倍、2.00倍和1.53倍。这一系列数据证实了这种“预适应”效应在微生物体内进行了响应,在高温环境下表现出更强的应激能力和更稳定的防御系统,这些特性对于维持白酒发酵期间复杂的微生物生态平衡和保障发酵进程的顺利完成至关重要。
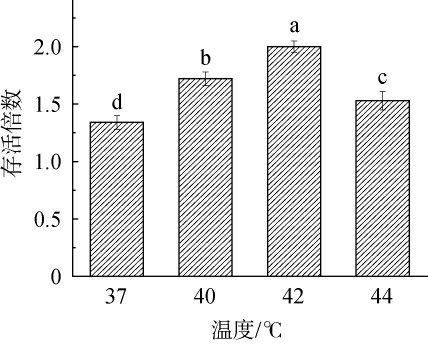
图2 热应激温度对菌株PK8高温胁迫下存活倍数的影响
Fig.2 Effect of thermal stress temperature on the survival fold of strain PK8 during high-temperature stress
值得注意的是,不同预处理温度对菌株的耐受性提升效果呈现先升后降的特征。其中42 ℃预处理表现出最优异的保护效果,这一温度条件可能是诱导酵母菌热休克蛋白等保护机制表达的最适温度点。CHAMNIPA N等[17]研究发现,P.kudriavzevii RZ8-1在42 ℃乙醇发酵过程中,热休克蛋白基因(ssq1、hsp90)、乙醇脱氢酶基因(adh1、adh2、adh3、adh4)以及甘油醛-3-磷酸脱氢酶基因(tdh2)的表达水平均有所提升,这为本实验结果提供了有力的解释。酵母在高温与适温条件下的代谢调节存在显著差异,温度过高(44 ℃)或过低(37 ℃)时,预处理效果均有所下降,这表明细胞能够通过调控耐高温相关代谢基因的表达来调整代谢产物,热应激预处理的保护效应具有温度依赖性。
2.3 热应激预处理对PK8菌株高温发酵主要挥发性代谢产物的影响
酵母菌高温发酵产生的主要挥发性代谢产物分析结果见表1。由表1可知,在42 ℃预处理条件下,乙醇和酯类(乙酸乙酯14.90 mg/L、己酸乙酯4.09 mg/L、辛酸乙酯5.16 mg/L和乙酸异戊酯6.54 mg/L等)含量均达到峰值。适度的热应激预处理,有助于增强细胞膜稳定性,从而提高糖酵解效率和酯酶活性,促进酯类合成[18]。而过高的预处理温度导致膜脂过氧化和关键酶失活,乙醇和酯类产量显著下降。在核盘菌的研究中,40 ℃高温处理能够显著诱导热休克蛋白HSP70的表达,且其表达量在高温处理的后期达到峰值[19]。据此推测,本实验中42 ℃通过诱导酵母菌的热休克蛋白的表达,修复变性蛋白和维持酶活性,显著提升细胞的耐受性,减少高温对细胞代谢的负面影响,从而提高发酵效率。
表1 不同热应激预处理下菌株PK8高温发酵主要挥发性代谢产物含量变化
Table 1 Changes of major volatile metabolites contents during high-temperature fermentation of strain PK8 under different thermal stress pretreatments
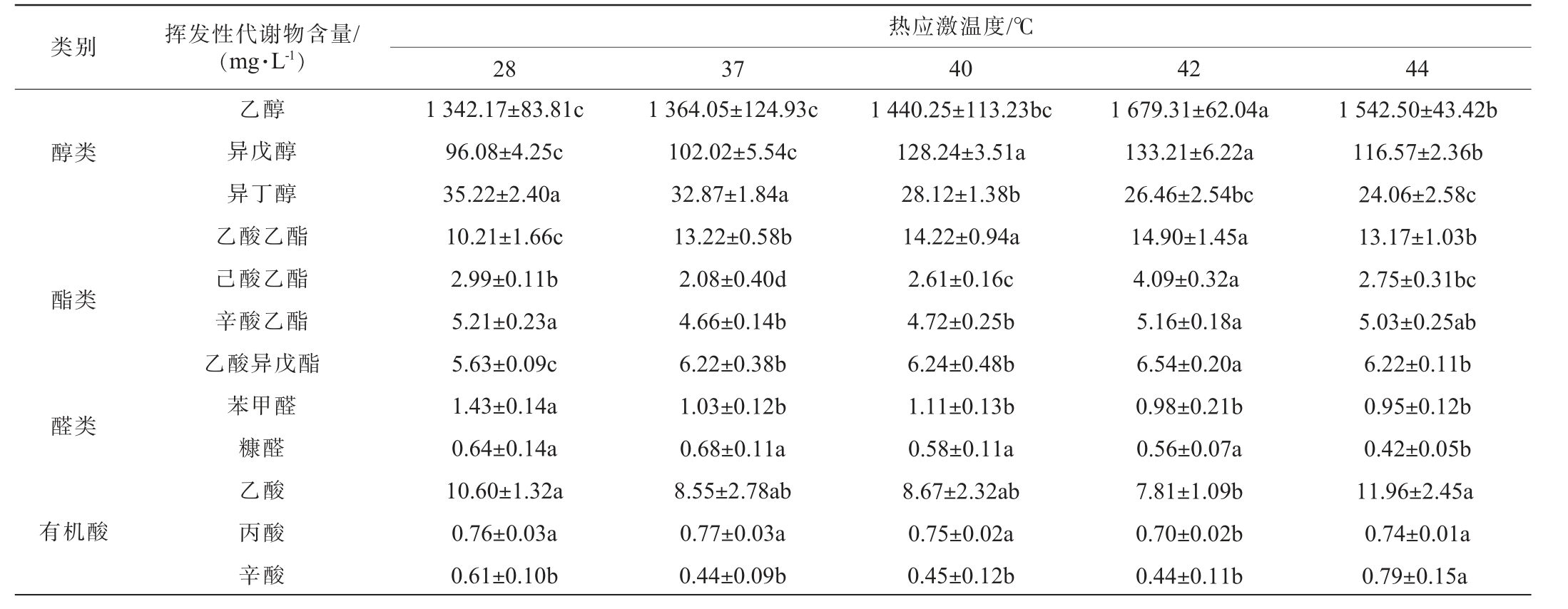
注:不同小写字母表示同一行数据存在差异显著(P<0.05)。
类别 挥发性代谢物含量/(mg·L-1)28 37热应激温度/℃40 42 44醇类酯类醛类有机酸乙醇异戊醇异丁醇乙酸乙酯己酸乙酯辛酸乙酯乙酸异戊酯苯甲醛糠醛乙酸丙酸辛酸1 342.17±83.81c 96.08±4.25c 35.22±2.40a 10.21±1.66c 2.99±0.11b 5.21±0.23a 5.63±0.09c 1.43±0.14a 0.64±0.14a 10.60±1.32a 0.76±0.03a 0.61±0.10b 1 364.05±124.93c 102.02±5.54c 32.87±1.84a 13.22±0.58b 2.08±0.40d 4.66±0.14b 6.22±0.38b 1.03±0.12b 0.68±0.11a 8.55±2.78ab 0.77±0.03a 0.44±0.09b 1 440.25±113.23bc 128.24±3.51a 28.12±1.38b 14.22±0.94a 2.61±0.16c 4.72±0.25b 6.24±0.48b 1.11±0.13b 0.58±0.11a 8.67±2.32ab 0.75±0.02a 0.45±0.12b 1 679.31±62.04a 133.21±6.22a 26.46±2.54bc 14.90±1.45a 4.09±0.32a 5.16±0.18a 6.54±0.20a 0.98±0.21b 0.56±0.07a 7.81±1.09b 0.70±0.02b 0.44±0.11b 1 542.50±43.42b 116.57±2.36b 24.06±2.58c 13.17±1.03b 2.75±0.31bc 5.03±0.25ab 6.22±0.11b 0.95±0.12b 0.42±0.05b 11.96±2.45a 0.74±0.01a 0.79±0.15a
由表1亦可知,不同温度的热应激预处理对毕赤酵母发酵过程中有机酸的代谢调控具有显著影响。在42 ℃预处理条件下,乙酸、丙酸和辛酸的含量分别降至7.81 mg/L、0.70 mg/L和0.44 mg/L,显著低于对照组及其他温度组(P<0.05)。然而,当预处理温度升高至44 ℃时,上述有机酸含量呈现显著上升趋势,乙酸、丙酸和辛酸的含量分别增长至11.96 mg/L、0.74 mg/L和0.79 mg/L,这一现象可能与热应激诱导的氧化还原平衡调控密切相关。研究证实,适温预处理能够有效激活毕赤酵母的抗氧化防御系统,超氧化物歧化和过氧化氢的活性显著提升[20],从而减少活性对关键代谢酶的氧化损伤。在此条件下,丙酮酸脱氢酶的活性得以维持,进而推动丙酮酸高效进入三羧酸循,而非通旁路途径生成乙酸。而当预处理温度超过44 ℃时,细胞膜完整性受损,丙酮酸脱羧酶热稳定性下降[21]。此时,丙酮酸代谢流向发生变化:一方面,丙酮酸脱氢酶复合体的活性因辅酶A供应不足而受到抑制;另一方面,醛脱氢酶在缺氧微环境中的表达上调,促使丙酮酸通过乙醛中间体大量转化为乙酸[22]。因此,42 ℃预处理组中有机酸含量的降低对发酵品质具有双重意义:其一,减少乙酸积累可避免发酵液pH值过度下降,维持酵母细胞膜电势稳定;其二,丙酸和辛酸的浓度控制有效抑制不良风味的产生。
2.4 热应激预处理对菌株PK8胞内pH值的影响
为解析热应激预处理对酵母菌高温耐受性的调控机制,对胞内pH值的动态变化进行了分析,结果见图3。由图3可知,对照组(28 ℃)胞内pH值为6.52,而随着预处理温度升高,胞内pH值呈现显著下降趋势。这是由于高温会导致细胞膜脂质双分子层流动性增加,影响细胞膜的通透性和离子转运功能,促使H+被动内流,从而降低胞内pH值[23]。当热应激温度达到44 ℃时,胞内pH值降低至5.45。表明适度的热应激预处理可能激活质子泵(如H+-ATP酶),通过主动外排H+部分抵消内流效应,以维持离子平衡[24],而极端高温(44 ℃)导致质子泵的关键酶热变性失活,丧失质子外排能力。此外,热胁迫还会导致酵母菌代谢产物的变化,进而间接影响胞内pH值。结合高温发酵下主要挥发性代谢产物结果可知,在高温条件下,酵母菌可能会产生更多的有机酸,这些有机酸的积累会进一步降低胞内pH值。
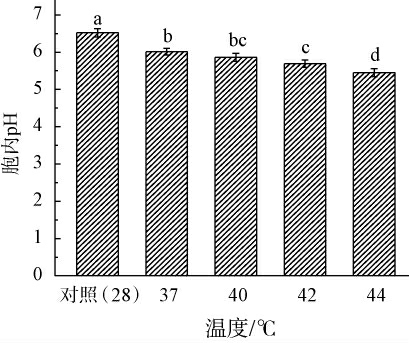
图3 热应激温度对菌株PK8胞内pH值的影响
Fig.3 Effect of thermal stress temperature on intracellular pH values of strain PK8
2.5 热应激预处理对菌株PK8应激响应的影响
ROS是由细胞内氧化还原状态失衡而引起的氧化应激产生的,细胞内积累的过量ROS会直接作用于脱氧核糖核酸(deoxyribonucleic acid,DNA)、蛋白质和脂质等生物大分子,造成细胞氧化损伤[25]。同时,这些ROS也可以作为信号分子来调节基因的表达,诱导细胞发生级联反应,最终影响细胞的活性,使细胞凋亡或坏死[26]。因此,酵母菌胞内的ROS水平是在胁迫环境受到氧化程度的间接反映。测定酵母菌在5个不同热应激温度下培养90 min的ROS水平,以荧光强度表示,结果见图4。由图4可知,相较于对照组,热应激处理条件下的酵母菌的胞内ROS水平均显著提升。表明预处理温度的增加会导致酵母菌细胞遭受到的氧化胁迫程度加重,进而引发胞内ROS的积累。当热应激温度为42 ℃时,ROS水平较37 ℃条件下降了29.90%,较40 ℃条件下降了39.69%,达到了除对照组以外的最低值。这一现象可能与热应激诱导的抗氧化系统高效响应相关。
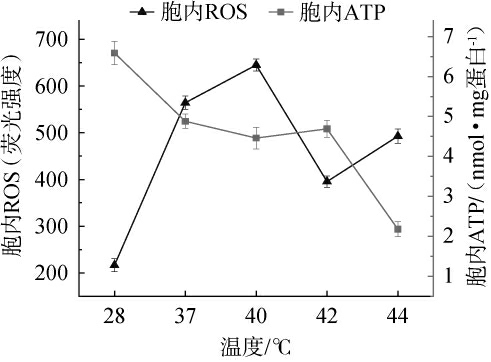
图4 热应激温度对菌株PK8胞内活性氧簇和三磷酸腺苷含量的影响
Fig.4 Effect of thermal stress temperature on intracellular reactive oxygen species and adenosine triphosphate contents of strain PK8
ATP作为一种丰富且必需的代谢物,参与了细胞生长、繁殖以及对外界环境变化时的应对活动等进程。当菌体受到环境胁迫时,ATP也会通过参与细胞的应激反应来进行防御[27]。因此,本研究通过观察酵母菌胞内ATP含量的变化,来探究氧化胁迫对酵母菌能量代谢产生的影响,结果见图4。由图4可知,酵母菌胞内ATP含量随热应激温度的升高而显著降低,一旦温度超过42 ℃将呈现急速下降趋势。这可能是由于酵母菌在应对热应激胁迫引起的氧化应激时,其细胞内部所进行的防御活动需要ATP的参与,ATP的过多消耗使得ATP的生产速度“供不应求”。当菌体细胞热应激程度较大,造成的氧化损伤较严重时,胞内ATP的生产进程也会受到不可逆的影响。
2.6 热应激预处理对菌株PK8膜脂肪酸的影响
在面对环境胁迫时,酵母菌会通过调节细胞膜脂肪酸的组成来增强自身的适应能力[28]。这种调节机制不仅有助于维持细胞膜的流动性,还能保护细胞免受外界不利条件的影响[29]。不同热应激温度下,酵母菌细胞膜脂肪酸组成的影响见图5。由图5A和5B可知,随着预处理温度升高(28~42 ℃),不饱和脂肪酸(C18∶1、C18∶2、C18∶3)比例显著增加,而饱和脂肪酸(C15∶0、C16∶0、C18∶0)比例同步下降。其中,42 ℃预处理组的油酸(C18∶1)含量达到34.68%,较对照组提升33.25%;亚油酸(C18∶2)含量增至24.92%(提升41.57%),而棕榈酸(C16∶0)和硬脂酸(C18∶0)较对照组分别降低32.20%和35.98%。不饱和脂肪酸因其双键结构而具有弯曲性,能够使细胞膜在高温下保持适当的流动性,从而维持细胞膜的柔韧性和功能[30]。毕赤酵母通过动态调节膜脂不饱和度,一方面防止高温导致的膜破裂,另一方面维持跨膜物质运输效率,在高温环境中维持菌株正常的生理功能[31]。

图5 热应激温度对菌株PK8细胞膜脂肪酸组成的影响
Fig.5 Effect of thermal stress temperature on the fatty acid composition of the cell membrane in strain PK8
(A)不饱和脂肪酸;(B)饱和脂肪酸;(C)不饱和度;(D)平均碳链长度。
由图5C可知,当热应激温度提升至44 ℃时,尽管不饱和脂肪酸与饱和脂肪酸的比值仍较对照组(28 ℃)提高,但较42 ℃条件下的峰值显著下降。这一现象表明,极端高温已突破酵母菌膜脂代谢的调控阈值。其机制可能涉及以下多因素协同作用:①去饱和酶系统的功能失活。高温抑制去饱和酶基因的转录调控,进一步限制不饱和脂肪酸的生物合成[32]。②氧化损伤与代谢抑制的级联效应。结合热应激预处理对菌株应激响应的影响也可推断,ROS水平激增可能引发多不饱和脂肪酸的链式氧化,导致膜脂双层结构破坏。ATP合成速率也大幅降低,致使脂质重塑所需的能量供应不足。③膜物理特性的逆向调控。在44 ℃条件下,饱和脂肪酸比例回升,导致膜刚性增加[33]。跨膜运输和信号传导受到一定抑制作用,从而超出酵母菌膜脂代谢的动态调控范围。
细胞膜脂肪酸的平均碳链长度是细胞膜结构和功能的重要指标,它反映了细胞膜的流动性和稳定性,同时也与细胞的生理状态和环境适应能力密切相关[34]。由图5D可知,当热应激温度由28 ℃增加至40 ℃,平均碳链长度由17.45下降至16.95,这表明细胞通过合成短链脂肪酸增强膜流动性以应对温和热应激。热应激温度升高到42 ℃时,平均碳链长度回升至17.34,接近对照组水平。这说明膜脂组成发生特异性调整:不饱和脂肪酸(如C18∶2、C18∶3)比例增加,通过双键的引入降低膜相变温度,同时长链脂肪酸(如C18∶0)的适度保留可防止膜过度流动导致的渗漏[35]。
3 结论
本研究探究了不同温度热应激预处理对P.kudriavzevii菌株PK8高温耐受性、代谢特性和胞内环境的调控作用。实验结果表明,42 ℃热应激预处理90 min对PK8的高温发酵性能提升效果最为显著。这一处理通过调节胞内环境稳态、平衡糖酵解与酯类物质合成通路,优化代谢流分布,显著增强了菌株的高温耐受性和发酵性能。细胞膜中不饱和脂肪酸与饱和脂肪酸的比值在此条件下达到最大值,膜流动性显著增强,从而为细胞在高温环境下的稳定性和功能性提供了有力支持。
未来的研究可以集中以下几方面:评估热应激预处理对酵母在长时间、大规模发酵条件下的耐受性和代谢稳定性;评估热应激预处理的普适性和特异性;结合转录组学、蛋白质组学和代谢组学技术,深入探究热应激预处理对酵母细胞的调控机制。通过进一步探索热应激预处理的长期效应、菌株差异性以及分子机制,为工业发酵工艺的优化提供更全面深入的理论基础和实践指导。
[1]郭欣然,田缘,孔保华,等.发酵食品中微生物交叉保护策略及其作用机制研究进展[J].食品科学,2024,45(18):232-241.
[2]YANG H, HE M, WU C.Cross protection of lactic acid bacteria during environmental stresses: Stress responses and underlying mechanisms[J].LWT-Food Sci Technol,2021,144:111203.
[3]刘秋影,李春生,杨贤庆,等.基于TMT的定量蛋白质组学技术解析盐胁迫提高库德毕赤酵母耐热性机制[J].食品科学,2022,43(14):102-110.
[4]潘婉舒,林晓芳,杨小平,等.乳酸胁迫对Pichia kudriavzevii固态发酵特性的影响[J].食品工业科技,2024,45(4):116-122.
[5]KHAN M A,ASAF S,KHAN A L,et al.Thermotolerance effect of plant growth-promoting Bacillus cereus SA1 on soybean during heat stress[J].BMC Microbiol,2020,20:1-14.
[6]TSAI S H, HSIAO Y C, CHANG P E, et al.Exploring the biologically active metabolites produced by Bacillus cereus for plant growth promotion,heat stress tolerance,and resistance to bacterial soft rot in Arabidopsis[J].Metabolites,2023,13(5):676.
[7]陈家露,支飞杰,李胜男,等.ycjX和ycjF基因在布鲁氏菌热应激中的作用[J].微生物学通报,2022,49(12):5159-5170.
[8]庄若茹,张巧玲,王俊国.不同应激处理方式对乳酸菌喷雾干燥过程中存活率的影响及内在机制[J].乳业科学与技术,2022,45(1):55-60.
[9]LOPEZ V,CAUVI D M,ARISPE N,et al.Bacterial Hsp70 (DnaK) and mammalian Hsp70 interact differently with lipid membranes[J].Cell Stress Chaperones,2016,21(4):609-616.
[10]CORTEGGIANI M, BOSSUET-GREIF N, NOUGAYRÈDE J P, et al.Uncoupling the Hsp90 and DnaK chaperone activities revealed the in vivo relevance of their collaboration in bacteria[J].Proc Natl Acad Sci,2022,119(37):e2201779119.
[11]王定康,张良,邹江鹏,等.盐预适应对鲁氏酵母菌高盐胁迫抗性的影响[J].食品科学技术学报,2021,39(3):73-79,128.
[12]吴重德.干酪乳杆菌抵御酸胁迫的生理机制解析[D].无锡:江南大学,2012.
[13]BREEUWER P, DROCOURT J, ROMBOUTS F M, et al.A novel method for continuous determination of the intracellular pH in bacteria with the internally conjugated fluorescent probe 5(and 6-)-carboxyfluorescein succinimidyl ester[J].Appl Environ Microbiol,1996,62(1):178-183.
[14]ZHANG H,KONG B,LIU H,et al.Physiology and antioxidant activity of Pediococcus pentosaceus R1 and Lactobacillus fermentum R6 in response to lactic acid stress[J].LWT-Food Sci Technol,2021,149:111878.
[15]ZHENG J, LIANG R, ZHANG L, et al.Characterization of microbial communities in strong aromatic liquor fermentation pit muds of different ages assessed by combined DGGE and PLFA analyses[J].Food Res Int,2013,54(1):660-666.
[16]KANG J, HUANG X, LI R, et al.Deciphering the core microbes and their interactions in spontaneous Baijiu fermentation: A comprehensive review[J].Food Res Int,2024,188:114497.
[17]CHAMNIPA N,THANONKEO S,KLANRIT P,et al.The potential of the newly isolated thermotolerant yeast Pichia kudriavzevii RZ8-1 for high-temperature ethanol production[J].Braz J Microbiol,2018,49(2):378-391.
[18]王倩,黄建春,卜乐男,等.双孢蘑菇对高温胁迫的响应及耐热机理[J].菌物学报,2021,40(6):1400-1412.
[19]吕蕊花,杨大群,杜雨彤,等.核盘菌热休克蛋白Hsp70基因的克隆及功能分析[J].生物工程学报,2024,40(10):3677-3688.
[20]程哲.热激处理增强生防酵母菌(Rhodotorula mucilaginosa)抗逆性及生防效力的研究[D].合肥:合肥工业大学,2016.
[21]STEVENSON B J, LIU J W, OLLIS D L.Directed evolution of yeast pyruvate decarboxylase 1 for attenuated regulation and increased stability[J].Biochemistry,2008,47(9):3013-3025.
[22]牛屹帆,董婷婷,李杏泽,等.丙酮酸生物代谢途径及代谢控制的研究进展[J].环境化学,2025,44(4):1195-1204.
[23]聂铭,杨裕然,李振轮.微生物胞内外pH稳态维持机制研究进展[J].微生物学报,2024,64(1):1-13.
[24]TRIANDAFILLOU C G, KATANSKI C D, DINNER A R, et al.Transient intracellular acidification regulates the core transcriptional heat shock response[J].eLife,2020,9:e54880.
[25]ZANDI P,SCHNUG E.Reactive oxygen species,antioxidant responses and implications from a microbial modulation perspective[J].Biology,2022,11(2):155.
[26]孙宸婧,顾安睿,曾若云,等.外源物质提高发酵过程抗逆性的研究进展[J].中国生物工程杂志,2025,45(5):71-79.
[27]程万琪,侯骞尧,刘春凤,等.线粒体自噬基因对酿酒酵母抗氧化性能的影响[J].生物工程学报,2023,39(8):3464-3480.
[28]刘安,王丹阳,王振,等.高耐受性酿酒酵母的适应性驯化选育与发酵[J].微生物学通报,2024,51(3):1018-1032.
[29]王府,申家鑫,石侃,等.耐酸和酸敏感酒酒球菌突变株酸胁迫下膜脂肪酸差异分析[J].中国酿造,2023,42(7):51-57.
[30]包秋华,代利霞,梅迩蓝.干酪乳杆菌Zhang在不同温度下的膜脂肪酸变化分析[J].中国乳品工业,2022,50(7):9-14.
[31]梅迩蓝,包秋华.细菌在逆境条件下膜脂肪酸变化的研究进展[J].微生物学杂志,2022,42(5):105-112.
[32]PHONG H X,KLANRIT P,DUNG N T P,et al.High-temperature ethanol fermentation from pineapple waste hydrolysate and gene expression analysis of thermotolerant yeast Saccharomyces cerevisiae[J].Sci Rep,2022,12(1):13965.
[33]张爱静,李琳琼,王鹏杰,等.热胁迫对大肠杆菌细胞膜和膜蛋白的影响[J].中国农业科学,2020,53(5):1046-1057.
[34]BATSALE M,BAHAMMOU D,FOUILLEN L,et al.Biosynthesis and functions of very-long-chain fatty acids in the responses of plants to abiotic and biotic stresses[J].Cells,2021,10(6):1284.
[35]许婉馨,范睿,凌铭煌,等.深海胶红酵母的低温适应性机制初步解析[J].菌物学报,2024,43(10):133-143.