烟酰胺单核苷酸(nicotinamide mononucleotide,NMN)是一种具有显著抗衰老和健康促进作用的生物活性分子,其可在烟酰胺单核苷酸腺苷酸转移酶(nicotinamide phosphoribosyltransferase,NMNAT)的催化作用下转化为烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide,NAD+)[1]。NAD+作为细胞代谢的核心辅因子,在脱氧核糖核酸(deoxyribonucleic acid,DNA)损伤修复、细胞凋亡、自噬调控、表观遗传修饰及衰老进程等关键生物学过程中发挥重要调控作用[2-3]。鉴于NMN广泛的生理功能,其已成为医药、保健品及化妆品领域的研究热点。
传统NMN的合成主要依赖化学合成法,但该方法存在反应条件苛刻、产物安全性低及环境污染等问题[4-5]。近年来,酶催化法和微生物发酵法因其绿色高效的特点受到广泛关注。其中,酶法虽然转化效率较高,但存在酶成本高昂、工艺稳定性差等局限[6-8]。然而,微生物发酵法因其操作简便、无需复杂酶纯化步骤且生产成本较低,展现出良好的工业化应用前景。目前,细胞内NMN的生物合成主要依赖两条代谢途径:①以烟酰胺核糖(nicotinamide ribose,NR)和腺嘌呤核苷三磷酸(adenosine triphosphate,ATP)为底物,在烟酰胺核糖激酶(nicotinamide ribokinase,NRK)催化下生成NMN;②以5-磷酸核糖焦磷酸(5-phosphoribosyl pyrophosphate,PRPP)和 烟酰 胺(niacinamide,NAM)为 前体,在烟酰胺磷酸核糖转移酶(nicotinamide phosphoribo syltransferase,NAMPT)的介导下合成NMN(图1)[9]。相较于第一条途径,利用大肠杆菌(Escherichia coli)生产NMN时,采用第二条途径(以烟酰胺和葡萄糖为底物)可显著降低生产成本并简化工艺流程,从而提高产量[9]。然而,NMN的发酵生产仍面临产物抑制问题。DHATT S等[10]研究发现,随着NMN积累,其反馈抑制效应会导致反应速率下降,从而限制最终产量。针对这一问题,廖一波[5]通过酶分子改造(如定点饱和突变)有效缓解了产物抑制,显著提升了NMN的合成效率。
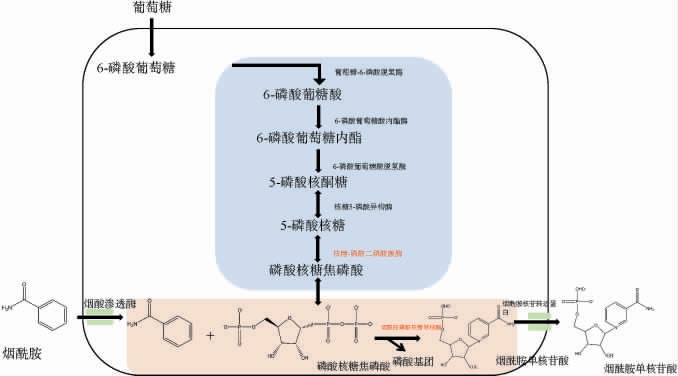
图1 以烟酰胺和葡萄糖为底物微生物发酵合成烟酰胺单核苷酸途径
Fig.1 Microbial fermentation pathway for the synthesis of nicotinamide mononucleotide using nicotinamide and glucose as substrates
基于此,本研究选取隐球菌科(Comamonadaceae)细菌来源的NAMPT基因在大肠杆菌(Escherichia coli)BL21(DE3)中进行异源表达。以其为出发菌株,以NAMPT作为受体、NMN小分子作为配体,采用分子对接技术确定突变位点,并采用同源重组技术构建突变菌株。通过测定NMN产量及NAMPT活力筛选得到高产NMN突变菌株,并通过单因素试验对其诱导条件进行优化,以期获得NMN高产菌株,为工业化生产提供优化策略。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株、质粒和引物
大肠杆菌(Escherichia coli)BL21(DE3)、pET-28a(+)质粒:天津北洋百川生物技术有限公司。本研究聚合酶链式反应(polymerase chain reaction,PCR)扩增所用引物见表1。
表1 本研究聚合酶链式反应扩增所用引物
Table 1 Primers used for polymerase chain reaction amplification in this study
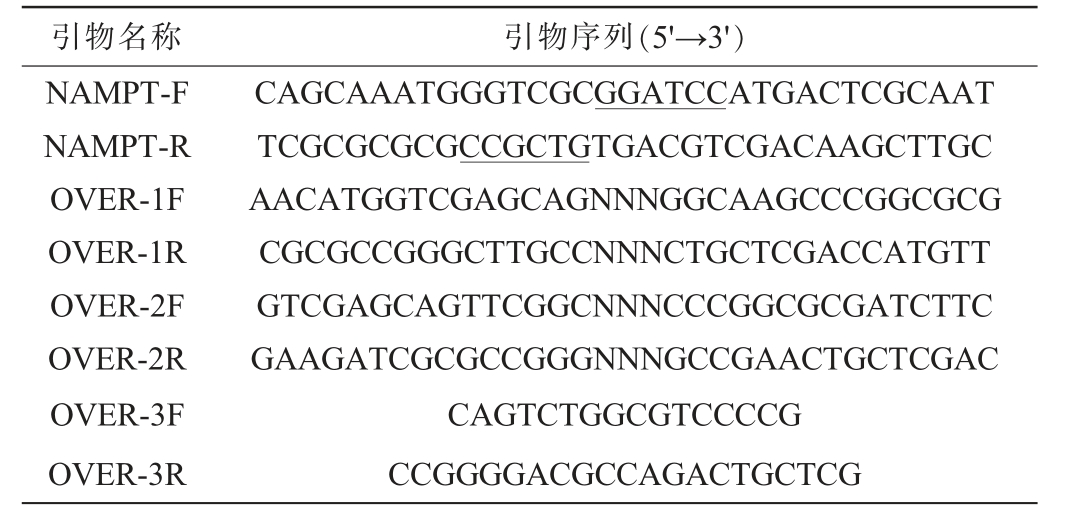
注:下划线为酶切位点。
引物名称 引物序列(5'→3')NAMPT-F NAMPT-R OVER-1F OVER-1R OVER-2F OVER-2R OVER-3F OVER-3R CAGCAAATGGGTCGCGGATCCATGACTCGCAAT TCGCGCGCGCCGCTGTGACGTCGACAAGCTTGC AACATGGTCGAGCAGNNNGGCAAGCCCGGCGCG CGCGCCGGGCTTGCCNNNCTGCTCGACCATGTT GTCGAGCAGTTCGGCNNNCCCGGCGCGATCTTC GAAGATCGCGCCGGGNNNGCCGAACTGCTCGAC CAGTCTGGCGTCCCCG CCGGGGACGCCAGACTGCTCG
1.1.2 化学试剂
葡萄糖、酵母抽提物、氯化钠、烟酰胺、卡那霉素、氨苄青霉素、盐酸壮观霉素、异丙基-β-D-硫代半乳糖苷(isopropylβ-D-thiogalactoside,IPTG)、葡萄糖、烟酰胺、Tris-HCl、氯化镁、甲酸、苯乙酮(均为分析纯):上海源叶生物有限公司;DP103-03质粒小提试剂盒;天根生化科技(北京)有限公司、![]() PCR Purification Kit:翌圣生物科技(上海)股份有限公司。其他试剂均为国产分析纯。
PCR Purification Kit:翌圣生物科技(上海)股份有限公司。其他试剂均为国产分析纯。
1.1.3 培养基
LB液体培养基[5]:胰蛋白胨10 g/L,酵母粉5 g/L,NaCl 10 g/L,蒸馏水1 000 mL,121 ℃高压蒸汽灭菌20 min。LB固体培养基:在LB液体培养基中添加20 g/L琼脂。
SOC液体培养基[5]:D-葡萄糖3.6 g/L,胰蛋白胨10 g/L,酵母粉5 g/L,NaCl 10 g/L,KCl 0.19 g/L,MgCl2 0.95 g/L,蒸馏水1 000 mL,115 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
GR22G冷冻离心机:日本日立公司;SKY-2102恒温型摇床:上海苏坤实业有限公司;LC-20A高效液相色谱(high performance liquid chromatography,HPLC)仪、UV-2600紫外-可见分光光度计:日本岛津公司;![]() 200 PRO多功能酶标仪:瑞士Tecan公司;Tanon天能EPS-300电泳仪:深圳艾维迪泰生物科技有限公司;SW-CJ-IFD超净工作台:上海知楚实验室设备有限公司;T30 PCR仪:杭州朗基科学仪器有限公司;JY88-PRO超声波细胞粉碎机:宁波新芝生物有限公司。
200 PRO多功能酶标仪:瑞士Tecan公司;Tanon天能EPS-300电泳仪:深圳艾维迪泰生物科技有限公司;SW-CJ-IFD超净工作台:上海知楚实验室设备有限公司;T30 PCR仪:杭州朗基科学仪器有限公司;JY88-PRO超声波细胞粉碎机:宁波新芝生物有限公司。
1.3 方法
1.3.1 NAMPT三维结构模型构建及突变位点的确定
将NAMPT的基因编码序列翻译为对应的氨基酸序列,随后利用SWISS-MODEL同源建模平台构建其三维蛋白质结构模型。将获得的3D模型导入PyMOL分子可视化软件(v3.1)进行结构优化处理,包括去除非蛋白小分子配体和水分子等。采用ChemDraw16.0.0.82构建NMN的三维分子结构模型。以处理后的NAMPT结构作为受体、NMN作为配体,采用AutoDock分子对接软件(v4.2)进行分子对接模拟[11-18]。对接完成后,筛选结合自由能最低的复合物构象输出。通过OpenBabel化学信息学工具进行文件格式转换后,再次使用PyMOL分子可视化软件(v3.1)进行结构分析,鉴定出关键结合位点残基。
1.3.2 突变菌株的构建及验证
从美国国家生物技术信息中心(National Center for Biotechnology Information,NCBI)的GenBank数据库获取Comamonadaceae bacterium来源的NAMPT基因编码序列(NCBI:RYF34637.1),并采用NovoPro在线工具针对大肠杆菌表达系统对其进行密码子优化。优化后的基因序列由九天基因公司完成全基因合成,并克隆至pET-28a(+)表达载体的多克隆位点,构建重组质粒pET-28a-NAMPT。将重组质粒pET-28a-NAMPT转入E.coli BL21(DE3)感受态细胞中,通过PCR扩增、测序获得正确的重组菌株,将其命名为出发菌株。
通过前期研究发现,在NAMPT的基因编码序列翻译为对应的氨基酸序列中第257位的苯丙氨酸突变为色氨酸,第259位的赖氨酸突变为缬氨酸时,NMN产量升高显著。因此,以NAMPT-F、OVER-1R和OVER-1F、NAMPT-R作为引物,NAMPT基因作为模板进行PCR扩增,PCR扩增产物经1%琼脂糖凝胶电泳检测合格后,纯化回收片段,以NAMPT-F、NAMPT-R为引物进行重叠延伸PCR,再与酶切好的pET-28a(+)载体进行同源重组,得到重组质粒。通过热激法将重组质粒转化至E.coli BL21(DE3)感受态细胞中。将转化产物涂布于含卡那霉素(50 μg/mL)的LB固体培养基平板,37 ℃恒温培养12~16 h。挑取单菌落作为模板,采用引物NAMPT-F、NAMPT-R进行菌落PCR。PCR扩增体系:模板1 μL,上下游引物各1 μL,2×Ape×HF CL PCR Master Mix 25 μL,双蒸水22 μL。PCR扩增条件:98 ℃预变性2 min;98 ℃变性10 s,60 ℃退火30 s,72 ℃延伸90 s,共30个循环;72 ℃再延伸10 min。将PCR扩增产物送至苏州金唯智生物科技有限公司进行测序,以验证目的基因片段与质粒连接情况。采用SnapGene软件(v5.2.0)对突变前后的测序结果进行比对,将测序正确的重组菌株命名为N1(第257位苯丙氨酸突变为色氨酸)。同理,以NAMPT-F、OVER-2R和OVER-2F、NAMPT-R为引物,通过PCR、转化、测序获得正确的重组菌株命名为N2(将第259位赖氨酸突变为缬氨酸)。以NAMPT-F、OVER-1F和OVER-1R、NAMPT-R作为引物,通过PCR、转化、测序获得正确的重组菌株命名为N3(将第257位苯丙氨酸突变为色氨酸和第259位赖氨酸突变为缬氨酸)。
1.3.3 突变菌株的NMN诱导表达及筛选
将出发菌株及突变菌株(N1、N2、N3)接种至LB液体培养基中,37 ℃、220 r/min条件下培养12 h作为种子液,将种子液的OD600nm值调整至0.8,以1%(V/V)的接种量转接至LB液体培养基中,装液量为50 mL/250 mL,于37 ℃、220 r/min条件下振荡培养至OD600nm值为0.8时,加入1 mmol/L IPTG,37 ℃、220 r/min条件下诱导表达12 h,再添加1 g/L葡萄糖和1 g/L烟酰胺培养12 h时,取样,采用HPLC法测定NMN产量[9],参考文献[19]测定NAMPT活力。
1.3.4 突变菌株产NMN诱导表达条件优化
挑取NMN产量最高的突变菌单菌落接种于含50μg/mL卡那霉素的LB液体培养基中,装液量为50 mL/250 mL,37 ℃、220 r/min条件下振荡培养至OD600nm值分别为0.6、0.8、1.0、1.2、1.4时,加入终浓度为1 mmol/L的IPTG诱导12 h,再添加1 g/L葡萄糖和1 g/L烟酰胺培养12 h后,取样测定NMN的产量,并采用紫外分光光度计在波长600 nm处测定吸光度值(OD600nm值)。在此基础上,分别考察IPTG浓度(0.2 mmol/L、0.4 mmol/L、0.6 mmol/L、0.8 mmol/L、1.0 mmol/L)[20]、诱导时间(8 h、10 h、12 h、14 h和16 h)诱导温度(25 ℃、30 ℃、35 ℃、40 ℃和45 ℃)及投料比(葡萄糖∶烟酰胺)(1∶3、1∶2、1∶1、2∶1、3∶1)[21]对突变菌株生长及产NMN的影响。
1.3.5 数据处理与统计分析
每个试验重复3次,采用SPSS及Origin 2021进行方差分析和作图,采用DNAMAN Raindy汉化版将NDA序列翻译为氨基酸序列,采用Chem3D 2021对NMN小分子进行3D建模。
2 结果与分析
2.1 NAMPT三维结构模型构建及突变位点的确定
为了防止反应生成的NMN与NAMPT结合占据与本该与底物NAM结合的活性位点或者阻挡底物NAM进入活性位点的通道,采用ChemDraw16.0.0.82、SWISS-MODEL分别构建NMN、NAMPT的三维分子结构模型,使用AutoDock分子对接软件(v4.2)将NAMPT与NMN进行分子对接模拟,结果见图2。由图2可知,对接能量最低的位点为257位苯丙氨酸(phenylalanine,Phe)(密码子TTT)和259位赖氨酸(lysine,Lys)(密码子AAG)。因此,确定Phe257和Lys259为突变位点。
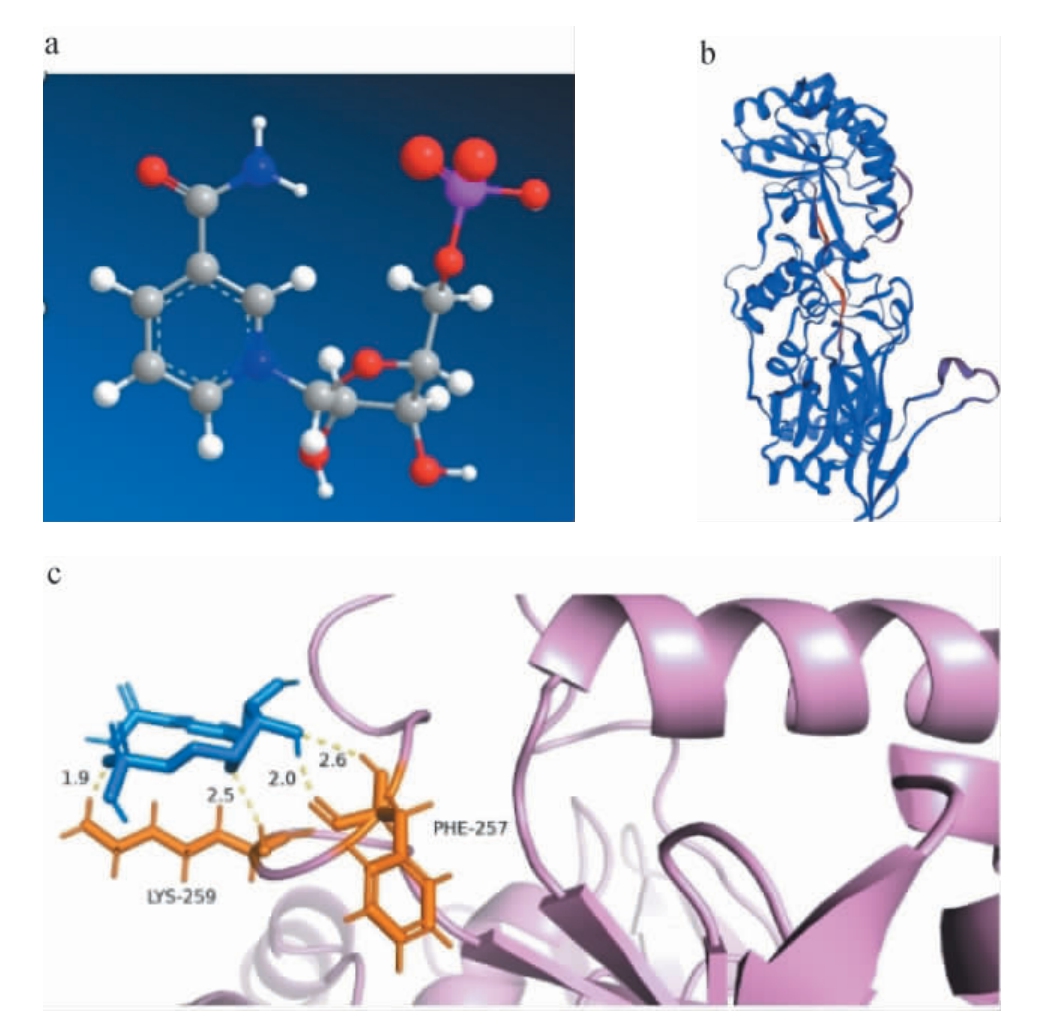
图2 烟酰胺单核苷酸(a)、烟酰胺磷酸核糖转移酶(b)的三维分子结构模型及分子对接模拟结果(c)
Fig.2 Three-dimensional molecular structure models of nicotinamide mononucleotide (a) and nicotinamide phosphoribosyltransferase(b) and molecular docking simulation results (c)
2.2 突变菌株的构建及验证
通过菌落PCR及测序对突变体N1~N3进行验证,测序结果见图3。由图3a可知,通过SnapGene软件(v5.2.0)对突变前后的测序结果进行比对,发现突变体N1 257位的Phe(密码子TTT)突变为了色氨酸(tryptophan,Trp)(密码子TCT);突变体N2 259位的Lys(密码子GTC)突变为了缬氨酸(valine,Val)(密码子AAG);突变体N3 257位的Phe(密码子TTT)突变为了Trp(密码子TCT),且259位的Lys(密码子GTC)突变为了Val(密码子AAG),说明突变体构建成功。
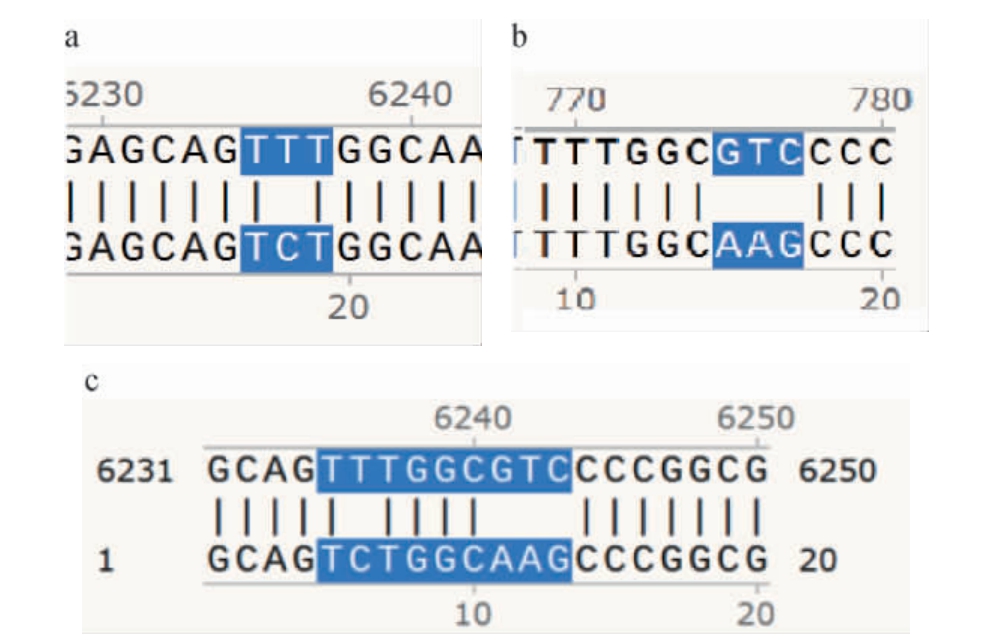
图3 突变菌株N1(a)、N2(b)及N3(c)的测序验证结果
Fig.3 Sequencing verification results of the mutant strains N1 (a),N2 (b) and N3 (c)
2.3 突变菌株的筛选
出发菌株及突变体N1、N2、N3的NMN产量及NAMPT活力测定结果见图4。由图4可知,突变体N1、N2、N3的NMN产量分别为6.88 mg/L、9.38 mg/L、10.05 mg/L,相比出发菌株分别显著提高5.30%、43.60%、46.10%(P<0.05);NAMPT活力分别为42.08 U/mL、46.23 U/mL、50.30 U/mL,相较于出发菌株分别提高5.73%、14.19%、21.13%。结果表明,双位点突变体N3的NMN产量及NAMPT活力均显著最高(P<0.05),其NMN产量与MARINESCU G C等[21]优化后的NMN产量水平相当。
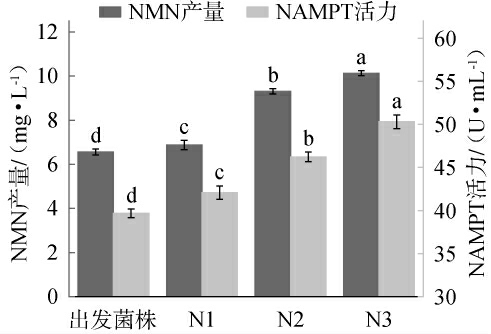
图4 出发菌株及突变菌株烟酰胺单核苷酸产量及烟酰胺磷酸核糖转移酶活力测定结果
Fig.4 Determination results of nicotinamide mononucleotide yield and nicotinamide phosphoribosyltransferase activities in the starting strain and mutant strain
不同小写字母表示差异显著(P<0.05)。
2.4 突变菌株N3产NMN诱导表达条件优化
2.4.1 诱导时机的选择
诱导时机对突变菌株N3生长及NMN产量的影响见图5。由图5可知,随着诱导时机的延长,NMN产量及OD600nm值均呈先升高后下降的趋势。当诱导时机(OD600 nm值)为1.2时,NMN产量最高,为12.00 mg/L,OD600 nm值为2.20。但在诱导时机(OD600nm值)为0.8时,OD600nm值最高,为2.29。分析原因可能是在OD600nm值较小时进行诱导,菌株主要进行生长,代谢产生的NMN较少,但OD600nm值较大时进行诱导,菌株代谢产生的废物可能抑制菌株的生长,进而导致NMN产量下降。因此,确定最佳诱导时机(OD600nm值)为1.2。
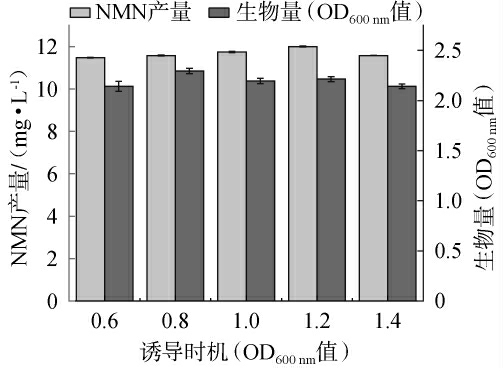
图5 诱导时机对突变菌株N3生长及烟酰胺单核苷酸产量的影响
Fig.5 Effect of induction timing on growth and nicotinamide mononucleotide yield of mutant strain N3
2.4.2 诱导剂浓度的选择
诱导剂浓度对突变菌株N3生长及NMN产量的影响见图6。由图6可知,随着诱导剂浓度的升高,NMN产量及OD600 nm值均呈现先升高后下降的趋势,当诱导剂浓度为0.50 mmol/L时,NMN产量最高,为12.20 mg/L,OD600nm值为2.00。但在诱导剂浓度为0.75 mmol时OD600 nm值最高,为2.10。分析原因可能是当诱导剂浓度为0.75 mmol/L时,蛋白合成速率超过分子伴侣辅助的折叠能力,错误折叠蛋白比例增加[22-23]。然而,当诱导剂浓度为0.50 mmol/L时,IPTG在菌体生长和蛋白功能表达间达到较优平衡。因此,确定最佳诱导剂浓度为0.5 mmol/L。
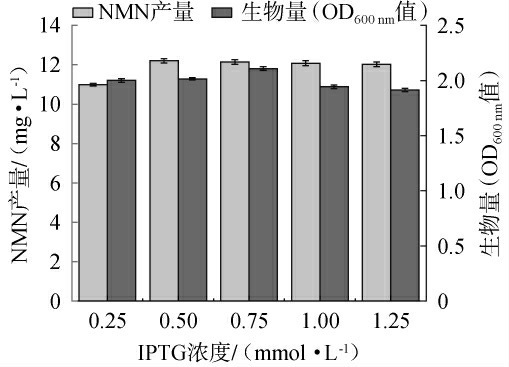
图6 诱导剂浓度对突变菌株N3生长及烟酰胺单核苷酸产量的影响
Fig.6 Effect of inducer concentration on growth and nicotinamide mononucleotide yield of mutant strain N3
2.4.3 诱导时间的选择
诱导时间对突变菌株N3生长及NMN产量的影响见图7。由图7可知,随着诱导时间的延长,NMN产量和OD600nm值均呈先升高后降低的趋势,当诱导时间为12 h时,NMN产量和OD600nm值均达到最高,分别为12.30 mg/L、2.00,表明此时细胞内功能性NAMPT的表达已实现充分积累并趋于稳定。分析原因可能是诱导时间过短,NAMPT表达不充足,催化效率不高;诱导时间过长,代谢负担加重或底物消耗导致菌体衰老、自溶,效率降低[20]。因此,确定最佳诱导时间为12 h。
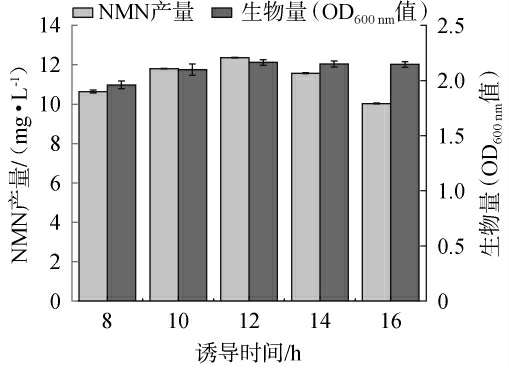
图7 诱导时间对突变菌株N3生长及烟酰胺单核苷酸产量的影响
Fig.7 Effect of induction time on growth and nicotinamide mononucleotide yield of mutant strain N3
2.4.4 诱导温度的选择
诱导温度对突变菌株N3生长及NMN产量的影响见图8。由图8可知,随着诱导温度的升高,NMN产量和OD600nm值均呈先升高后降低的趋势,当诱导温度为30 ℃时,NMN产量和OD600 nm值均达到最高,分别为12.80 mg/L、2.00。分析原因可能是,诱导温度过低或过高,都会影响菌株的生长以及NAMPT的活性,进而导致NMN产量降低[20,24]。因此,确定最佳诱导温度为30 ℃。
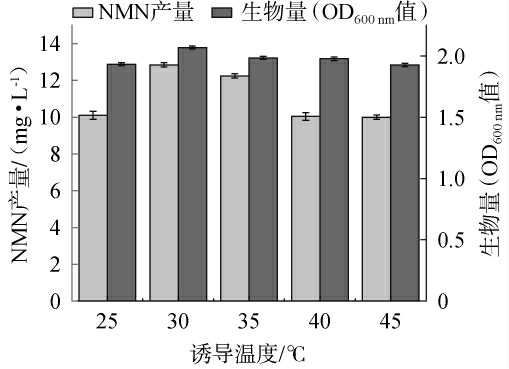
图8 诱导温度对突变菌株N3生长及烟酰胺单核苷酸产量的影响
Fig.8 Effect of induction temperature on growth and nicotinamide mononucleotide yield of mutant strain N3
2.4.5 投料比的选择
投料比(葡萄糖∶烟酰胺)对突变菌株N3生长及NMN产量的影响见图9。由图9可知,随着葡萄糖含量的升高,NMN产量和OD600 nm值均呈先升高后降低的趋势,当葡萄糖与烟酰胺比例为2∶1时,NMN产量最高,为13.20 mg/L,同时OD600nm值达到2.1。这一配比实现了碳源在菌体生长和NMN合成途径之间的最优分配。分析原因可能是,葡萄糖供给不足时,菌体主要将碳源用于基础代谢和生长需求,导致NMN合成受限;但过量的葡萄糖也可能抑制菌株的生长,且烟酰胺底物相对不足时,也会限制NMN的合成效率,进而导致NMN产量降低[25]。因此,确定最佳投料比(葡萄糖∶烟酰胺)为2∶1。
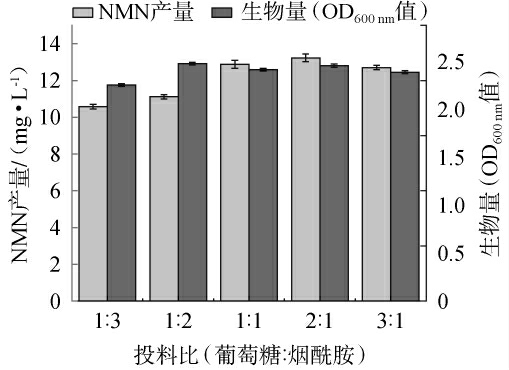
图9 投料比(葡萄糖∶烟酰胺)对突变菌株N3生长及烟酰胺单核苷酸产量的影响
Fig.9 Effect of feed ratio (glucose∶nicotinamide) on growth and nicotinamide mononucleotide yield of mutant strain N3
综上,确定突变菌株N3产NMN的最佳诱导表达条件为诱导时机(OD600nm值)=1.20、IPTG浓度0.50 mmol/L、诱导温度30 ℃、诱导时间12 h、投料比(葡萄糖∶烟酰胺)2∶1。在此条件下,NMN产量比优化前提高31.34%。
3 结论
本研究在大肠杆菌中成功表达Comamonadaceae细菌来源的NAMPT基因,其NMN产量为6.53 mg/L;在此基础上,通过重叠PCR和同源重组的方法将出发菌株第257位和259位的氨基酸残基分别定点突变为色氨酸、缬氨酸后获得单突变菌株N1、N2及双突变菌株N3,其NMN产量分别为6.88 mg/L、9.38 mg/L、10.05 mg/L,较出发菌株分别提高5.36%、43.64%和53.91%;NAMPT活力分别为42.08 U/mL、46.23 U/mL、50.30 U/mL,较出发菌株分别提高5.73%、14.19%、21.13%。突变菌株N3产NMN的最佳诱导条件为诱导时机(OD600 nm值)1.2、诱导剂浓度0.5 mmol/L、诱导时间12 h、培养温度30 ℃、投料比(葡萄糖∶烟酰胺)2∶1,在此条件下,NMN产量达到13.20 mg/L,较优化前提高31.34%。该研究结果为后续发酵生产NMN提供了优质底盘菌株。
[1]梁宁娟,杨同金,蒋小涵.烟酰胺单核苷酸的急性及亚急性经口毒性[J].中国工业医学杂志,2024,37(3):271-274.
[2]邓丽丽,王佳文,袁丁.竹节参总皂苷通过和炎症小体途径减轻衰老大鼠神经细胞凋亡的作用研究[J].中草药,2017,48(23):4941-4951.
[3]LIU Y, YASAWONG M, YU B.Metabolic engineering of Escherichia coli for biosynthesis of β-nicotinamide mononucleotide from nicotinamide[J].Microb Biotechnol,2021,14(6):2581-2591.
[4]SHOJI S,YAMAJI T,MAKINO H,et al.Metabolic design for selective production of nicotinamide mononucleotide from glucose and nicotinamide[J].Metab Eng,2021,65(5):167-177.
[5]廖一波.烟酰胺单核苷酸的生物酶法合成[D].广州:华南理工大学,2020.2020.003920.
[6]MAHARJAN A, SINGHVI M, KIM B S, et al.Biosynthesis of a therapeutically important nicotinamide mononucleotide through a phosphoribosyl pyrophosphate synthetase 1 and 2 engineered strain of Escherichia coli[J].ACS Synth Biol,2021,10(11):3055-3065.
[7]UNBIN W,RUI X,YUXIN F,et al.Rational design of a de novo enzyme cascade for scalable continuous production of antidepressant prodrugs[J].ACS Catal,2022,12(7):3767-3775.
[8]毛歆安,龚劲松,苏畅.烟酰胺核糖激酶在大肠杆菌中的高效异源表达、酶学特性分析和发酵工艺探究[J].食品与发酵工业,2025,51(6):50-57.
[9]LIU L, BAI L Q, LI Y, et al.Research progress on the application of β-nicotinamide mononucleotides in cosmetics[J].China Detergent Cosmetics,2023,8(2):73-80.
[10]DHATT S,NANDI M,CHAUDHURY P,et al.Substrate inhibition versus product feedback inhibition: In the perspective of single molecule enzyme kinetics[J].Int J Chem Kinet,2021,53(8):775-786.
[11]SAKSHI K,APOORVA P,DEEP KOUR H,et al.Molecular interaction study of L-ornithine with bovine serum albumin using spectroscopic and molecular docking methods[J].Sci Rep,2025,15(1):11997.
[12]ARNCE LR,BUBNELLJ E,AQUADRO C F,et al.Comparative analysis of drosophila bam and bgcn sequences and predicted protein structural evolution[J].J Mol Evol,2025,93(2):278-291.
[13]ALSAHAG M.Computational discovery of natural inhibitors targeting enterovirus D68 3C protease using molecular docking pharmacokinetics and dynamics simulations[J].Sci Rep,2025,15(1):11015.
[14]MASUMI SUGIYAMA,KENNETH S KOSIK,ELENI PANAGIOTOU,et al.Geometry based prediction of tau protein sites and motifs associated with misfolding and aggregation[J].Sci Rep,2025,15(1):10283.
[15]BENAZZOUZ TOUAMI A, IGHILAHRIZ K, MAKHLOUFI CHEBLI M,et al.Synthesis,biological evaluation,ADMET studies,and molecular docking of novel coumarin-isoxazole derivatives as dual inhibitors of Hsp90 protein and acetylcholinesterase enzyme[J].J Mol Struct,2025,133(3):141776.
[16]YAN J,CHENG W X,ZHANG P,et al.Conformational ensembles for protein structure prediction[J].Sci Rep,2025,15(1):8513-8513.
[17]HUA W,JIANG N,WU Y,et al.Synthesis of NMN by cascade catalysis of intracellular multiple enzymes[J].RSC Adv, 2023, 13(40): 28131-28138.
[18]MALHOTRA Y, JOHN J, YADAV D, et al.Advancements in protein structure prediction: A comparative overview of AlphaFold and its derivatives[J].Comput Biol Med,2025,27(8):1416-1430.
[19]孙晓瑄,张瑞婕,孙雯,等.重组微小囊担子菌氨肽酶DmpA高效催化生产L-肌肽[J/OL].食品工业科技,1-22[2025-08-28].https://doi.org/10.13386/j.issn1002-0306.2025010059.
[20]朱乐婷,宋文军,娄婷婷.青春双歧杆菌蔗糖磷酸化酶诱导表达条件的优化及其酶学性质[J].食品研究与开发,2024,45(23):194-202.
[21]MARINESCU G C,POPESCU R G,STOIAN G,et al.β-nicotinamide mononucleotide (NMN) production in Escherichia coli[J].Sci Rep,2018,8(1):12278.
[22]LU J, ZHAO Y, ZHANG J, et al.High-level expression of Aerococcus viridans pyruvate oxidase in Escherichia coli by optimization of vectors and induction conditions[J].Lett Appl Microbiol,2018,67(3):262-269.
[23]DELIVORIA D C, KONIA E, MATIS I, et al.Optimization of a highthroughput screen for monitoring disease-associated protein misfolding and aggregation in bacteria[J].ACS Synth Biol,2025,14(6):2283-2293.
[24]MORÃO L G,MANZINE L R,CLEMENTINO L O D,et al.A scalable screening of E.coli strains for recombinant protein expression[J].Plos One,2022,17(7):e0271403.
[25]HUANG Z,LI N,YU S,et al.Systematic engineering of Escherichia coli for efficient production of nicotinamide mononucleotide from nicotinamide[J].ACS Synth Biol,2022,11(9):2979-2988.