蛋白酶是一类广泛存在于自然界中的酶类,能通过水解作用降解氨基酸多肽链中的肽键,具有特异性[1]。作为三大工业酶之一,蛋白酶的需求逐年增长。研究表明,蛋白酶占全球酶类销售额的30%,被广泛应用于牛肉嫩化[2]、烘焙、食品保鲜[3]、酿造[4]、洗涤剂[5]、制革、制药[6]、化妆品以及医学检验[7]等领域。蛋白酶的主要来源包括植物(菠萝、木瓜)、动物(牛胃)和微生物(芽孢杆菌属[8]、假单胞菌属[9])。由于伦理和环境等因素影响,动植物源蛋白酶的大规模工业化生产受到较大程度限制。而微生物蛋白酶具有的经济优势和广泛生物多样性使其倍受青睐,所产蛋白酶适用于不同工业需求场景。
作为应用于功能性食品的主要益生菌之一,植物乳植杆菌(Lactiplantibacillus plantarum)可预防心血管疾病,维持肠道内菌群平衡[10]。植物乳植杆菌具有产蛋白酶的能力,可将蛋白质分解为功能性多肽和游离氨基酸[11],提高食物消化效率,促进风味形成,生成功能性成分进而增加发酵底物的附加值[12],具有很高的研究价值。KUERMAN M等[13]研究发现,植物乳植杆菌可增强酸诱导凝胶的质构特性。然而,植物乳植杆菌在产酶工业上的应用受到外在培养条件影响,需要在发酵工艺中优化产蛋白酶植物乳植杆菌的培养条件和培养基成分,提高蛋白酶产能。因此,本研究将一株分离自发酵泡菜的菌株作为目标菌株,微孔法初步鉴定其产酶能力后,通过单因素、响应面试验优化菌株G119产酶活力,以期为后续蛋白酶制剂的高效制备和工业化应用提供实验基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
植物乳植杆菌(Lactiplantibacillus plantarum)G119:分离自四川泡菜,保藏于西南民族大学食品微生物实验室。
1.1.2 试剂
干酪素、果糖、葡萄糖、可溶性淀粉、蔗糖、麦芽糖、胰蛋白胨、硫酸铵、豆粕、尿素、牛肉浸粉、明胶、酵母粉、三氯乙酸:上海麦克林生化科技股份有限公司;脱脂乳粉、福林酚、乳酸、乳酸钠、L-酪氨酸:上海源叶生物科技有限公司;NaCl、CaCl2、MgCl2、KNO3、CuSO4、ZnSO4:成都科隆化学品有限公司。以上试剂均为分析纯或生化试剂。
1.1.3 培养基
MRS肉汤培养基:蛋白胨10.0 g/L,牛肉浸粉8.0 g/L,酵母粉4.0 g/L,葡萄糖20.0 g/L,磷酸氢二钾2.0 g/L,柠檬酸氢二铵2.0 g/L,乙酸钠5.0 g/L,硫酸镁0.2 g/L,硫酸锰0.04 g/L,吐温80 1.0g/L,121 ℃高压蒸汽灭菌15 min。
牛奶培养基:12 g脱脂奶粉,5 g琼脂,1 000 mL超纯水,110 ℃高压蒸汽灭菌15 min。
1.2 仪器与设备
DHP-9162B电热恒温培养箱:上海一恒科学仪器有限公司;5810R冷冻离心机:艾本德(上海)国际贸易有限公司;SP-384全波长酶标仪:美谷分子仪器(上海)有限公司;UV-1900型紫外可见分光光度计:翱艺仪器(上海)有限公司;MLS-3030H高压蒸汽灭菌锅:上海拜格生物科技发展有限公司。
1.3 方法
1.3.1 菌株G119活化
将2%(V/V)的菌株G119甘油保藏菌液接种于MRS肉汤培养基中,于37 ℃、180 r/min条件下振荡培养24 h,连续培养3次,获得培养3代的种子液。
1.3.2 菌株产蛋白酶能力初步鉴定
将培养3代的菌株G119种子液接种至牛奶培养基,于37 ℃培养48 h,若培养基中出现水解圈,则说明该菌具有产蛋白酶能力,以水解圈直径/微孔直径(HE值)初步评估菌株产蛋白酶能力[14]。
1.3.3 菌株G119生长曲线绘制
参考WANG X Z等[15]的方法,在MRS肉汤培养基中接种2%(V/V)菌株G119的3代种子液,观察72 h内菌株的生长情况并绘制生长曲线。
1.3.4 蛋白酶活力测定
采用福林酚法,以酪蛋白为底物对蛋白酶活力进行测定[16],并以L-酪氨酸绘制标准曲线。
1.3.5 产酶培养基组成优化单因素试验
初始发酵条件:将菌株G119第3代种子菌液以2%(V/V)的接种量接入MRS肉汤培养基,于初始pH 6、37 ℃、180 r/min条件下振荡培养24 h,测得初始蛋白酶活力为45.84 U/mL。
采用单因素轮换法,在初始发酵条件的基础上,依次考察碳源种类及最佳碳源添加量、氮源种类及最佳氮源添加量、无机盐种类及最佳无机盐添加量对菌株G119产蛋白酶活性的影响。
碳源种类及添加量优化:参考张婷等[17]的方法,考察碳源种类(葡萄糖、果糖、可溶性淀粉、蔗糖、麦芽糖,20 g/L)对菌株G119产蛋白酶的影响。确定最适碳源为果糖后,考察果糖添加量(10 g/L、15 g/L、20 g/L、25 g/L、30 g/L)对菌株G119产蛋白酶的影响。
氮源种类及添加量优化:参考陈杰等[18]的方法,考察氮源种类(牛肉浸粉、硫酸铵、豆粕、尿素、明胶、酵母粉,10 g/L)对菌株G119产蛋白酶的影响。确定最适氮源为酵母粉后,考察酵母粉添加量(5 g/L、10 g/L、15 g/L、20 g/L、25 g/L)对菌株G119产蛋白酶的影响。
无机盐种类及添加量优化:参考李娜等[19]的方法,考察无机盐种类(NaC2H3O2、NaCl、CaCl2、MgCl2、KNO3、ZnSO4、CuSO4,5 g/L)对菌株G119产蛋白酶的影响。确定最适无机盐为NaCl后,考察NaCl添加量(2.5 g/L、5 g/L、7.5 g/L、10 g/L、12.5 g/L)对菌株G119产蛋白酶的影响。
1.3.6 产酶条件优化单因素试验
在MRS肉汤培养基中接种2%(V/V)菌株G119的第3代种子液,于37 ℃、180 r/min振荡培养24 h。在此基础上,控制单一变量,分别考察培养时间(12 h、18 h、24 h、30 h、36 h)、培养温度(25 ℃、30 ℃、35 ℃、37 ℃、40 ℃)、培养基初始pH(4、5、6、7、8)和菌液接种量(1.0%、1.5%、2.0%、2.5%、3.0%)对菌株G119产蛋白酶的影响。
1.3.7 产酶条件优化响应面试验
在单因素试验结果的基础上,选取对蛋白酶活力影响最显著的3个因素培养时间(A)、培养温度(B)、发酵液初始pH(C)为自变量,以蛋白酶活力(Y)为响应值,采用Design Expert 13.0软件设计3因素3水平的Box-Behnken(BB)试验。
1.3.8 数据处理
使用IBM SPSS Statistics 27.0、Origin 2022、Design Expert 13.0等软件进行试验数据的处理分析和绘图。所有试验均重复3次。
2 结果与分析
2.1 菌株产酶能力鉴定
以微孔扩散法对菌株G119产蛋白酶能力进行初步判断,结果见图1。由图1可知,菌株G119接种于牛奶培养基并在37 ℃培养48 h后,出现明显的水解圈,HE值为3.93。由此可知,菌株G119具有良好的产蛋白酶能力。

图1 菌株G119在牛奶培养基上所产的水解圈
Fig.1 Hydrolysis ring produced by strain G119 on milk medium
2.2 菌株G119的生长曲线
菌株G119在72 h内的生长曲线见图2。由图2可知,培养0~10 h时菌株生长速度缓慢,为细菌生长的延滞期;10 h后菌株进入对数生长期,并在20 h左右达到生长的稳定期,菌株生长趋势逐渐平缓;当培养时间延至36 h,OD600nm值达到最大为2.37;此后,可能受到营养物质枯竭或其他环境因素影响,菌株G119的生长活力开始下降。
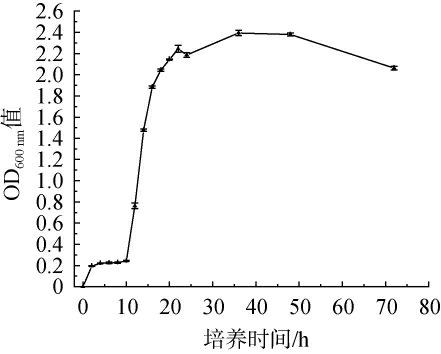
图2 菌株G119生长曲线
Fig.2 Growth curve of strain G119
2.3 菌株G119产蛋白酶培养基优化单因素试验
2.3.1 不同碳源种类及果糖添加量对菌株G119产蛋白酶活力的影响
不同碳源种类对菌株G119产蛋白酶活力的影响见图3A。由图3A可知,以果糖为培养基碳源时,菌株G119产蛋白酶活最高,因此选择果糖作为菌株G119产蛋白酶培养基的最佳碳源。
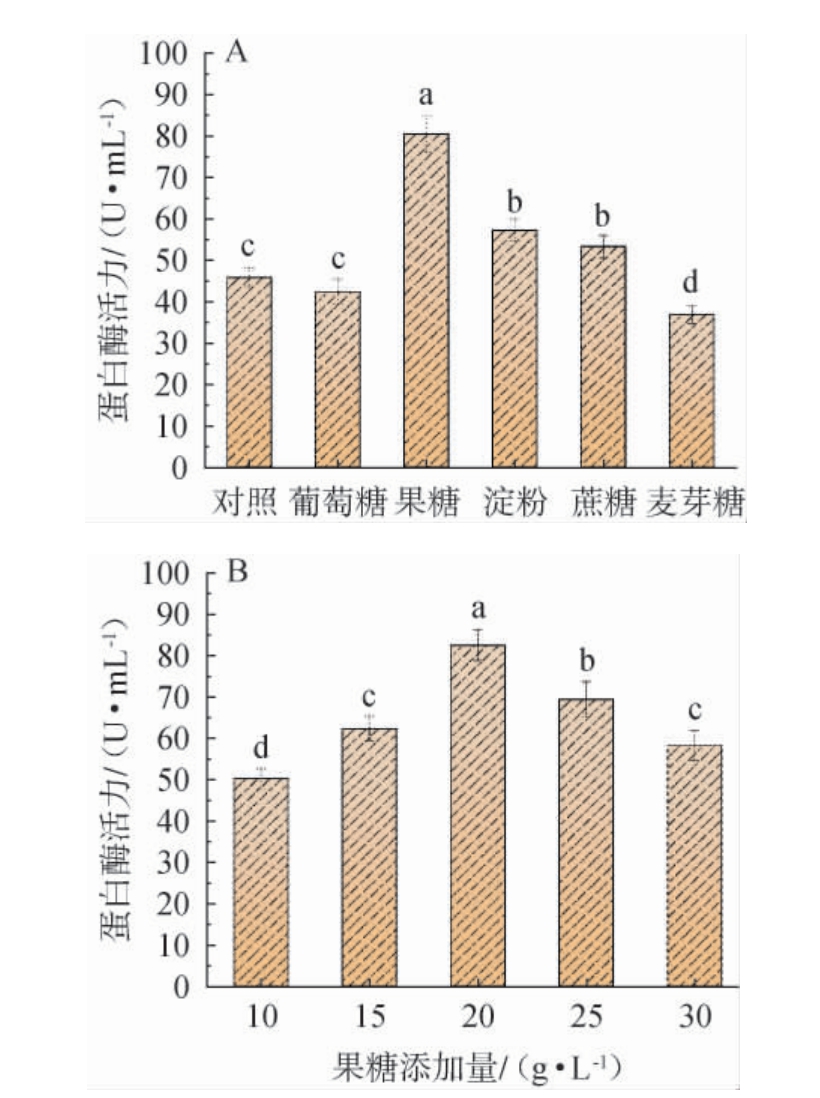
图3 不同碳源种类(A)及果糖添加量(B)对菌株G119产蛋白酶活力的影响
Fig.3 Effect of different carbon sources types (A) and fructose addition (B) on protease activity produced by strain G119
不同小写字母表示差异显著(P<0.05)。下同。
不同果糖添加量对菌株G119产蛋白酶活力的影响见图3B。由图3B可知,随着果糖添加量的升高,菌株G119产蛋白酶活力呈先升高后降低的趋势;当果糖添加量为20 g/L时,菌株所产蛋白酶活力最高,为82.47 U/mL,与对照组相比,酶活力显著提升了79.91%(P<0.05)。碳源为微生物提供生长繁殖所需要的能量,赵华等[22]的研究表明,随着碳源含量的升高,蛋白酶活性呈现先升高后下降的趋势,与本研究结果类似,这可能是因为氧含量降低、代谢物积累等情况所造成的。因此,选择果糖添加量为20 g/L。
2.3.2 不同氮源种类及酵母粉添加量对菌株G119产蛋白酶活力的影响
不同氮源种类对菌株G119产蛋白酶活力的影响见图4A。由图4A可知,以酵母粉为培养基氮源时,菌株G119产蛋白酶活最高,因此选择酵母粉作为菌株G119产蛋白酶培养基的最佳氮源。
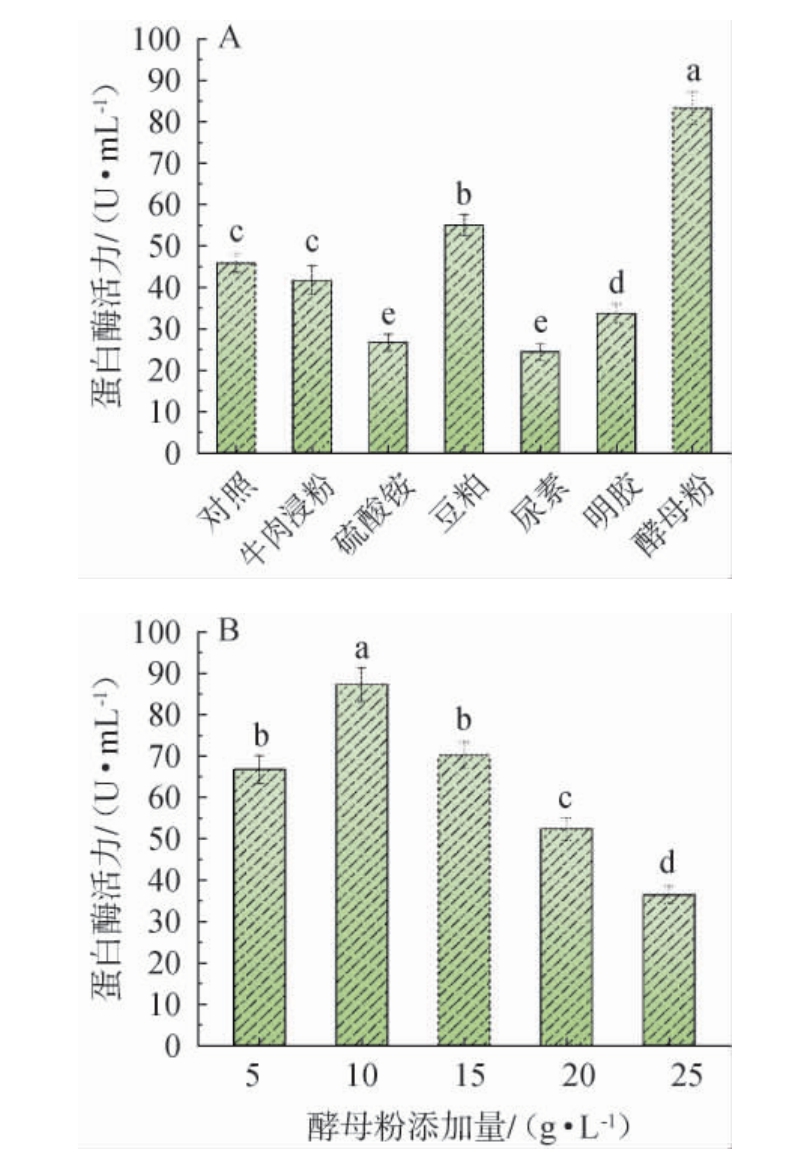
图4 不同氮源种类(A)及酵母粉添加量(B)对菌株G119产蛋白酶活力的影响
Fig.4 Effect of different nitrogen sources types (A) and yeast powder addition (B) on protease activity produced by strain G119
不同酵母粉添加量对菌株G119产蛋白酶活力的影响见图4B。由图4B可知,随着酵母粉添加量的升高,蛋白酶活力呈先升高后降低的趋势;当酵母粉添加量为10 g/L时,菌株G119所产蛋白酶活力最高,为87.24 U/mL,与对照组相比,酶活力显著提升了90.31%(P<0.05)。在微生物细胞合成过程中,氮源在微生物的生长繁殖中发挥着重要作用,卢丽媛等[23]的研究表明,随着培养基中氮源含量的上升,可能发生细菌代谢失衡,致使菌株产酶活力下降。因此,选择酵母粉添加量为10 g/L。
2.3.3 不同无机盐种类及NaCl添加量对菌株G119产蛋白酶活力的影响
不同无机盐种类对菌株G119产蛋白酶活力的影响见图5A。由图5A可知,与对照相比,6种无机盐中,NaCl对菌株G119所产蛋白酶的活力有提升,因此选择NaCl作为菌株G119产蛋白酶培养基的最佳无机盐。
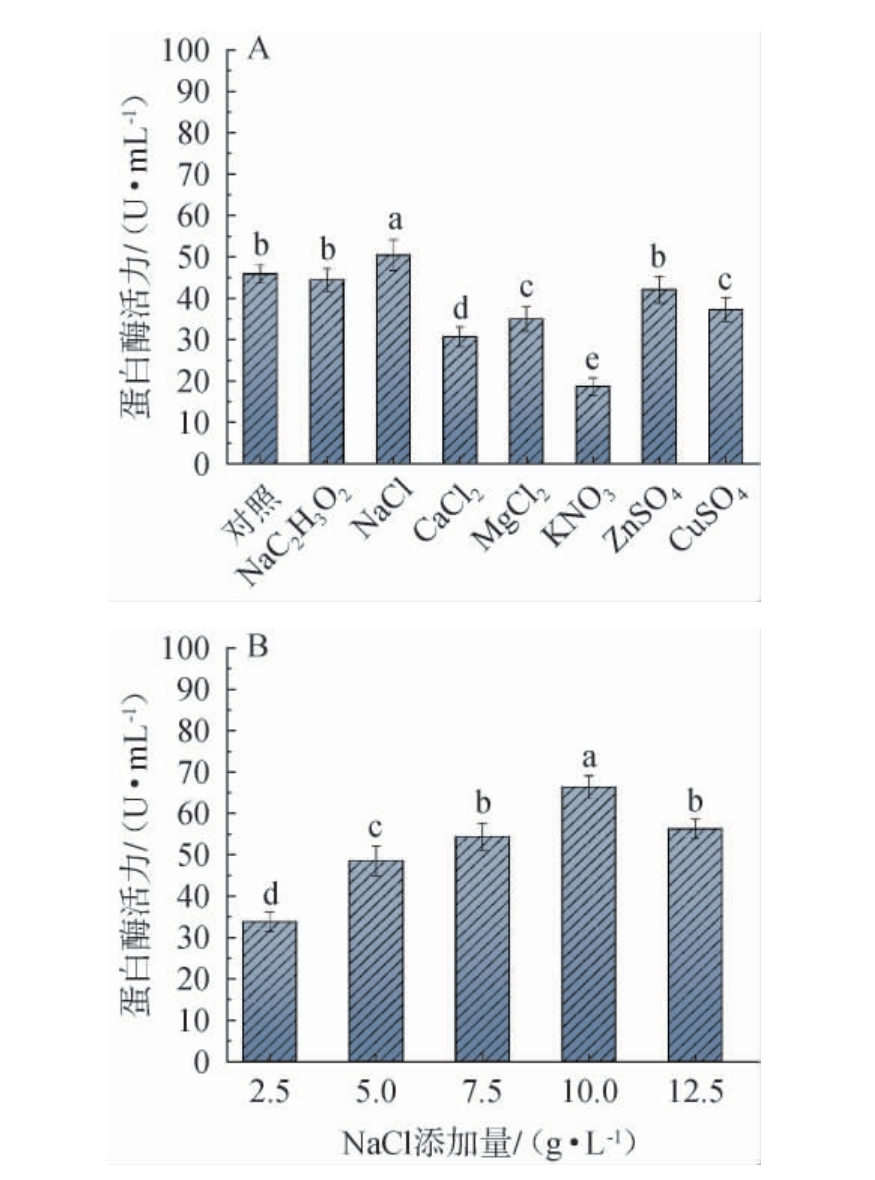
图5 不同无机盐种类(A)及NaCl添加量(B)对菌株G119产蛋白酶活力的影响
Fig.5 Effect of different inorganic salts types (A) and NaCl addition(B) on protease activity produced by strain G119
不同NaCl添加量对菌株G119所产蛋白酶活力的影响见图5B。由图5B可知,随着NaCl添加量的升高,蛋白酶活力呈先升高后降低的趋势;当NaCl添加量为10 g/L时,菌株G119所产蛋白酶活力最高,为66.34 U/mL,与对照组相比,产酶能力提升了44.72%(P<0.05)。NaCl作为无机盐可以提供与酶活力相关的Na+,促进菌体的代谢产酶活性[24]。因此,选择NaCl添加量为10 g/L。
2.4 菌株G119产蛋白酶培养条件优化单因素试验
在初始培养条件下,培养时间、培养温度、发酵液初始pH和种子液接种量对菌株G119产蛋白酶的影响见图6。
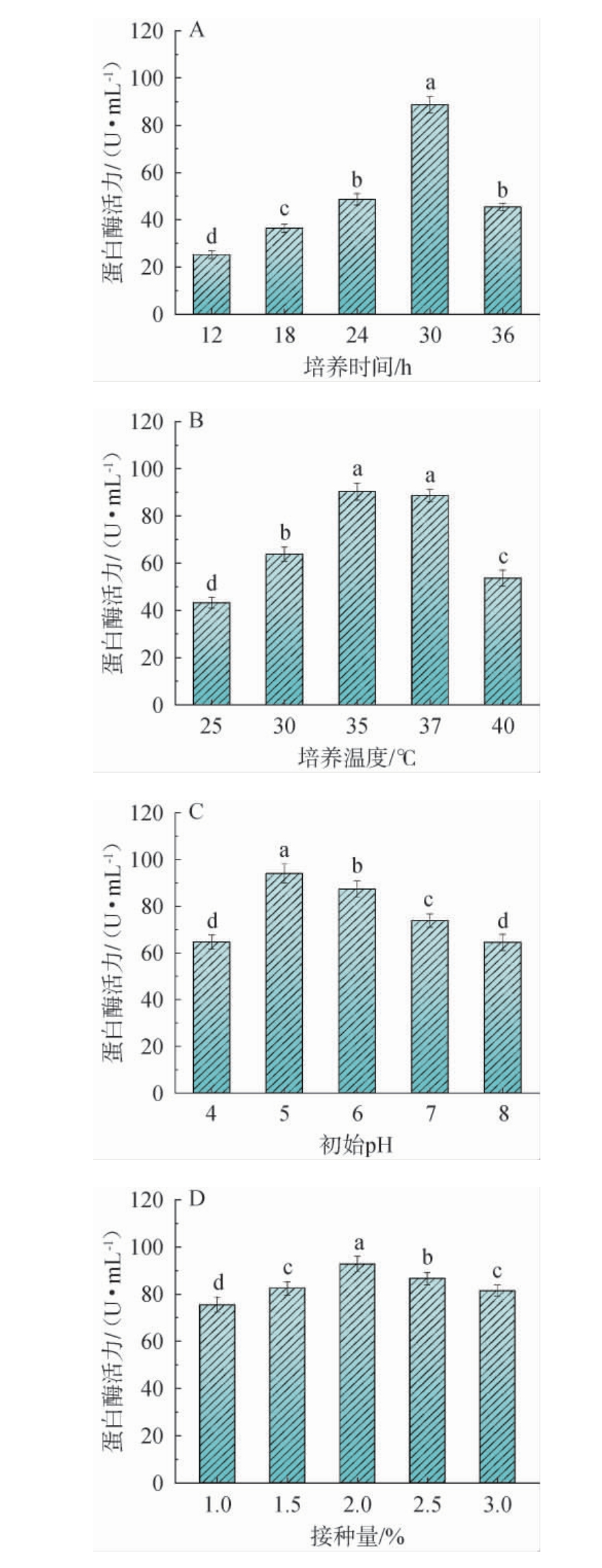
图6 培养时间(A)、培养温度(B)、初始pH(C)和接种量(D)对菌株G119产蛋白酶活性的影响
Fig.6 Effects of culture time (A), temperature (B), initial pH (C), and inoculum (D) on protease activity produced by strain G119
培养时间、培养温度、初始pH、接种量对菌株G119产蛋白酶活力的影响见图6。由图6A可知,随着培养时间的延长,蛋白酶活力呈先升高后降低的趋势;发酵30 h时蛋白酶活力达到最大,为88.69 U/mL;当培养时间超过30 h后,蛋白酶活力开始下降。可能是由于在培养后期由于营养物质逐渐消耗和减少,菌株生长和代谢受到抑制,产酶量降低。这与李正风等[25]的研究结果一致。因此,选择菌株的培养时间控制为30 h。由图6B可知,随着培养温度的升高,蛋白酶活力呈先升高后降低的趋势;当培养温度为35 ℃时,蛋白酶活力达到最大,为90.36 U/mL;当培养温度高于35 ℃后,蛋白酶活力开始下降。彭洁英等[26]的研究认为,培养温度是影响微生物代谢的关键因素之一,过高或过低的培养温度均会对菌株生长产生不利影响,进而影响蛋白酶的产生和释放效率,与本研究结果类似。因此,选择菌株的培养温度控制为35 ℃。由图6C可知,随着培养基初始pH的升高,蛋白酶活力呈先升高后降低的趋势;当培养基初始pH为5时,蛋白酶活力达到最大,为94.06 U/mL;随着培养基初始pH进一步升高,蛋白酶活力开始下降。因此,选择培养基初始pH为5。由图6D可知,随着接种量的升高,蛋白酶活力呈先升高后降低的趋势;当接种量为2%时,蛋白酶活力达到最大,为92.77 U/mL;随着接种量的进一步升高,蛋白酶活力开始下降。因此,选择接种量为2%。
2.5 产酶培养条件优化响应面试验
2.5.1 响应面试验设计与结果
在单因素试验结果的基础上,确定菌液接种量为2%,选择对蛋白酶活力影响最显著的3个因素培养时间(A)、培养温度(B)、发酵液初始pH(C)为自变量,以蛋白酶活力(Y)为响应值,采用Design Expert 13软件设计4因素3水平的Box-Behnken(BB)试验。试验设计及结果见表1,方差分析见表2。
表1 菌株G119产蛋白酶活力培养条件优化Box-Behnken试验设计及结果
Table 1 Design and results of Box-Behnken tests for culture conditions optimization of protease activity produced by strain G119
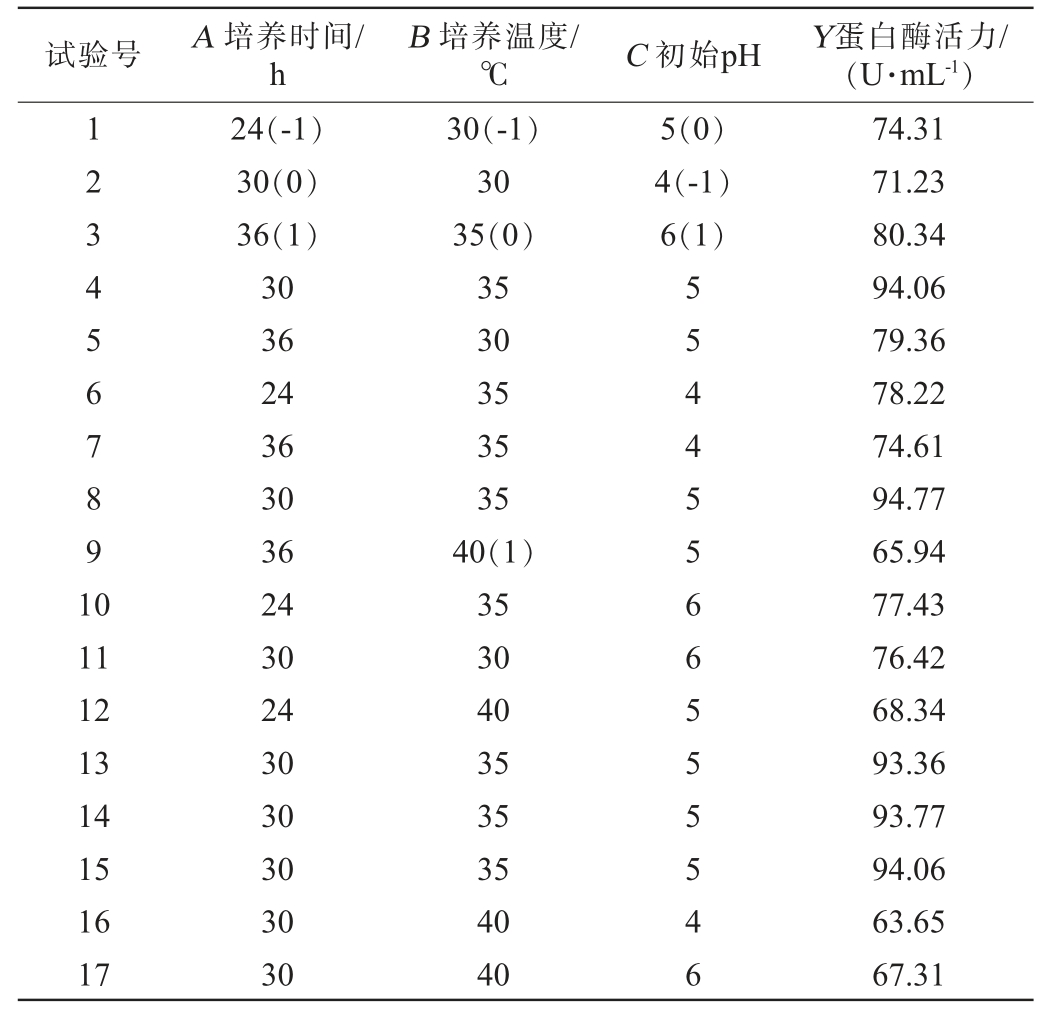
试验号 A 培养时间/h B 培养温度/℃ C 初始pH Y蛋白酶活力/(U·mL-1)1234567891 0 5(0)4(-1)6(1)11 12 13 14 15 16 17 24(-1)30(0)36(1)30 36 24 36 30 36 24 30 24 30 30 30 30 30 30(-1)30 35(0)35 30 35 35 35 40(1)35 30 40 35 35 35 40 40 55445566555546 74.31 71.23 80.34 94.06 79.36 78.22 74.61 94.77 65.94 77.43 76.42 68.34 93.36 93.77 94.06 63.65 67.31
表2 回归模型方差分析
Table 2 Variance analysis of regression model
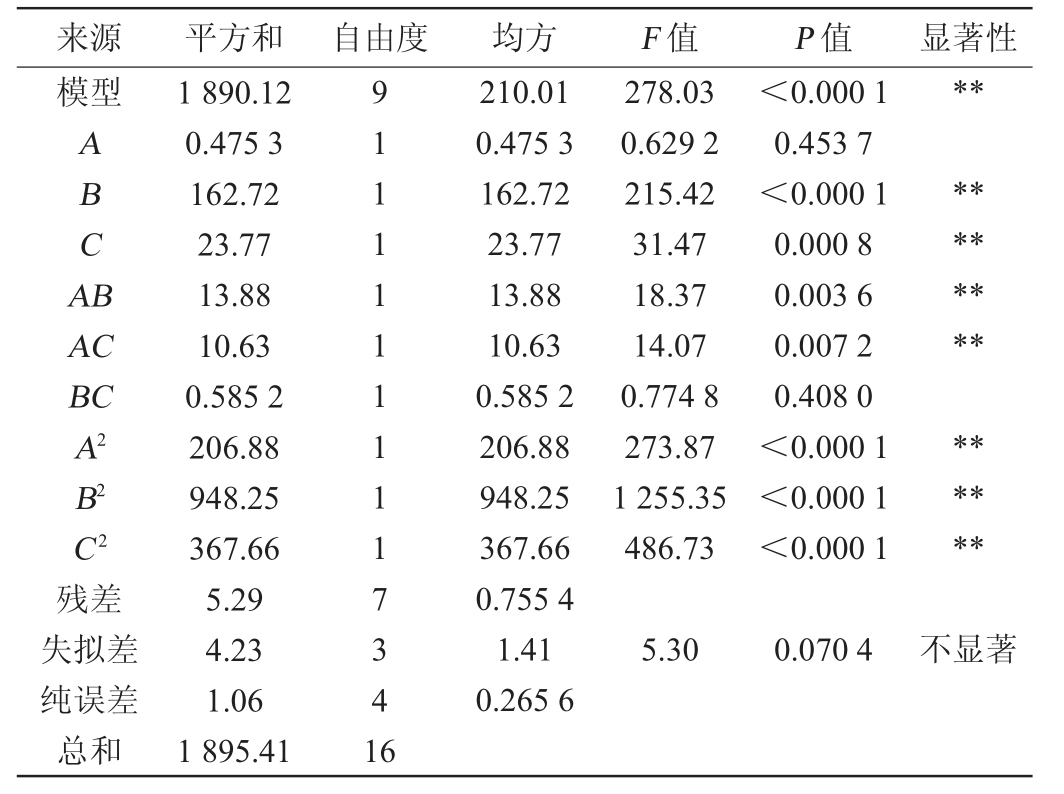
来源 平方和 自由度 均方 F 值 P 值 显著性模型**ABCA B AC BC A2 B2 C2 278.03 0.629 2 215.42 31.47 18.37 14.07 0.774 8 273.87 1 255.35 486.73<0.000 1 0.453 7<0.000 1 0.000 8 0.003 6 0.007 2 0.408 0<0.000 1<0.000 1<0.000 1**************残差失拟差纯误差总和1 890.12 0.475 3 162.72 23.77 13.88 10.63 0.585 2 206.88 948.25 367.66 5.29 4.23 1.06 1 895.41 91111111117341 6 210.01 0.475 3 162.72 23.77 13.88 10.63 0.585 2 206.88 948.25 367.66 0.755 4 1.41 0.265 6 5.30 0.070 4不显著
采用Design-Expert 13对表1数据进行多元二次回归拟合,得到蛋白酶活力的二次多项回归方程:Y=94+0.243 8A-4.51B+1.72C-1.86AB+1.63AC-0.3825BC-7.01A2-15.01B2-9.34C2。
由表2可知,回归模型极显著(P<0.01),失拟项不显著(P>0.05),说明该模型具有可重复性、可靠。决定系数R2=0.997 2,调整决定系数R2adj=0.993 6,说明模型拟合度较好。由P值可知,一次项B、C,交互项AB、AC,二次项A2、B2、C2对蛋白酶活力影响极显著(P<0.01),其他项不显著(P>0.05);由F值可知,各因素对蛋白酶活力的影响由大到小依次为培养温度(B)>初始pH(C)>培养时间(A)。各因素交互作用对蛋白酶活力影响的响应面及等高线见图7。
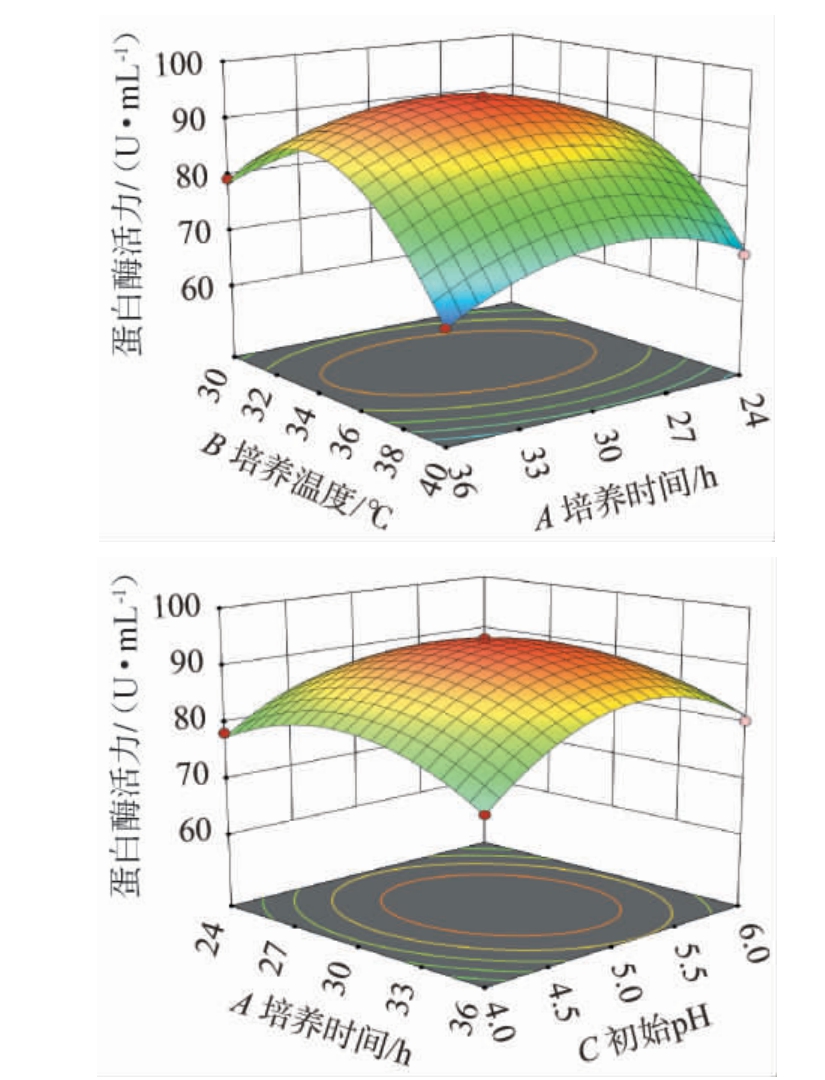
图7 各因素间交互作用对菌株G119产蛋白酶活力影响的响应面及等高线
Fig.7 Response surface plots and contour lines of effect of interaction between various factors on the protease activity produced by strain G119
响应面越陡峭、等高线越椭圆说明各因素间交互作用影响越大,相反交互作用影响越小。由图7可知,AB、AC交互作用对蛋白酶活力影响的响应面均呈凸面,坡度陡峭,等高线呈椭圆形,说明对蛋白酶活力影响较大,这与方差分析结果一致。
2.5.2 验证试验
采用Design-Expert 13软件对多元二次回归方程进行最优求解,得到菌株G119产蛋白酶活力最佳条件为培养时间30.30 h,培养温度34.23 ℃,初始pH 5.1,在此条件下蛋白酶活力预测值为94.45 U/mL;为方便实际操作,将最佳培养条件调整为培养时间30 h,培养温度34 ℃,初始pH 5,在此优化条件下进行3次验证试验,测得菌株G119产蛋白酶活力平均值为93.66 U/mL,较预测值偏差0.84%,表明该模型对菌株G119产酸性蛋白酶活力的预测准确度较高。
3 结论
本研究对分离自四川发酵泡菜的植物乳植杆菌G119产酶条件进行优化,得到产酶培养基组成为酵母粉10.0 g/L,果糖20.0 g/L,NaCl 10.0 g/L;最优产酶条件为培养时间30 h,培养温度34 ℃,初始pH 5,在此条件下,菌株G119产蛋白酶活力达到93.66 U/mL,比初始蛋白酶活力(45.84 U/mL)提高了1.04倍。有效提升了菌株的蛋白酶产量,为后续菌株蛋白酶的应用与工业化生产奠定了实验基础。
[1]KUERMAN M,SHI R Y,ZHANG Y S,et al.Lactiplantibacillus plantarum strains with proteolytic abilities showed diverse effects on casein gel formation during fermentation[J].Food Hydrocoll,2024,148:109406.
[2]董世容,刘雨蝶,杨希,等.超声波协同半胱氨酸促进木瓜蛋白酶对冷鲜牛肉嫩化作用的研究[J].食品科技,2023,48(7):85-91.
[3]DENG J J,HUANG W Q,LI Z W,et al.Biocontrol activity of recombinant aspartic protease from Trichoderma harzianum against pathogenic fungi[J].Enzyme Microb Technol,2018,112:35-42.
[4]张欢,王端好,陆光瑞,等.酸性蛋白酶对发酵黄豆酱品质的影响[J].中国酿造,2021,40(8):150-156.
[5]NEOG P R, SAINI S, KONWAR B K.A sustainable alternative to hazardous chemicals in detergent industry[J].Protein Expr Purif,2024,219:106479.
[6]MENG S H,GAO Y,QIANG G W,et al.Rational design,synthesis and biological evaluation of novel HIV-1 protease inhibitors containing 2-phenylacetamide derivatives as P2 ligands with potent activity against DRVResistant HIV-1 variants[J].Bioorg Med Chem Lett,2024,101:129651.
[7]KONG X R, WANG B M, CHEN X Y, et al.Hinokiflavone attenuates the virulence of methicillin-resistant Staphylococcus aureus by targeting caseinolytic protease P[J].Antimicrob Agents Chemother,2022,66(8):e0024022.
[8]JEON S H, SEONG H J, KIM H, et al.Improvement of branched-chain amino acid production by isolated high-producing protease from Bacillus amyloliquefaciens NY130 on isolated soy/whey proteins and their muscle cell protection[J].Food Chem,2024,450:139327.
[9]DU B Y,LU M,LIU H M,et al.Pseudomonas isolates from raw milk with high level proteolytic activity display reduced carbon substrate utilization and higher levels of antibiotic resistance[J].LWT-Food Sci Technol,2023,181:114766.
[10]尹红梅,夏圣坤,钟亚东,等.植物乳杆菌NCU137发酵薏苡仁调节免疫抑制小鼠免疫和肠道黏膜屏障功能[J].食品科学,2024,45(11):136-143.
[11]汪晓雅,陈芳,刘思慧,等.不同胁迫体系对植物乳杆菌zwq9生物膜形成及其产蛋白酶活力的影响[J].食品研究与开发,2023,44(5):194-201.
[12]李丹阳,李宇辉,高云云,等.新疆哈萨克族风干肉中产蛋白酶乳酸菌的筛选及酶学特性研究[J].食品与发酵工业,2020,46(9):57-63.
[13]KUERMAN M, LIU Z R, LIU Y J, et al. Lactiplantibacillus plantarum enhances the texture of fermented milk by facilitating protein gelatinization through the action of a novel coagulation-promoting protease[J].Food Hydrocoll,2024,154:110044.
[14]梁安健,石沁兰,王金丽,等.产蛋白酶波茨坦短芽孢杆菌的鉴定及产酶条件优化[J].现代食品科技,2024,40(5):73-83.
[15]WANG X Z,WANG Z G,FENG T.Screening of yeast in various vineyard soil and study on its flavor compounds from brewing grape wine[J].Molecules,2022,27(2):512.
[16]周欢,宋艳梅,范光彩,等.福林酚法高通量测定牛奶中蛋白酶活力的优化[J].中国乳业,2024(7):92-97.
[17]张婷,刘喜莹,陈涛.泡盛曲霉固态发酵产阿魏酸酯酶条件优化[J].中国酿造,2024,43(2):140-145.
[18]陈杰,李豆南,刘茂强,等.产耐高温果胶酶菌株筛选鉴定、产酶条件优化及酶学性质研究[J].中国酿造,2023,42(5):176-183.
[19]李娜,附俊杰,刘军,等.一株产中性蛋白酶菌株的筛选及其发酵产酶条件优化[J].食品工业科技,2023,44(1):189-199.
[20]司阔林,徐捐捐,岳田利,等.布氏乳杆菌产γ-氨基丁酸发酵条件的优化[J].食品科学,2020,41(2):87-93.
[21]曹辰辰,冯美琴,孙健,等.响应面法优化益生发酵剂接种发酵香肠工艺[J].食品科学,2019,40(6):69-76.
[22]赵华,任青霞,张敏,等.酒曲中高产蛋白酶菌株的筛选及其发酵培养基优化[J].中国酿造,2023,42(5):157-164.
[23]卢丽媛,周丽艳,宋天悦,等.1株产蛋白酶菌株的分离鉴定及其产酶条件的优化[J].现代畜牧兽医,2022(1):1-7.
[24]唐洁,杨强,刘源才,等.高糖化力米根霉G1培养条件优化[J].中国酿造,2022,41(7):173-178.
[25]李正风,张鹏,王萝萍,等.摩加夫芽孢杆菌产酶条件优化及对烟叶品质的影响[J].中国烟草科学,2023,44(3):69-76.
[26]彭洁英,黄琳茹,方坚濠,等.产果胶酶菌株的分离鉴定及其产酶条件优化[J].中国酿造,2023,42(10):86-93.