大曲是我国常用的传统固态发酵剂,被广泛应用于白酒、食醋等酿造食品。按制曲过程中的最高曲块温度,大曲可分为低温大曲、中温大曲及髙温大曲三大类,其中低温大曲最高曲块温度一般控制在40~50 ℃;中温大曲的制曲最高曲块温度范围控制在50~60 ℃;高温大曲最高曲块温度范围控制在60~70 ℃[1]。山西老陈醋传统酿造工艺的一大特点是以曲代粮,用曲量大(60%左右),所用大曲为低温大曲,其最高曲块温度为46~48 ℃,主要以大麦和豌豆作为主要原料,经粉碎、加水调制压制而成的曲块,经入房排列、上霉期、晾霉期、潮火期、大火期、后火期、养曲期等几个阶段在开放的自然环境下制备而成[2]。大曲在山西老陈醋酿造中起到重要的物系、菌系和酶系角色,对最终食醋产品的营养、风味品质和酿醋效率、出品率和品质稳定性具有重要的影响作用。
目前,相关研究集中在低温大曲、中高温大曲和高温大曲的微生物、酶活和风味方面[3-5]。汤涵岚等[6]通过在实验室模拟食醋大曲固态发酵过程发现,将最高曲块温度提高至60 ℃可提高纤维素分解功能,优化大曲的代谢活性和产物形成。低温大曲存在酶活性低、酶谱丰富度差、发酵力弱、风味单薄等问题,对适合食醋酿造专用大曲的开发具有重要意义。小麦作为中高温大曲和高温大曲制备的主要原料,其高粘度和营养价值为微生物的生长及繁殖提供了优越条件,有助于大曲曲块温度的提升。适当曲块温度的升高不仅加速了酶活表达和风味物质合成,还通过筛选耐热功能菌群增强大曲的稳定性与功能性,最终在风味复杂度、发酵效率及产品一致性方面显著提升大曲品质[7-8]。
本研究在传统山西老陈醋大曲制曲工艺基础上,采用添加小麦的方式制备山西老陈醋大曲,探讨小麦添加对大曲曲房及曲块温度的提温效果,分析大曲制备过程中优势微生物菌群数量、酶活、理化指标和挥发性风味物质变化,以期为老陈醋大曲制备工艺参数优化提供数据支撑,为功能性强化大曲的开发奠定理论基础。
1 材料与方法
1.1 材料与试剂
1.1.1 原料
大麦(大麦3018)(淀粉:64.32g/100g,蛋白质:8.39g/100g,粗纤维:7.13%)、小麦(川麦93)(淀粉:61.73 g/100 g,蛋白质:11.81 g/100 g,粗纤维:7.13%):山西晋沃农业科技有限公司。
1.1.2 试剂
硫酸铜、亚铁氢化钾、酒石酸钾钠、无水乙酸钠、磷酸二氢钾(均为分析纯):天津市恒兴化学试剂有限公司;琼脂(生化试剂):北京奥博星生物技术有限公司;福林试剂(分析纯):北京索莱宝科技有限公司;3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)(分析纯):上海阿拉丁生化科技股份有限公司;可溶性淀粉(生化试剂):生工生物工程(上海)股份有限公司;干酪素、酪氨酸(均为生化试剂):上海河南万佳分析仪器有限公司;2-辛醇标准品(纯度>99%):西格玛奥德里奇(上海)贸易有限公司。
1.1.3 培养基
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基、MRS培养基、孟加拉红培养基、平板计数琼脂(plate count agar,PCA)培养基:北京奥博星生物技术有限责任公司。
1.2 仪器与设备
PB-21酸度计:申贝科学仪器(苏州)有限公司;DSX-30L高压蒸汽灭菌锅:上海申安医疗器械有限公司;HPX-150恒温培养箱:上海跃进医疗器械有限公司;DHG-9240A台式恒温鼓风干燥箱:上海一恒科学仪器有限公司;Trace 1300型气相色谱(gas chromatography,GC)仪、ISQ型质谱(mass spectrometry,MS)仪:美国Thermo Fisher公司。
1.3 方法
1.3.1 山西老陈醋大曲的制备工艺流程及操作要点
大麦、豌豆→粉碎、搅拌→加水→压曲→卧曲→上霉→晾霉→潮火→大火→后火→出房→贮存
操作要点:将大麦和豌豆按照质量比为7∶3粉碎混匀,使用分级筛过筛,粗面30%~40%,细面60%~70%,加入原料总质量的37%~50%的水混匀,将混匀的材料放进制曲机压制成砖形(28 cm×17 cm×6 cm),水分含量在36%左右。将压好的曲块呈三层排列于铺有苇杆并有洒谷糠的曲房,四周用苇席遮盖,即进入卧曲阶段,接下来进入上霉期(SM)(0~2 d)、晾霉期(LM)(2~3 d)、潮火期(CH)(3~9 d)、大火期(DH)(9~15 d)、后火期(HH)(15~21 d)5个阶段制得出房曲,总共为21 d,期间通过翻曲、调整曲快排列方式/间距、开关窗等调节曲房温湿度,出房曲再经3个月的成熟、干燥阶段,最终形成曲香纯正、曲表菌丝分布均匀、酶系丰富的优质成品大曲。
对照组:采用上述老陈醋大曲制备工艺进行制备。
实验组:添加15%的小麦代替大麦,即大麦∶小麦∶豌豆质量比为5.5∶1.5∶3.0,其余工艺操作同对照组。
1.3.2 分析检测
(1)微生物菌群测定
细菌总数、真菌总数、霉菌、酵母菌、乳酸菌及芽孢杆菌数的测定:参考丁伟等[9]的方法。
(2)基础理化指标和酶活的测定
液化力、糖化力、发酵力和酯化力、水分、总酸、淀粉、氨基酸态氮的测定:参照QB/T 4257—2011《酿酒大曲通用分析方法》[10];蛋白酶活的测定:分光光光度法[11];纤维素酶活力测定:DNS比色法[12];还原糖含量测定:DNS比色法[13]。
(3)挥发性风味成分的测定
采用气质联用技术测定山西老陈醋大曲制备过程中大火结束、后火结束以及成曲3个关键时间点样品的挥发性风味成分[14]。
挥发性香气成分萃取:将萃取头在进样口于270 ℃老化至无杂峰,在待测样品中加入10 μL 2-辛醇作为内标物(质量浓度8.22 mg/L),于45 ℃孵化炉中平衡30 min,顶空吸附30 min,将萃取插入进样口,270 ℃解吸5 min。
GC条件:载气为高纯氦气(He),流量1 mL/min,不分流。升温程序为起始温度40 ℃保持3 min;以4 ℃的速度升至160 ℃,保持1 min;再以10 ℃/min的速度升至270 ℃,保持5 min。
MS条件:电子电离(electronic ionization,EI)源,接口温度280 ℃,离子源温度280 ℃,电子能量70 eV,质量扫描范围41~500 amu。
定性定量分析:与美国国家标准与技术研究院(national institute of standards and technology,NIST)谱库比对,根据保留时间定性,采用内标法定量。
1.3.3 数据处理与统计分析
所有样品均重复测定3次,数据以“平均值±标准差”表示。使用SPSS26.0软件对数据进行单因素方差分析,采用Excel 2023和Origin 2018绘图。
2 结果与分析
2.1 山西老陈醋大曲制备过程中温度的变化
大曲制备操作工艺要点强调“前缓、中挺、后缓落”的原则[15],山西老陈醋大曲制备过程中曲房、曲块温度的变化见图1。
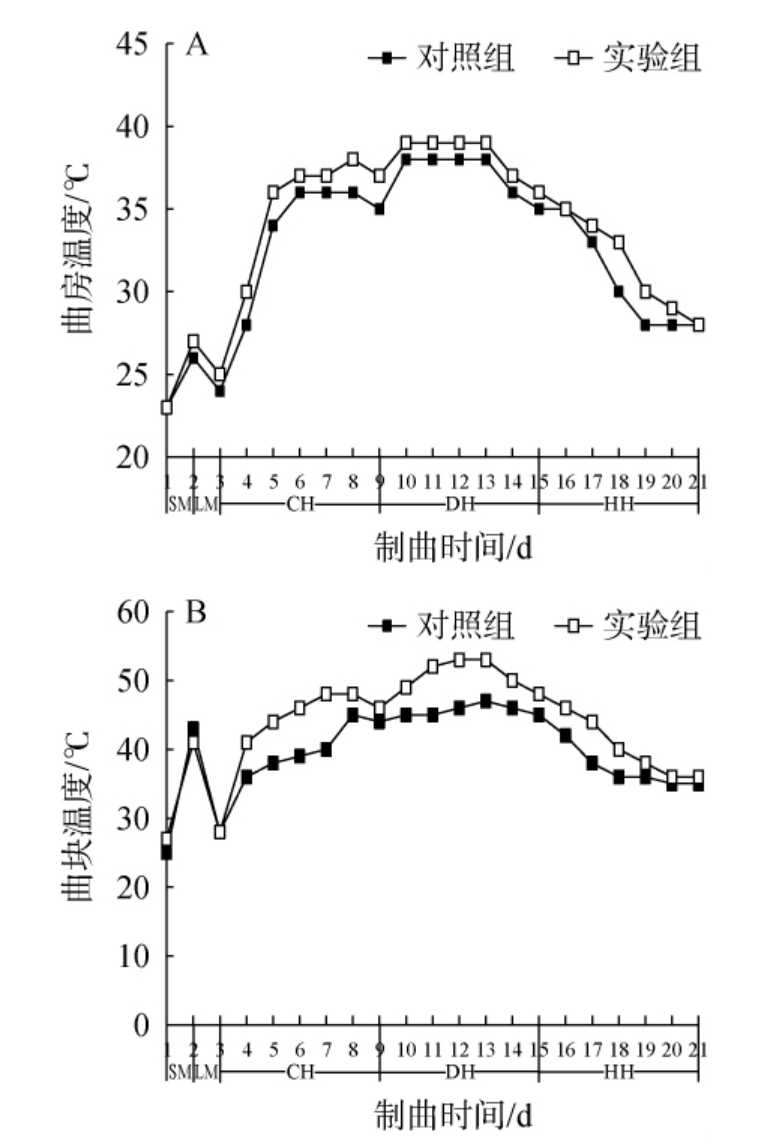
图1 山西老陈醋大曲制备过程中曲房温度(A)和曲块温度(B)的变化
Fig.1 Change of Daqu room temperature (A) and Daqu blocks temperature (B) during the preparation process of Shanxi aged vinegar Daqu
由图1可知,2种老陈醋大曲在制备过程中的曲房、曲块温度变化趋势一致。上霉期,对照组、实验组老陈醋大曲曲房温度分别从23 ℃上升至2 d的26 ℃、27 ℃,曲块温度分别从25 ℃、27 ℃上升至43 ℃、41 ℃。此过程伴随着旺盛的微生物新陈代谢活动,包括分解有机物、合成新的细胞物质等,释放大量生物热[16]。进入晾霉期,对照组和实验组老陈醋大曲的曲房温度分别降至24 ℃、25 ℃,曲块温度均下降至28 ℃。晾霉期揭席,散发温度和潮气,曲坯培养由保温转为排潮,在保持一定曲块温度的基础上缓慢排潮。当曲醅表面发干、坚硬就可进入潮火期,潮火期微生物生长非常活跃,霉菌和酵母菌的生长非常活跃,从曲块表面向内部深入生长,对照组和实验组老陈醋大曲的曲房温度上升至8 d的36 ℃、38 ℃,曲块温度分别升高至45 ℃、48 ℃,第9天进入大火期,到13 d时,对照组、实验组老陈醋大曲曲房温度分别为38 ℃、39 ℃,曲块温度分别上升至47 ℃、53 ℃。大火期作为关键环节之一,有助于筛选出耐高温的微生物,优化微生物群落结构,以及增强曲块中酶的活性,有利于通风和后续的发酵过程[17]。随着发酵过程的进行,微生物代谢活动减少,产生的热量也随之减少,同时为确保曲块中心残余水分散失、成熟,进行开窗通风,对照组、实验组曲房温度由13 d的38 ℃降至21 d的28 ℃,曲块温度分别由47 ℃、53 ℃逐渐下降至35 ℃、36 ℃。因此,添加小麦可以提高老陈醋大曲在潮火期和大火期的温度,并且在后火期曲房温度下降平缓,有利于大曲品质形成和稳定性。
2.2 山西老陈醋大曲制备过程中微生物菌群的变化
细菌构成了食醋大曲的“生香引擎”,它们能够产生淀粉酶和蛋白酶,通过分解蛋白质和多肽,产生独特风味[18]。由图2A~2C可知,制曲前期(0~9 d),对照组、实验组老陈醋大曲细菌总数分别增加至8.99 lg CFU/g、9.15 lg CFU/g,乳酸菌数分别增加至7.09 lg CFU/g、7.25 lg CFU/g,芽孢杆菌数分别增加至8.48lgCFU/g、8.76 lgCFU/g,随着发酵的进行,细菌总数逐渐下降至21 d的7.15 lg CFU/g、7.67 lg CFU/g,乳酸菌数逐渐下降至21 d的3.18 lg CFU/g、3.45 lg CFU/g,芽孢杆菌数逐渐下降至21 d的6.83 lg CFU/g、7.04 lg CFU/g。在老陈醋大曲的储存阶段,老陈醋大曲细菌总数呈下降趋势,乳酸菌数和芽孢杆菌数呈上升趋势,储存3个月对照组、实验组成曲细菌总数分别为6.69 lg CFU/g、7.38 lg CFU/g,乳酸菌数分别为3.49 lg CFU/g、3.98 lg CFU/g,芽孢杆菌数分别为7.09 lg CFU/g、7.25 lg CFU/g。
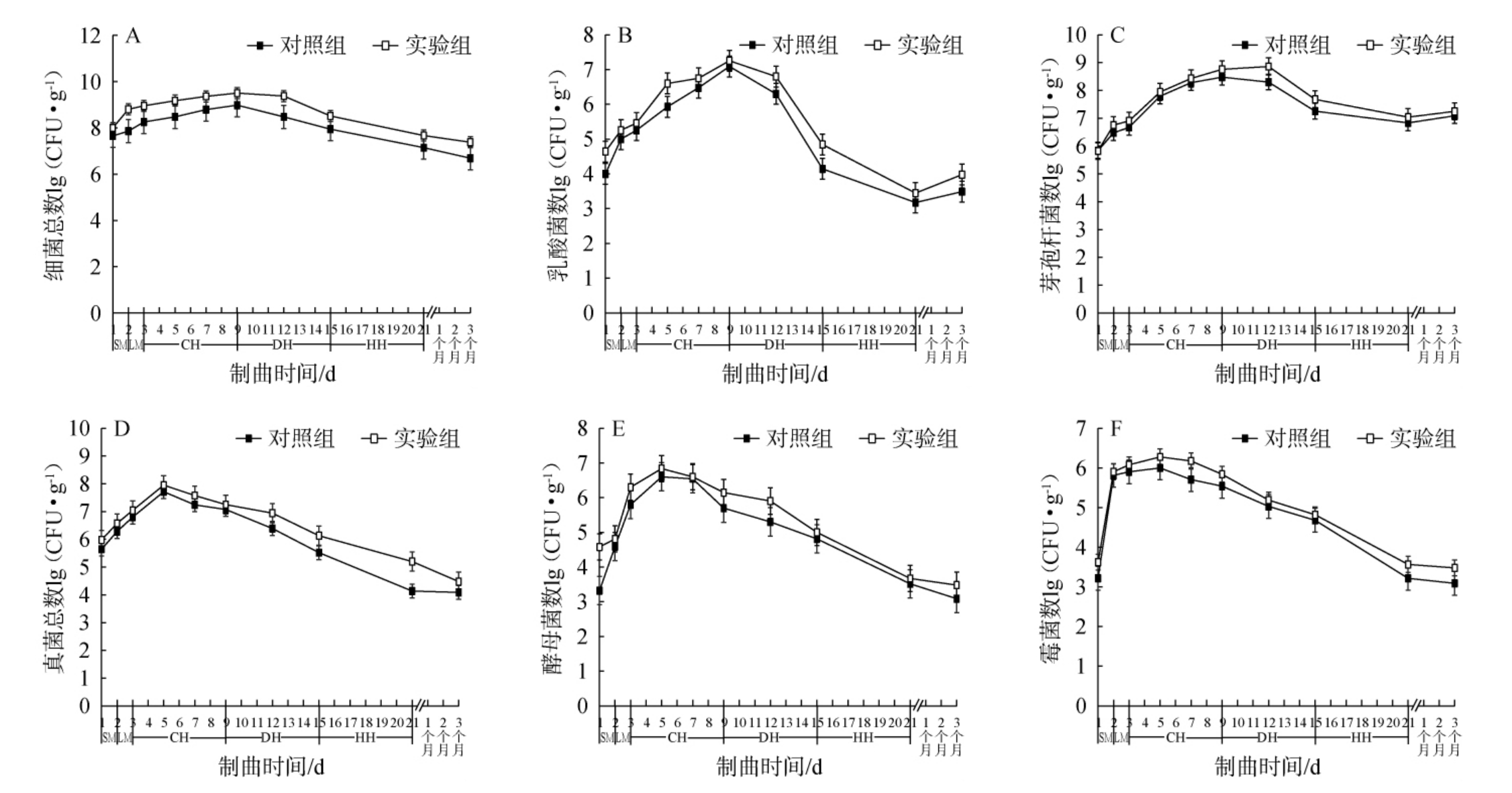
图2 山西老陈醋大曲制备过程中微生物菌群的变化
Fig.2 Changes of microbial communities during preparation process of Shanxi aged vinegar Daqu
老陈醋大曲真菌主要包括霉菌和酵母菌,霉菌能代谢产生液化酶、糖化酶、蛋白酶、酯化酶、纤维素酶等多种酶类,这些酶类均有助于大曲原料降解、风味物质及其前体物形成,酵母菌可分为产醇酵母和产酯酵母,具有产酒、糖化提高酯化度、贡献风味物或香气前体及高效利用原料等功能[19]。由图2D~2F可知,在制曲过程中,真菌总数、酵母菌数和霉菌数均呈现先上升后下降的趋势。0~5 d时,对照组、实验组老陈醋大曲真菌总数逐渐增加至7.72 lg CFU/g、7.95 lg CFU/g,酵母菌数逐渐增加至6.60 lg CFU/g、6.84 lg CFU/g,霉菌数逐渐增加至6.00 lg CFU/g、6.28 lg CFU/g,随着发酵的进行,真菌总数逐渐下降至21 d的4.14 lg CFU/g、5.20 lg CFU/g,酵母菌数逐渐下降至21 d的3.52 lg CFU/g、3.67 lg CFU/g,霉菌数逐渐下降至21 d的3.22 lg CFU/g、3.57 lg CFU/g。在老陈醋大曲的储存阶段,老陈醋大曲真菌总数、酵母菌数和霉菌数呈下降趋势,储存3个月对照组、实验组成曲真菌总数分别为4.09 lg CFU/g、4.48 lg CFU/g,酵母菌数分别为3.09 lg CFU/g、3.46 lg CFU/g,霉菌数分别为3.09 lg CFU/g、3.48 lg CFU/g。
综上,实验组老陈醋大曲的微生物数量整体高于对照组老陈醋大曲,这是因为15%的小麦添加提升了曲块温度,促进了微生物的生长繁殖和各类代谢酶的产生,导致营养物质的分解和转化效率提升,进一步为微生物的生长繁殖提供了必要的碳源、氮源和生长因子。
2.3 山西老陈醋大曲制备过程中酶活的变化
根据GB/T 4257—2011《酿酒大曲通用分析方法》[10],分解大曲“物系”中碳水化合物能力的衡量指标主要是液化力、糖化力和纤维素酶。液化力反映大曲中液化型淀粉酶分解淀粉的能力,其中液化型淀粉酶主要是由霉菌和枯草芽孢杆菌产生[20]。糖化力反映大曲中糖化型淀粉酶从淀粉的非还原性末端开始依次水解α-1,4-葡萄糖苷键产生葡萄糖的能力,主要与霉菌相关[21],XIA Y等[16]研究发现,大曲优势真菌属曲霉属在浓香大曲中具有富集淀粉酶的能力,对大曲糖化力具有一定的贡献。纤维素酶是由内切葡聚糖酶、外切葡聚糖酶和β-葡萄糖苷酶组成的复合酶系,可将纤维素分解为纤维二糖和葡萄糖,主要来源是黑曲霉、红曲霉和木霉[22-23]。
由图3A可知,对照组、实验组老陈醋大曲制备过程中液化力和糖化力变化趋势趋于一致,且实验组液化力和糖化力高于对照组。1~12 d时,液化力和糖化力整体呈上升趋势;12 d时,对照组和实验组老陈醋大曲的液化力分别为1.53 U和1.60 U,糖化力分别为721 U和786 U;随着发酵的进行,液化力趋于平稳,而糖化力先下降后上升的变化趋势,对照组和实验组成曲的液化力分别为1.48 U、1.56 U,糖化力分别为744 U、930 U。小麦本身所含有的糖化酶活力高于大麦,且含有较高的淀粉和蛋白质含量,为微生物的生长代谢提供了更为丰富的营养[24]。
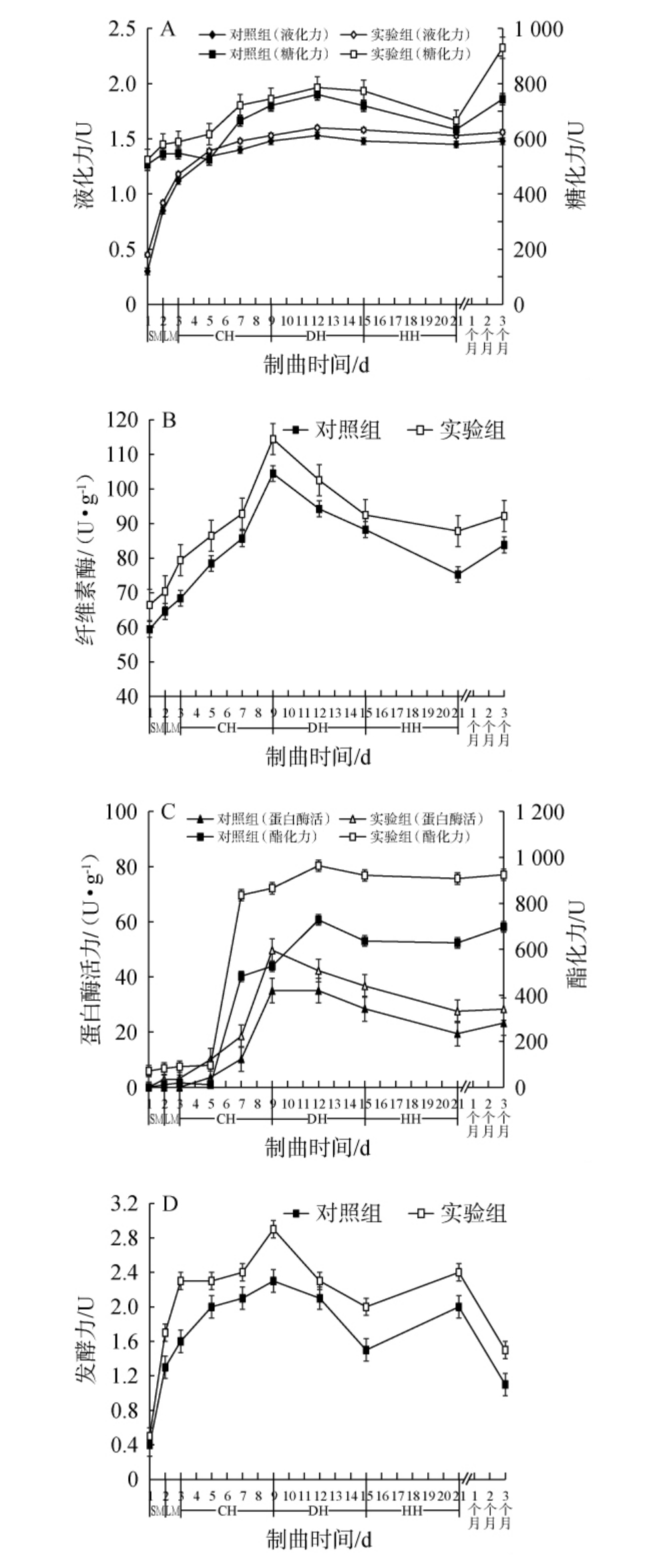
图3 山西老陈醋大曲制备过程中酶活的变化
Fig.3 Changes of enzymatic activities during preparation process of Shanxi aged vinegar Daqu
由图3B可知,对照组和实验组纤维素酶活力变化趋势相似,且实验组纤维素酶活力高于对照组。在1~9 d内,纤维素酶活力整体呈上升趋势,卧曲(1 d)时对照组和实验组纤维素酶活力分别为59.42 U/g和66.46 U/g,第9天分别升高至104.45 U/g和114.45 U/g;随着发酵的进行,纤维素酶活力缓慢下降,到21 d分别降至75.27 U/g和87.84 U/g。从出房到储存阶段,大曲纤维素酶活力呈上升趋势,对照组和实验组储存3个月的成曲纤维素酶活力分别为83.84 U/g和92.17 U/g。大曲的纤维素酶活力提升,不仅提高原料中纤维素降解率,释放被包裹的淀粉颗粒,还增加可发酵糖总量[25]。
蛋白酶将原料谷物中的粗蛋白水解成多肽和氨基酸等,为微生物的生长繁殖给予能量和营养。氨基酸可以继续生成高级醇及由其衍生出来的酯类等挥发性化合物,也可与还原糖发生美拉德反应生成含氮类化合物,其为代谢产物提供结构物质形成香味物质[26]。由图3C可知,对照组和实验组蛋白酶活力变化趋势相似,且实验组蛋白酶活力高于对照组。在制曲前期(1~9 d),蛋白酶活力整体呈上升趋势,对照组、实验组老陈醋大曲蛋白酶活力升高至35.03 U/g、49.71 U/g。制曲后期(9~21 d),蛋白酶活力呈缓慢下降趋势,对照组和实验组出房曲的蛋白酶活力分别降至19.43 U/g、27.56 U/g,在储存阶段,蛋白酶活力呈上升趋势,实验组储存3个月成曲的蛋白酶活力为28.34 U/g,较对照组(23.29 U/g)提高了21.68%。
酯化力是指大曲中酯化酶催化游离有机酸与乙醇合成酯的能力[13]。由图3C可知,在1~5 d内,对照组老陈醋大曲酯化力增长缓慢,潮火期5~9 d,对照组老陈醋大曲酯化力由11 U升高至527 U,在大火期阶段,酯化力得到二次提升,到第12天时,蛋白酶活力达到最高峰为728 U,这个过程是重要的大曲“提香”阶段,添加了小麦的实验组大曲的提温效果也正显现如此。实验组老陈醋大曲酯化力变化趋势与对照组类似,但在整个制曲过程中,实验组的酯化力高于对照组,特别是第12天时,实验组老陈醋大曲酯化力为964 U,较对照组提高了32.42%。在大曲储存阶段,酯化力呈上升趋势,实验组成曲酯化力为925 U,较对照组提高了32.52%。
发酵力反映大曲中的微生物可将糖发酵生成酒精和二氧化碳的能力[13]。由图3D可知,对照组老陈醋大曲从第1天的0.4 U上升至第3天的1.6 U,再上升至第9天的2.3 U,随后开始迅速下降,降低至第15天的1.5 U,在后火期又开始回升至21 d的2.0 U,储存期呈下降趋势,其成曲降低至1.1 U。制曲过程中实验组大曲发酵力变化趋势与对照组一致,实验组老陈醋大曲的发酵力整体高于对照组,其成曲发酵力为1.5 U,较对照组提高了36.36%。
综上,实验组老陈醋大曲在液化力、糖化力、纤维素酶活力、蛋白酶活力、酯化力及发酵力等关键指标上均优于对照组,这是因为小麦的高糖化酶活力及丰富营养成分为微生物代谢提供了更优条件。
2.4 山西老陈醋大曲制备过程中理化指标的变化
2.4.1 老陈醋大曲制备过程中水分和总酸的变化
水分对制曲具有重要的意义,适宜的水分含量能够为微生物的繁殖创造良好的环境条件。成品曲一般要求不超过13%,水分含量较低,微生物的生长代谢则会受到一定的抑制,成品曲更易于储存;若老陈醋大曲出房曲水分过高,可能会导致大曲出现第二次霉变,进而影响其品质。由图4A可知,整个老陈醋大曲制造过程中实际上是一个水分流失的过程,由于温度上升,老陈醋大曲中的水分从入房排列时的37%下降至出房曲的10%。与对照组相比,实验组大曲水分含量无显著差异,其出房曲水分含量为10.57%。卧曲时的曲块质量至少需要达到3.5 kg,而最后产出的曲块质量大约为3 kg。

图4 山西老陈醋大曲制备过程中理化指标的变化
Fig.4 Changes of physicochemical indexes during preparation process of Shanxi aged vinegar Daqu
对发酵过程中的总酸进行控制,可以有效地阻止有害菌的生长,并为微生物参与发酵创造良好的环境[27]。由图4B可知,对照组老陈醋大曲总酸含量从卧曲(第1天)的0.15mmol/10g急剧上升,在晾霉结束达到最高值1.38 mmol/10 g,进入潮火期,对照组老陈醋大曲总酸含量迅速下降,总酸含量缓慢下降至21 d的0.35 mmol/10 g,在储存期内,酸度呈下降趋势,储存3个月成曲总酸含量为0.23 mmol/10 g。这是由于制曲初期,微生物代谢旺盛,产酸菌快速代谢碳水化合物,通过糖酵解途径生成乳酸、乙酸等有机酸,使大曲总酸快速上升,进入潮火期后,水分大量散失,产酸菌因脱水进入代谢停滞或衰亡状态,酸度下降明显,在大火和后火期间,部分耐高温芽孢杆菌开始生长繁殖,通过分解肽类物质持续产酸,总酸的下降速度减缓,而在大曲储存过程中大曲微生物会进行持续代谢活动,从而消耗大曲中的有机酸;其次储存过程中大曲中的产酸菌数量相应减少,有机酸通过产生少量乙醇并发生酯化反应从而产生酯类物质,导致不同贮存时间大曲酸度降低[28-29]。实验组老陈醋大曲总酸变化趋势与对照组一致。整体来看,实验组老陈醋大曲的总酸含量高于对照组大曲,其成曲总酸为0.37 mmol/10 g,较对照组提高了60.87%。这是因为实验组大曲的在制曲过程中整体曲块温度较高,有研究表明,大曲的总酸主要是在高温转化阶段生成的,制曲的顶温和高温的时间对大曲的总酸有直接影响,曲块温度高的大曲其总酸也相对较高[30]。
2.4.2 老陈醋大曲制备过程中淀粉和还原糖的变化
大曲中淀粉含量反映大曲中微生物的数量和与降解淀粉有关的酶类的活性[27]。由图4C可知,在老陈醋大曲制备过程中淀粉含量整体呈下降趋势,对照组和实验组老陈醋大曲由1 d的65.40 g/100 g和69.98 g/100 g分别下降至21 d的53.93 g/100 g和52.55 g/100 g,储存3个月的对照组和实验组成曲淀粉含量分别为54.18 g/100 g和53.87 g/100 g。这是因为制曲前期温度、湿度比较适宜,细菌、真菌、酵母大量增殖,糖化酶、液化酶、蛋白酶大量积累,水解原料中的淀粉,使淀粉含量下降。制曲前期,实验组大曲中淀粉含量相较于对照组较高,这是因为老陈醋大曲制备时用小麦作为原料替换部分大麦,小麦淀粉含量高于大麦淀粉含量。
还原糖是大曲酵母菌和细菌分解淀粉形成的重要产物,代表着微生物代谢活动的旺盛程度[40]。对照组老陈醋大曲的还原糖从卧曲的0.49 g/100 g急剧上升到潮火第2天的1.65 g/100 g,再迅速下降至大火第3天的0.58 g/100 g,之后开始缓慢下降至成曲的0.43 g/100 g。一方面原料不断分解产生还原糖,另一方面还原糖被微生物利用,或与氨基酸形成羰氨缩合,并且在特定的环境下可以引发美拉德反应,从而生成香气成分的前体物质[21]。实验组的还原糖含量变化趋势与上述一致,在制曲过程中,实验组老陈醋大曲大曲在制曲第7天还原糖含量达到最高,为1.85 g/100 g,其成曲还原糖含量为0.47 g/100 g,相较于对照组提高了12.12%。这是因为实验组制曲原料小麦淀粉含量整体优于大麦,其糖化力、液化力和纤维素酶活力较高。
2.4.3 老陈醋大曲制备过程中氨基酸态氮的变化
大曲的品质优劣直接受到氨基酸态氮含量的影响。若大曲中氨基酸态氮的含量较高,其香气将更为浓烈;相反,若氨基酸态氮含量较低,则其香味会显得较为清淡[27]。由图4D可知,对照组及实验组老陈醋大曲氨基酸态氮含量变化趋势一致,均呈先上升后下降的趋势,对照组和实验组均在第9天达到最高值,分别为0.27 g/100 g、0.29 g/100 g,到21 d时,其含量分别降低至0.16 g/100 g、0.19 g/100 g;储存期内氨基酸态氮含量呈缓慢上升趋势,其成曲中氨基酸态氮含量分别为0.21 g/100 g、0.24 g/100 g,相较于对照组提高了14.29%。
综上,实验组老陈醋大曲在总酸、还原糖和氨基酸态氮含量均高于对照组老陈醋大曲,这表明小麦原料替代结合温度调控可有效优化大曲发酵过程中的物质转化。
2.5 山西老陈醋大曲制备过程中挥发性香气成分的变化
老陈醋大曲制备过程中大火结束、后火结束以及成曲三个关键时间点样品中共检出54种挥发性风味物质,包含14种醇类、12种酯类、5种醛类、3种烷烃、4种酮类、7种酸类、4种吡嗪类以及5种其他类化合物。选取其中含量较高的22种物质进行聚类分析,结果见图5。
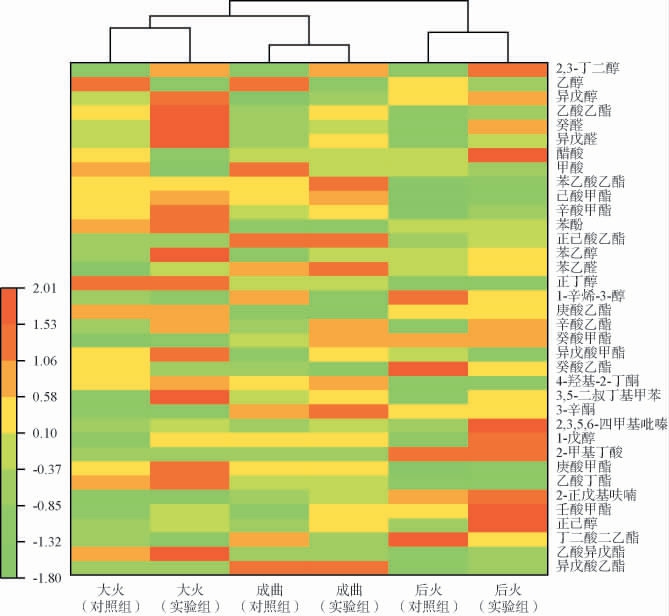
图5 山西老陈醋大曲制备过程中挥发性风味物质聚类分析热图
Fig.5 Heat map of cluster analysis of volatile flavor components during preparation process of Shanxi aged vinegar Daqu
由图5可知,对照组和实验组老陈醋大曲制备过程中大火结束和成曲样品聚为一类,后火结束样品聚为一类。实验组老陈醋大曲成曲挥发性风味物质总含量(10.03 mg/100 g)高于对照组(5.13 mg/100 g)。现有研究表明,老陈醋大曲样品中典型特征挥发性香气物质为2,3-丁二醇、2,3,5,6-四甲基吡嗪、苯乙醇、苯乙醛、正己醇[30]。添加15%小麦的老陈醋大曲成曲中2,3-丁二醇、2,3,5,6-四甲基吡嗪、苯乙醇、苯乙醛和正己醇的含量分别为4.86 mg/100 g、0.69 mg/100 g、0.15 mg/100 g、0.18 mg/100 g和0.21 mg/100 g,较对照组分别提高了358.49%、335.00%、200.00%、20.00%和90.91%,侯小歌等[30]研究发现,己醇和四甲基吡嗪可作为强筋小麦大曲区分其他大曲特征挥发性代谢化合物。四甲基吡嗪(川芎嗪)不仅是大曲和老陈醋的关键风味物质,为大曲带来浓郁的坚果香和烘烤香气,赋予老陈醋醇厚的焦糖香和微妙的酱香,并且其具有扩张血管,改善微循环及抑制血小板积聚作用的功能[31],是GB/T 19777—2013《地理标志产品山西老陈醋》[32]中规定的山西老陈醋的特征功能成分。有研究表明[33],川芎嗪的合成途径主要是美拉德反应和微生物合成途径,其中美拉德反应是指在加热条件下,羰基化合物(如还原糖)与含氨基物质(氨基酸、肽等)反应生成α-二羰基中间体,经斯特勒克降解形成α-氨基酮,最终通过缩合反应生成吡嗪类化合物(如川芎嗪)。在制曲过程中,温度是川芎嗪的合成关键影响因素,因此采用添加小麦进行大曲提温,进而提升老陈醋成品中川芎嗪的含量。
3 结论
本研究通过添加15%小麦替代大麦制备山西老陈醋大曲,系统性揭示了小麦添加对老陈醋大曲制备过程中温度动态、微生物演替、酶活变化及挥发性风味物质的影响规律。结果表明,小麦添加使大火期曲块最高温度提高了6 ℃,进而影响了微生物的菌群数量和酶活。与对照组相比,实验组优势菌群丰度更高,直接驱动液化力、糖化力、纤维素酶活、酯化力、蛋白酶活、发酵力的提升。添加小麦的工艺显著促进2,3-丁二醇、2,3,5,6-四甲基吡嗪(川芎嗪)、苯乙醇、苯乙醛和正己醇等关键风味物质的积累,赋予大曲更浓郁的醇香与酱香特征。未来可深入探讨微生物种类、数量、代谢酶系与理化指标的关系,揭示大曲发酵机制,助力改进生产工艺、提升大曲质量。
[1]潘强林,岳松,张庆,等.大曲功能菌的分离及应用进展[J].食品与发酵工业,2024,50(16):408-420.
[2]王保军,王建云,彭仕颉,等.传统醋用大曲生产工艺升级的研究发展[J].食品安全导刊,2023(8):115-118.
[3]LIU J J,CHEN J Y,FAN Y,et al.Biochemical characterisation and dominance of different hydrolases in different types of Daqu-a Chinese industrial fermentation starter[J].J Sci Food Agr,2018,98(1):113-121.
[4]FAN G S,SUN B G,FU Z L,et al.Analysis of physicochemical indices,volatile flavor components, and microbial community of a light-flavor Daqu[J].J Am Soc Brew Chem,2018,76(3):209-218.
[5]胥鑫钰,吕志远,张梦梦,等.中高温大曲培养过程中的多组学研究[J].酿酒,2022,49(4):49-52.
[6]汤涵岚.基于宏基因组分析增温对食醋大曲固态发酵过程中微生物菌群的影响[D].广州:华南理工大学,2019.
[7]侯小歌,樊俊鹏,郭福利,等.小麦品种对浓香大曲细菌群落与挥发性风味化合物的影响[J].食品工业科技,2024,45(24):133-146.
[8]王洋,谢菲,杜礼泉,等.酿酒专用小麦大曲中挥发性风味成分与微生物群落相关性分析[J].中国酿造,2024,43(2):71-81.
[9]丁伟,魏莎莎,闫裕峰,等.山西老陈醋大曲制备过程中理化因子、微生物群落变化及风味形成规律[J].中国酿造,2022,41(5):52-59.
[10]中华人民共和国工业和信息化部.QB/T 4257—2011 酿酒大曲通用分析方法[S].北京:轻工业出版社,2011.
[11]炊伟强.大曲传统感官评价与其内在质量、理化指标的关系[D].无锡:江南大学,2010.
[12]尉嘉眙,常强,蒋超,等.大曲理化性质与白酒产品风味的相关性分析[J].食品工业科技,2020,41(18):244-251.
[13]冯锋.传统食醋大曲固态发酵过程中微生物多样性及其主要优势微生物产酶的研究[D].广州:华南理工大学,2016.
[14]黄婷.镇江香醋酿造微生物功能解析及酿醋人工菌群构建[D].无锡:江南大学,2022.
[15]王志强,蒋学剑,张亮,等.浓香型白酒大曲制备过程中细菌群落、环境因子和理化特性研究[J].酿酒科技,2023(11):35-41.
[16]XIA Y, ZHOU W, DU Y K, et al.Difference of microbial community and gene composition with saccharification function between Chinese Nongxiangxing Daqu and Jiangxiangxing daqu[J].J Sci Food Agr,2023,103(2):637-647.
[17]张新红,张源.浓香型大曲质量影响因素研究进展[J].生物化工,2020,6(4):118-122.
[18]李伟安,曹建全,刘建波,等.影响浓香型大曲糖化力的因素[J].酿酒,2022,49(5):77-79.
[19]李兵.浓香型白酒大曲中五种主要酶产生菌的多样性及变化规律研究[D].成都:西华大学,2020.
[20]张清玫.浓香大曲微生物群落结构解析与功能微生物筛选[D].无锡:江南大学,2022.
[21]刘石雪,武艳丽,王秀菊,等.中高温大曲发酵过程中理化指标及微生物消长规律研究[J].酿酒科技,2024(8):25-29,37.
[22]宋川,刘双平,敖宗华,等.白酒酿造微生物酯化酶的研究进展[J].酿酒,2024,51(2):34-40.
[23]美合热阿依·木台力甫,凯迪日耶·玉苏普,王继莲.微生物来源纤维素酶的工业应用进展[J].农产品加工,2021(16):60-62,68.
[24]向双全,周志刚,张志刚,等.大曲蛋白酶对固态酿酒发酵的影响[J].酿酒科技,2016(7):47-50.
[25]XIAO H G,HUI M,SUN Z K,et al.Associations between wheat varieties and the functional microbial community of Nongxiangxing daqu from northern China[J].LWT-Food Sci Technol,2023,185:115119.
[26]WU Y S,HOU Y X,CHEN H,et al."Key Factor"for Baijiu quality:research progress on acid substances in Baijiu[J].Foods, 2022, 11(19):2959.
[27]张亮,王志强,汤承友,等.提高制曲温度和延长中挺时间对大曲质量的影响[J].酿酒,2023,50(1):107-109.
[28]王佳丽.山西老陈醋大曲制备过程中微生物群落动态变化及优良霉菌的筛选[D].晋中:山西农业大学,2019.
[29]刘荣,杨勇强,杨希盛.清香大曲培曲过程中理化指标的变化[J].食品工业,2023,44(7):37-39.
[30]侯小歌,樊俊鹏,郭福利,等.小麦品种对浓香大曲细菌群落与挥发性风味化合物的影响[J].食品工业科技,2024,45(24):133-146.
[31]刘雄.中、高温大曲固态发酵过程微生物菌群结构变化的研究[D].广州:华南理工大学,2017.
[32]中华人民共和国卫生部中国国家标准化管理委员会.GB/T 19777—2013 地理标志产品 山西老陈醋[S].北京:中国标准出版社,2013.
[33]张翔宇.枯草芽孢杆菌D17生成川芎嗪机制解析[D].太原:山西大学,2024.