灰葡萄孢菌(Botrytis cinerea)是一种广泛分布的植物病原真菌,该菌具有高度多宿主特性[1-3],可侵染超过200种单子叶和双子叶植物,包括葡萄、草莓、番茄等经济作物,引发灰霉病[4]。灰葡萄孢菌的分生孢子具有强扩散能力,可通过气流或机械接触传播,常导致作物采前减产与采后腐烂[5-6]。目前,针对灰葡萄孢菌的防控策略仍以化学防治为主,使用化学药剂虽效果显著,但长期使用会导致病原菌产生抗药性[7-8],对环境造成污染,且会引发食品安全问题。生物防治作为一种环境友好型的防控手段,关注度逐年提升,已成为研究热点。张晓云等[9]筛选获得一株贝莱斯芽胞杆菌(Bacillus velezensis)HMB28023,采用对峙培养法发现其对灰葡萄孢菌具有明显的抑菌效果,抑菌率为71.4%;HU D等[10]从葡萄种植地分离到的酿酒酵母(Saccharomyces cerevisiae)KONDO170908可有效抑制灰葡萄孢菌,并能够明显降低葡萄灰霉病的发病率;李素平等[11]研究发现,利用筛选获得的自溶性产酶溶杆菌LE16能够显著抑制灰葡萄孢菌的生长繁殖,抑菌率为34.99%~100%。
解淀粉芽孢杆菌(Bacillus amyloliquefaciens)作为一种潜在的高效生防菌,具有多种优良特性,如产生抗菌物质、诱导植物抗性等[12-13],在生物防治领域具有广阔的应用前景。解淀粉芽孢杆菌能够分泌多种抑菌活性物质,如脂肽类抗生素伊枯草菌素、泛革素和表面活性素等[14-16],能够破坏病原菌的细胞结构、抑制其生理功能,发挥其广谱抗菌作用[17]。廖凤平等[18]从海底淤泥中分离筛选到一株可有效抑制指状青霉(Penicillium digitatum)生长的解淀粉芽孢杆菌HY2-1,通过对其发酵条件优化,其发酵液对指状青霉的抑菌圈直径提高了26.5%;李扬凡等[19]利用筛选获得的解淀粉芽孢杆菌HMB33604对马铃薯黑痣病进行防治效果测定,结果表明,菌株HMB33604发酵液和上清液对马铃薯黑痣病防效显著,抑菌率分别为52.2%和66.4%;王楠等[20]研究发现,解淀粉芽孢杆菌SH-53发酵液对番茄枯萎病菌生长具有显著抑制作用,通过发酵条件优化,抑菌率提升了14.06%。
在实际应用中生防菌菌株生物量较低,发酵产生的抑菌物质含量较少,难以满足生物防治工业化的需求[21],通过优化生防菌发酵条件可提高其菌体数量及代谢产物的分泌。相较于单因素试验的孤立变量分析,响应面法(response surface methodology,RSM)可同时评估多个因素间的交互作用,通过二次多项式模型拟合复杂非线性关系,克服了传统正交试验仅适用于线性或低阶交互作用的局限,并且能够直观观察因素与响应值之间的关系,快速定位最优条件[22-23]。因此,本研究以前期筛选获得的一株解淀粉芽孢杆菌HRH317为研究对象,以对灰葡萄孢菌的抑菌圈直径为响应值,通过单因素试验及响应面法对菌株HRH317的发酵条件进行优化,增强菌体代谢产物的分泌,进而提升菌株HRH317对灰葡萄孢菌的抑菌活性,以期为开发解淀粉芽孢杆菌HRH317生防菌剂提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
解淀粉芽孢杆菌HRH317:分离自山西农业大学玉米田,保藏于中国微生物菌种保藏管理委员会普通微生物中心(编号为CGMCC No.7314);灰葡萄孢菌:广州微生物保藏中心(编号为GDMCC3.47)。
1.1.2 试剂
牛肉膏、蛋白胨(均为生化试剂):合肥博美生物科技有限责任公司;氯化钠、葡萄糖、琼脂(均为分析纯):合肥基努生物科技有限公司;其他试剂均为国产分析纯或生化试剂。
1.1.3 培养基
斜面培养基[24]:牛肉膏0.3 g、蛋白胨1.0 g、氯化钠0.5 g、琼脂2.0 g、蒸馏水100 mL,pH 7.2,121 ℃高压蒸汽灭菌20 min。
种子培养基[24]:蛋白胨1.0 g、氯化钠0.5 g、牛肉膏0.5 g、蒸馏水100 mL,pH 7.2,121 ℃高压蒸汽灭菌20 min。
发酵培养基[24]:蛋白胨1.0 g、牛肉膏0.5 g、葡萄糖1.0 g、氯化钠0.5 g、蒸馏水100 mL,pH 7.0,121 ℃高压蒸汽灭菌20 min。
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基[24]:马铃薯20.0 g、葡萄糖2.0 g、琼脂2.0 g、氯霉素0.01 g、蒸馏水100 mL,pH 7.2,121 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
UV-1601型紫外分光光度计:北京北分瑞利分析仪器(集团)有限责任公司;BKQ-B50II型高压蒸汽灭菌锅:山东博科消毒设备有限公司;BBS-DSC型超净工作台:济南鑫贝西生物技术有限公司;TGL-16 WS型高速离心机:湖南湘仪实验室仪器开发有限公司;YJY-200 B型摇床:上海跃进医疗器械有限公司;SPX-450 B型生化培养箱:杭州绿博仪器有限公司;PHSJ-3F型pH计:上海仪天科学仪器有限公司;牛津杯(外径7.8 mm,内径6.0 mm,高10.0 mm):上海精密仪器仪表有限公司。
1.3 方法
1.3.1 解淀粉芽孢杆菌HRH317的活化
接种环取斜面保藏菌种HRH317至斜面培养基,37 ℃恒温培养24 h,制成斜面菌种,活化2次,备用。
1.3.2 解淀粉芽孢杆菌HRH317种子液的制备
采用接种环从斜面上挑取1/3活化后的解淀粉芽孢杆菌HRH317菌苔,接种于种子培养基,装液量为50 mL/250 mL,于37 ℃、150 r/min条件下,摇床恒温培养24 h,制得种子液。
1.3.3 解淀粉芽孢杆菌HRH317发酵液的制备
将解淀粉芽孢杆菌HRH317种子液以2%(V/V)的接种量接种于发酵培养基,装液量为40 mL/250 mL,35 ℃、150 r/min条件下,摇床恒温振荡培养24 h,制得发酵液[25-26]。
1.3.4 解淀粉芽孢杆菌HRH317发酵上清液的制备
以4 ℃、10 000 r/min条件下将解淀粉芽孢杆菌HRH317发酵液离心20 min,收集上清液,经0.22 μm微孔滤膜过滤,将滤液置于4 ℃下保存备用。
1.3.5 灰葡萄孢菌孢子悬液的制备
将斜面保藏的灰葡萄孢菌菌种划线接种于PDA培养基斜面,28 ℃恒温培养5 d,制成斜面菌种,活化2次,斜面中加入5 mL无菌生理盐水,制成孢子悬液。孢子悬液经无菌脱脂棉过滤,收集滤液,用无菌生理盐水调制孢子悬液浓度为1.0×106 CFU/mL,4 ℃保存备用。
1.3.6 抑菌活性的测定
取200 μL灰葡萄孢菌孢子悬液均匀涂布于PDA培养基平板中,无菌镊子夹取1个牛津杯置于加入孢子悬液的平板中心,牛津杯中加入200 μL解淀粉芽孢杆菌HRH317发酵上清液,以发酵培养基为对照,将培养皿置于4 ℃冰箱中,24 h后取出置于28 ℃恒温培养箱中培养5 d,期间观察菌体生长情况,培养结束取出培养皿,采用游标卡尺测量抑菌圈直径,以抑菌圈的直径作为衡量抑菌活性大小的指标[27]。
1.3.7 解淀粉芽孢杆菌HRH317发酵条件优化
(1)单因素试验
在1.3.3基础上,以抑菌圈直径(Y)为评价指标,考察不同发酵温度(31 ℃、33 ℃、35 ℃、37 ℃、39 ℃)、发酵时间(12 h、18 h、24 h、30 h、36 h)、装液量(20 mL/250 mL、30mL/250mL、40mL/250mL、50mL/250mL、60mL/250mL)、接种量(1%、2%、3%、4%、5%)对解淀粉芽孢杆菌HRH317对灰葡萄孢菌抑菌活性的影响。
(2)响应面试验设计
在单因素试验结果的基础上,固定接种量为2%,选择影响较大的因素发酵温度(X1)、发酵时间(X2)、装液量(X3)为考察指标,以抑菌圈直径为响应值,采用Design-Expert 13.0设计3因素3水平的Box-Behnken响应面优化试验,试验因素与水平见表1。
表1 解淀粉芽孢杆菌HRH317发酵条件优化Box-Behnken响应面试验因素与水平
Table 1 Factors and levels of Box-Behnken response surface experiments for Bacillus amyloliquefaciens HRH317 fermentation conditions optimization

因素-1水平0 1 X1发酵温度/℃ X2发酵时间/h X3装液量/(mL·250 mL-1)35 18 40 37 24 50 39 30 60
1.3.8 数据处理
每个试验重复3次,采用Excel 2010、SPSS 23.0处理数据,结果用“平均值±标准差”表示;采用Excel 2010、Design-Expert 13.0软件绘图。
2 结果与分析
2.1 解淀粉芽孢杆菌HRH317发酵条件优化单因素试验
2.1.1 不同发酵温度对解淀粉芽孢杆菌HRH317抑菌效果的影响
不同发酵温度对解淀粉芽孢杆菌HRH317抑菌效果的影响见图1。
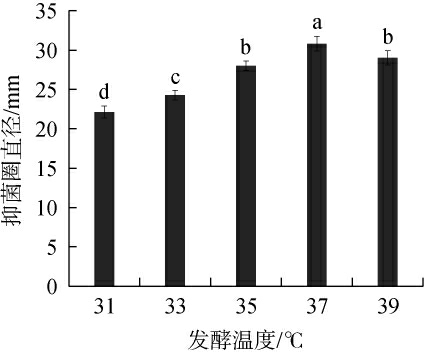
图1 不同发酵温度对解淀粉芽孢杆菌HRH317抑菌效果的影响
Fig.1 Effect of different fermentation temperature on the antibacterial effect of Bacillus amyloliquefaciens HRH317
不同小写字母表示差异显著(P<0.05)。下同。
由图1可知,随着发酵温度的升高,解淀粉芽孢杆菌HRH317对灰葡萄孢菌的抑菌圈直径呈先增大后减小的趋势,当发酵温度为37 ℃时,抑菌圈直径最大,为(30.82±0.93)mm。分析原因可能是,发酵温度升高使微生物菌体新陈代谢加快,酶活性增大,因而合成和分泌抑菌物质的能力随之增强,但发酵温度过高会导致微生物生长受到抑制,影响抑菌物质的产生[28],因此,选择37 ℃为最佳发酵温度。
2.1.2 不同发酵时间对解淀粉芽孢杆菌HRH317抑菌效果的影响
不同发酵时间对解淀粉芽孢杆菌HRH317抑菌效果的影响见图2。由图2可知,解淀粉芽孢杆菌HRH317对灰葡萄孢菌的抑菌圈直径随发酵时间延长,呈先升高后降低的趋势,当发酵时间为24 h时,抑菌圈直径最大,为(32.06±0.71)mm。分析原因可能是,发酵初期,菌体代谢活动相对较弱,产生的抑菌物质较少,随着发酵的进行,菌体代谢活动旺盛,大量合成分泌抑菌物质[29],抑菌活性增强;但发酵时间过长,由于营养物质大量被消耗,菌体合成抑菌物质的能力下降,影响对灰葡萄孢菌的抑菌效果,因此,选择24 h为最优发酵时间。
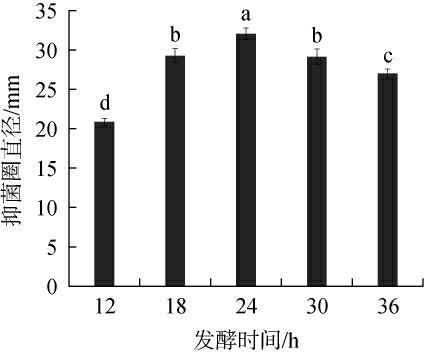
图2 不同发酵时间对解淀粉芽孢杆菌HRH317抑菌效果的影响
Fig.2 Effect of different fermentation time on the antibacterial effect of Bacillus amyloliquefaciens HRH317
2.1.3 不同装液量对解淀粉芽孢杆菌HRH317抑菌效果的影响
不同装液量对解淀粉芽孢杆菌HRH317抑菌效果的影响见图3。
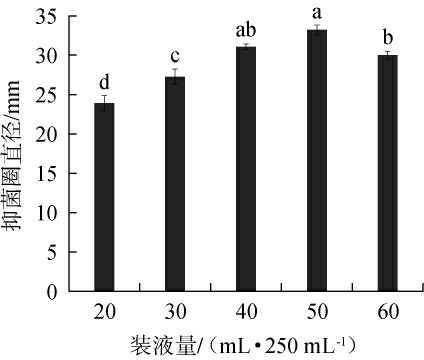
图3 不同装液量对解淀粉芽孢杆菌HRH317抑菌效果的影响
Fig.3 Effect of different loading volume on the antibacterial effect of Bacillus amyloliquefaciens HRH317
由图3可知,随着装液量的增加,解淀粉芽孢杆菌HRH317对灰葡萄孢菌的抑菌圈直径呈先升高后降低的趋势,当装液量为50 mL时,抑菌圈直径最大,为(33.21±0.65)mm。分析原因可能是,装液量过多会造成溶氧量降低,影响菌体代谢产物的产生[30],抑菌物质合成减少,导致抑菌活性下降,因此,选择50 mL/250 mL为最佳装液量。
2.1.4 不同接种量对解淀粉芽孢杆菌HRH317抑菌效果的影响
不同接种量对解淀粉芽孢杆菌HRH317抑菌效果的影响见图4。由图4可知,随着接种量的升高,解淀粉芽孢杆菌HRH317对灰葡萄孢菌的抑菌圈直径呈先升高后降低的趋势,当接种量为2%时,抑菌圈直径最大,为(33.92±0.96)mm。分析原因可能是,接种量较低时,菌体数量较少,代谢产物积累缓慢[31],但接种量过多时,菌体数量过多,易造成溶氧量供给不足,发酵液中抑菌物质的合成受限[18],因此,选择2%为最佳接种量。
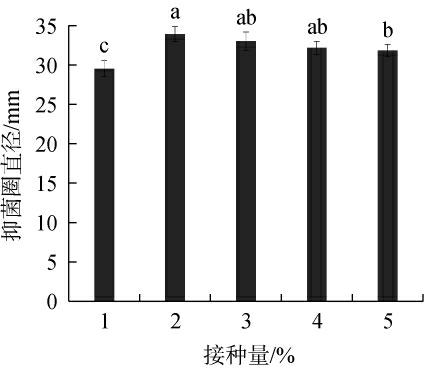
图4 不同接种量对解淀粉芽孢杆菌HRH317抑菌效果的影响
Fig.4 Effect of different inoculum on the antibacterial effect of Bacillus amyloliquefaciens HRH317
2.2 解淀粉芽孢杆菌HRH317发酵条件优化响应面试验结果
2.2.1 响应面试验结果与分析
在单因素试验结果的基础上,固定接种量为2%,选择影响较大的因素发酵温度(X1)、发酵时间(X2)、装液量(X3)为考察指标,以抑菌圈直径(Y)为响应值,采用Design-Expert 13.0设计3因素3水平的Box-Behnken响应面优化试验,试验设计及结果见表2,方差分析见表3。
表2 解淀粉芽孢杆菌HRH317发酵条件优化Box-Behnken响应面试验设计及结果
Table 2 Design and results of Box-Behnken response surface experiments for Bacillus amyloliquefaciens HRH317 fermentation conditions optimization
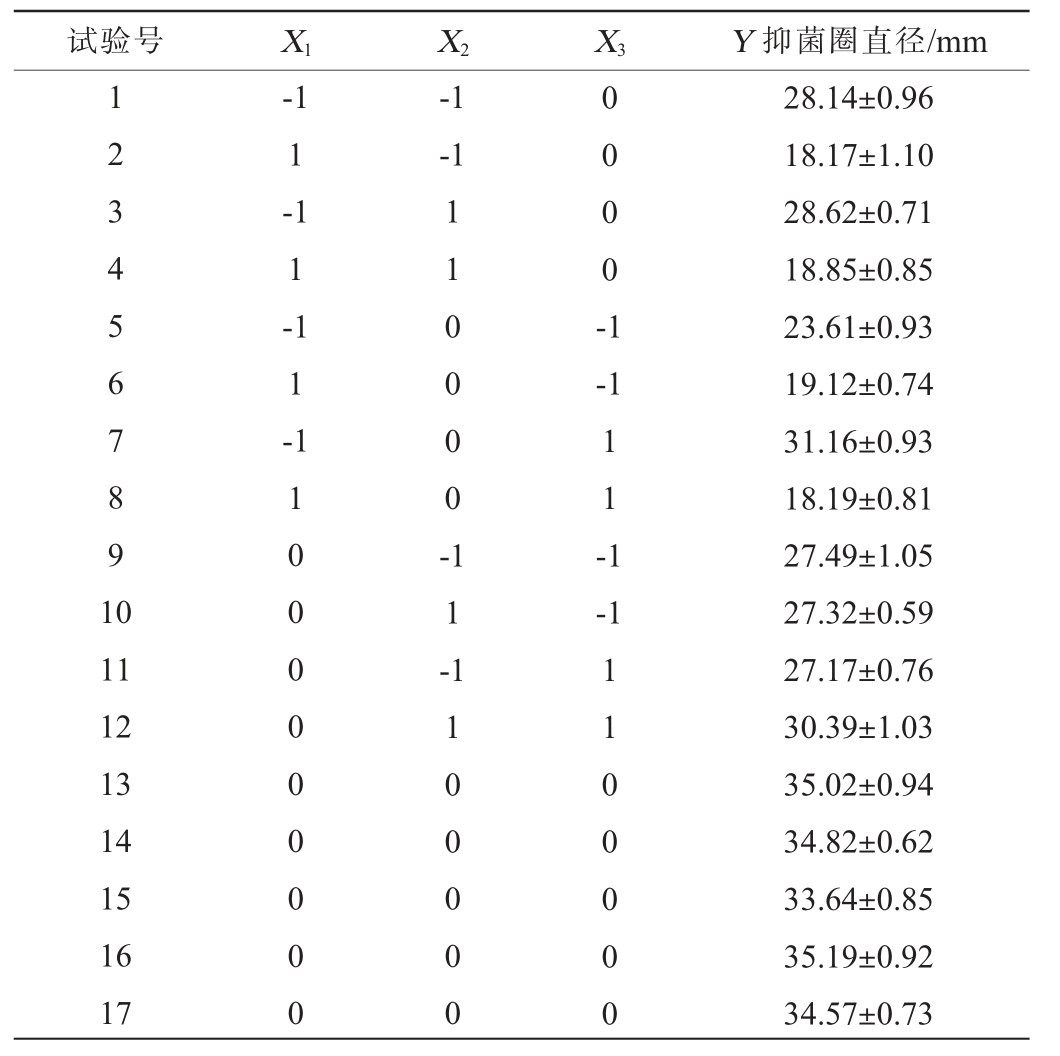
试验号 X1 X2 X3 Y 抑菌圈直径/mm 1234567891 0-1 1-1 1-1 1-1-1-1 11 0000 -0 0 0 0 -1-1 1 1 -1-1 11 12 13 14 15 16 17 1000000 000 1 1 -1100000 1100000 28.14±0.96 18.17±1.10 28.62±0.71 18.85±0.85 23.61±0.93 19.12±0.74 31.16±0.93 18.19±0.81 27.49±1.05 27.32±0.59 27.17±0.76 30.39±1.03 35.02±0.94 34.82±0.62 33.64±0.85 35.19±0.92 34.57±0.73
表3 回归模型方差分析
Table 3 Variance analysis of regression model
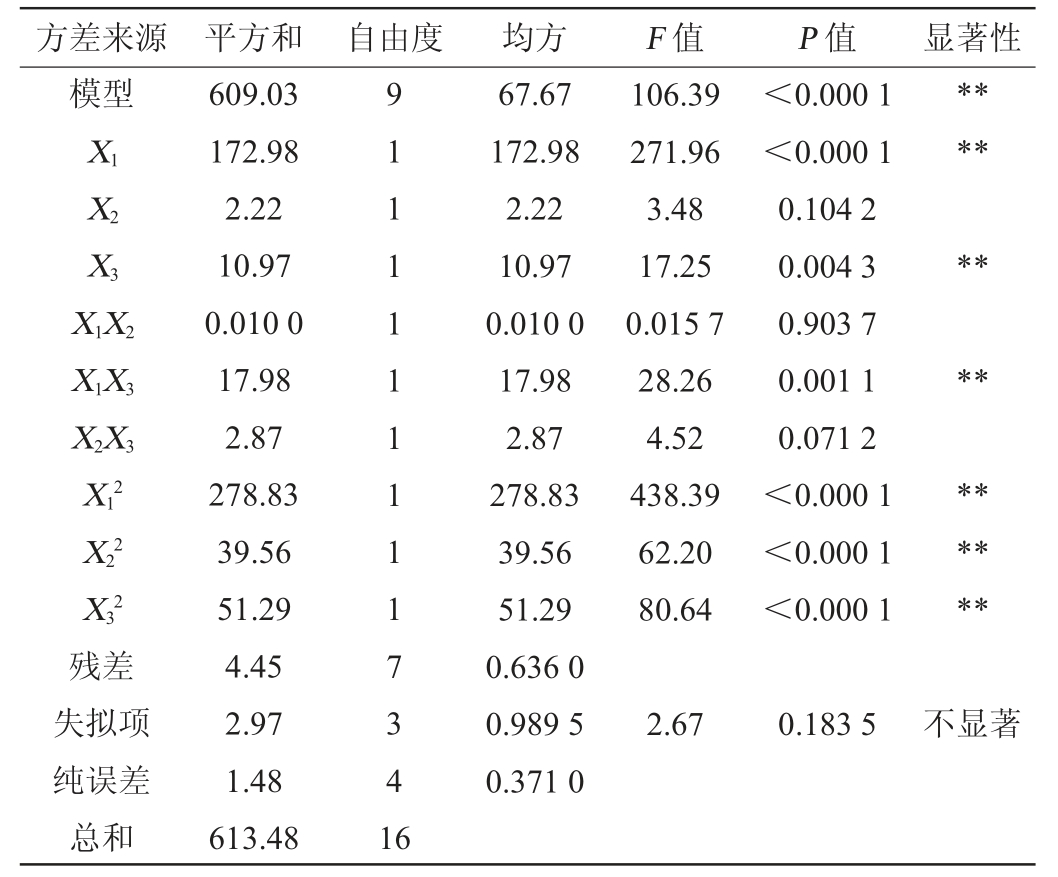
注:“*”表示对结果影响显著(P<0.05),“**”表示对结果影响极显著(P<0.01)。
方差来源 平方和 自由度 均方 F 值 P 值 显著性模型X1 X2 X3 X1X2 X1X3 X2X3 X12 X22 X32残差失拟项纯误差总和609.03 172.98 2.22 10.97 0.010 0 17.98 2.87 278.83 39.56 51.29 4.45 2.97 1.48 613.48 91111111117341 6 67.67 172.98 2.22 10.97 0.010 0 17.98 2.87 278.83 39.56 51.29 0.636 0 0.989 5 0.371 0 106.39 271.96 3.48 17.25 0.015 7 28.26 4.52 438.39 62.20 80.64<0.000 1<0.000 1 0.104 2 0.004 3 0.903 7 0.001 1 0.071 2<0.000 1<0.000 1<0.000 1**************2.67 0.183 5不显著
利用Design Expert 13.0软件对表2数据进行二次多元回归拟合分析,得到抑菌圈直径对发酵温度、发酵时间、装液量的二次多项式回归方程:Y=34.65-4.65X1+0.526 3X2+1.17X3+0.05X1X2-2.12X1X3+0.8475X2X3-8.14X12-3.07X22-3.49X32
由表3可知,模型的P<0.000 1,极显著(P<0.01),失拟项P值为0.183 5,不显著(P>0.05),说明模型的拟合度良好,能够有效解释响应变量的变异;决定系数R2=0.992 7,调整决定系数R2Adj=0.983 4,表明该模型解释了99%以上的数据变异,且预测能力良好;变异系数(coefficient of variation,CV)=2.88%,说明试验误差较小,进一步验证了模型的可靠性。由P值可知,一次项X1、X3、交互项X1X3及二次项X12、X22、X32对结果影响均极显著(P<0.01)。由F值可知,影响解淀粉芽孢杆菌HRH317抑菌活性的因素主次顺序为X1>X3>X2。
2.2.2 响应面分析
利用Design-Expert13.0软件进一步绘制出自变量和因变量的三维立体响应面曲面图,更加直观地表明其中一个因变量保持在中心值时其他两个因变量的变化对解淀粉芽孢杆菌抑菌效果的影响,更加准确的筛选出发酵的最优条件,结果见图5。
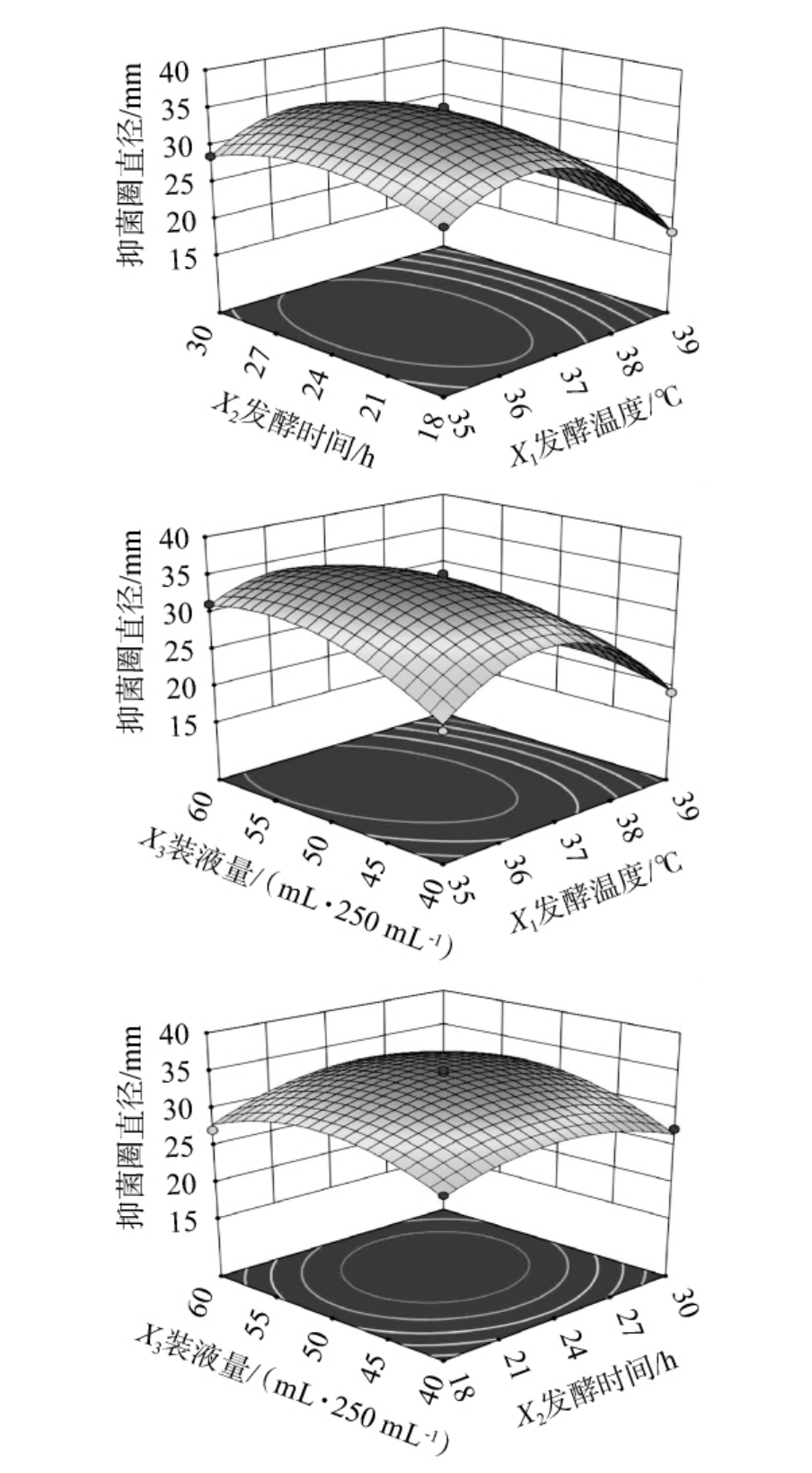
图5 各因素间交互作用对解淀粉芽孢杆菌HRH317抑菌效果影响的响应曲面及等高线
Fig.5 Response surface plots and contour lines of effects of interaction between each factor on the antibacterial effect of Bacillus amyloliquefaciens HRH317
由图5可知,各因素间交互作用的响应面曲面均呈凸面,说明都存在最大值,其中发酵温度与装液量间交互作用对解淀粉芽孢杆菌HRH317抑菌圈效果影响的响应面曲面最陡峭,等高线接近椭圆形,说明对结果影响较大;发酵时间与发酵温度间交互作用对解淀粉芽孢杆菌HRH317抑菌圈效果影响的响应面曲面中,随发酵温度变化呈现的曲线坡度较陡峭,说明对抑菌圈效果影响明显,而随发酵时间变化呈现的曲线坡度较缓,说明其对抑菌圈效果影响次之,等高线虽接近椭圆形,但二者交互作用对结果影响较小;发酵时间与装液量间交互作用对解淀粉芽孢杆菌HRH317抑菌圈效果影响的响应面曲面坡度较缓,等高线接近圆形,说明对结果影响也较小,这与方差分析结果一致。
2.2.3 验证性试验
采用Design-Expert13.0对回归方程求一阶偏导,得出解淀粉芽孢杆菌HRH317抑制灰葡萄孢菌的最优发酵条件为发酵温度36.36℃、发酵时间24.53h、装液量52.94 mL/250 mL,在此条件下,抑菌圈直径的预测值可达35.58 mm。为便于试验操作,将优化后的发酵条件修正为发酵温度36 ℃、发酵时间25 h、装液量53 mL/250 mL,以此条件下重复3次验证试验,得到抑菌圈直径实测值为(34.97±0.16)mm,与预测值一致,由此可以证明回归方程有效可靠。解淀粉芽孢杆菌HRH317发酵上清液对灰葡萄孢菌的抑菌圈直径比优化前的(28.02±0.69)mm提高了24.8%,说明优化发酵条件能够有效提升抑菌活性。
3 结论
为提高解淀粉芽孢杆菌HRH317发酵上清液对灰葡萄孢菌的抑菌效果,本研究以抑菌圈直径为响应值,通过单因素试验和响应面试验优化得到解淀粉芽孢杆菌HRH317抑制灰葡萄孢菌的最佳发酵条件为发酵温度36 ℃、发酵时间25 h、装液量53 mL/250 mL,在此条件下,抑菌圈直径为(34.97±0.16)mm,较优化前的抑菌圈直径[(28.02±0.69)mm]提高了24.8%,本研究结果为后续开发菌株生防菌剂提供数据支持。
[1]SI H L, ZHANG K, LI B, et al. BcSDR1 is involved in regulation of glucose transport and cAMP and MAPK signaling pathways in Botrytis cinerea[J].J Int Agr,2022,21(9):2628-2640.
[2]李白,张子妍,张强,等.灰葡萄孢bZIP家族基因的全基因组鉴定与表达规律分析[J].农业生物技术学报,2022,30(4):762-771.
[3]ZHANG K,YUAN X M,ZANG J P,et al.The kynurenine 3-monooxygenase encoding gene, BcKMO, is involved in the growth, development, and pathogenicity of Botrytis cinerea[J].Front Microbiol,2018,9:1039.
[4]XIAO G L, ZHANG Q H, ZENG X G, et al.Deciphering the molecular signatures associated with resistance to Botrytis cinerea in strawberry flower by comparative and dynamic transcriptome analysis[J].Front Plant Sci,2022,13:888939.
[5]ZHANG H Y, GODANA E A, SUI Y, et al.Biological control as an alternative to synthetic fungicides for the management of grey and blue mould diseases oltable grapes:A review[J].Crit Rev Microbiol,2020,46(4):1-13.
[6]王方方,付清泉,史学伟,等.灰霉病致病机理及其防治措施研究进展[J].中国果菜,2024,44(1):47-53.
[7]ZHANG Y, LI X, SHEN F, et al.Characterization of Botrytis cinerea isolates from grape vineyards in China[J].Plant Disease,2018, 102(1):40-48.
[8]夏蕾,杨大海,孙浩翔,等.卡伍尔链霉菌拮抗灰葡萄孢菌最佳发酵条件研究[J].东北农业科学,2024,49(5):41-45.
[9]张晓云,王雪美,丛蓉,等.防治葡萄灰霉病的贝莱斯芽胞杆菌HMB28023筛选及其抑菌物质[J].中国生物防治学报,2025,41(1):122-131.
[10]HU D,MAENO N,MINAMI N,et al.Antifungal activities of vineyardhabitat wild yeast for grape gray-mold disease and its effects on spontaneous winemaking[J].Anton Leeuw,2024,117(1):27-40.
[11]李素平,袁玲,迟少艺,等.一种自溶性产酶溶杆菌新菌株LE16对温室番茄灰霉病的抑制作用[J].微生物学报,2022,62(10):3871-3885.
[12]刘小玉,付登强.解淀粉芽胞杆菌在农业生产中的应用[J].中国果菜,2022,42(8):81-84.
[13]赵月盈.解淀粉芽胞杆菌抗病机制研究进展[J].亚热带农业研究,2021,17(3):205-210.
[14]金伟伟,贾振华,宋水山.芽胞杆菌产生的脂肽类抗生素的结构和应用[J].微生物学杂志,2017,37(3):122-127.
[15]杨蕊,石红利,郎剑锋,等.解淀粉芽孢杆菌PB-1对灰葡萄孢的抑菌机理[J].江苏农业科学,2024,52(16):149-155.
[16]WOLDEMARIAM YOHANNES K,WAN Z,et al.Prebiotic,probiotic,antimicrobial,and functional food applications of Bacillus amyloliquefaciens[J].J Agr Food Chem,2020,68(50):14709-14727.
[17]崔皓玥,田露,胡乐梅,等.解淀粉芽孢杆菌wxy-b3产脂肽类物质对苹果斑点落叶病菌的抑菌活性研究[J].陕西科技大学学报,2025,43(1):46-51.
[18]廖凤平,李昆太,谭明辉,等.脂肽产生菌解淀粉芽孢杆菌HY2-1的发酵条件优化[J].中国酿造,2024,43(7):209-214.
[19]李扬凡,邵美琪,刘畅,等.解淀粉芽孢杆菌HMB33604的抑菌物质及对马铃薯黑痣病的防治效果[J].中国农业科学,2021,54(12):2559-2569.
[20]王楠,廖永琴,申云鑫,等.酸模根际解淀粉芽胞杆菌SH-53发酵条件优化及其生防作用[J].植物保护学报,2024,51(4):817-829.
[21]朱海云,马瑜,柯杨,等.抗猕猴桃细菌性溃疡病蜡样芽胞杆菌MA23培养基及发酵条件优化[J].中国农学通报,2021,37(7):112-118.
[22]YAZID H, BOUZID T, EL MOUCHTARI E M, et al.Insights into the adsorption of Cr(VI) on activated carbon prepared from walnut shells:Combining response surface methodology with computational calculation[J].Clean Technol,2024,6(1):199-220.
[23]LI R F,WANG B,LIU S,et al.Optimization of the expression conditions of CGA-N46 in Bacillus subtilis DB1342(p-3N46)by response surface methodology[J].Interdiscip Sci,2016,8(3):277-283.
[24]郝林.食品微生物学实验技术[M].北京:中国农业出版社,2001:11-15.
[25]单哲,李敬盼,孙镇平,等.解淀粉芽孢杆菌液体发酵动态变化规律的研究[J].饲料研究,2015(7):65-69.
[26]ZHANG S M,SHA C Q,WANG Y X,et al.Isolation and characterization of antifungal endophytic bacteria from soybean[J].Inst Microbiol,2008,35(10):1593-1599.
[27]孙长花,王征远,刘俊,等.八角茴香提取液的抑菌效果及稳定性探讨[J].食品工业,2020,41(12):189-192.
[28]ZENG J S, TUNG H H, WANG G S.Effects of temperature and microorganism densities on disinfection by-product formation[J].Sci Total Environ,2021,794:148627.
[29]祝小霞,石慧敏,叶建仁.Bacillus megaterium ZS-3最佳发酵培养条件优化[J].微生物学杂志,2024,44(6):42-52.
[30]任涛,钮成拓,郑飞云,等.淀粉液化芽孢杆菌BS5582产蛋白酶的发酵条件优化、酶学性质分析及其在牛皮脱毛中的应用[J].食品与发酵工业,2024,50(22):106-114.
[31]徐海刚,刘佳慧,熊智.解淀粉芽孢杆菌产α-淀粉酶的培养基优化[J].食品安全导刊,2022(36):126-130.