鹿茸菇(Lyophyllum decastes)是一种食药兼用的名贵食用菌,富含蛋白质、β-葡聚糖、多种氨基酸和维生素,凭借其独特的口感和丰富的营养价值,成为我国广受欢迎的食用菌之一[1]。研究表明,长期食用鹿茸菇有助于滋补强身、增强免疫力、延缓衰老,还具有改善便秘、降低胆固醇、缓解糖尿病、抑制过敏和预防癌症等多种健康益处[2-3]。由于新鲜鹿茸菇极易腐烂,难以长期储存[4],因此迫切需要开发有效的保存方法。调味酱发酵是一种历史悠久且经济实用的食品保存方法,长期以来与民俗饮食文化密切相关[5]。发酵不仅能更好地保留原料中的营养物质,还能通过微生物代谢产生独特的风味物质,从而提升发酵酱的感官品质[6]。因此,研究鹿茸菇酱的加工工艺和品质特性,对于延长鹿茸菇保质期,丰富食用菌产品市场具有重要意义。
香辛料作为一种常见的调味料,不仅能提升食品的风味,还具备防腐抑菌作用,从而显著改善产品品质。吴宝珠等[7]研究发现,将大蒜、生姜和花椒添加到糍粑辣椒酱中,可以提高其有机酸和总酸含量,进而影响酱料的滋味特性。班雨函等[8]研究发现,在低盐虾酱中添加紫苏,可显著改变其微生物多样性和群落结构,降低挥发性盐基氮含量,并改善产品品质。陈洪生等[9]研究发现,在休闲酱卤猪手中添加丁香提取物,可显著降低细菌总数和硫代巴比妥酸值,同时增强蛋白质与水的结合作用,延长卤制品的保质期。丁香中富含丁香酚、乙酰丁香酚、丁香醛和石竹烯,这些成分可通过破坏细胞膜结构,有效抑制多种致病性微生物[10]。因此,香辛料有助于调味酱的品质改善和风味提升。
调味酱的腐败变质与其微生物数量和种类密切相关。由于自然界中大多数微生物无法在琼脂平板上培养,传统的纯培养方法难以快速、高效、准确地全面解析微生物群落结构,限制了调味酱微生物多样性研究的深入开展[11]。随着生物技术的不断发展,高通量测序技术近年来被广泛应用于发酵食品微生物群落多样性的研究[12]。目前,对鹿茸菇酱的研究大多集中于加工工艺和新型产品开发,而对其微生物群落的研究较少,尤其是关于添加香辛料的鹿茸菇酱中细菌群落多样性的研究尚鲜见报道。本研究在鹿茸菇酱制备过程中分别添加花椒、紫苏和丁香三种香辛料,采用高通量测序技术及理化分析,比较其细菌群落结构和理化特性的差异,揭示微生物与理化特性的关系,旨在为提升鹿茸菇酱品质提供数据支持。
1 材料与方法
1.1 材料与试剂
鹿茸菇:本地农贸市场;花椒、紫苏、丁香:亳州市孙思邈生物科技有限公司;豆瓣酱:郫县恒星调味品有限公司。
氢氧化钠、甲醛、无水乙醇、异丙醇、石油醚、乙醚、乙酸、三氯甲烷、碘化钾、硫代硫酸钠(均为分析纯):国药集团化学试剂有限公司;![]() 脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:美国Mpbio公司;16S核糖体核糖核酸(ribosomal ribonucleic acid,rRNA)V3-V4引物(338F:5'-ACTCCTACGGGAGGCAGCA-3'和806R:5'-GGACTACHVGGGTWTCTAAT-3'):北京睿博兴科生物技术有限公司。
脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:美国Mpbio公司;16S核糖体核糖核酸(ribosomal ribonucleic acid,rRNA)V3-V4引物(338F:5'-ACTCCTACGGGAGGCAGCA-3'和806R:5'-GGACTACHVGGGTWTCTAAT-3'):北京睿博兴科生物技术有限公司。
1.2 仪器与设备
FE28型pH计、XPR105DR/AC型电子天平:瑞士梅特勒托利多公司;LC-MSB-S型磁力搅拌器、HH-420型恒温数显水浴锅:上海力辰仪器科技有限公司;DHG-9140型恒温鼓风干燥箱:上海一恒科学仪器有限公司;TG16-WS型台式高速离心机:湖南湘仪实验室仪器开发有限公司;R-3001型旋转蒸发仪:郑州长城科工贸有限公司;HM-CWF1型超微量分光光度计:山东恒美电子科技有限公司;Illumina Miseq测序仪:美国Illumina公司。
1.3 方法
1.3.1 鹿茸菇酱制备
将花椒、紫苏、丁香置于恒温鼓风干燥箱105 ℃烘干1 h,粉碎机研磨5 min,过60目网筛,得到香辛料粉末,备用[8]。新鲜鹿茸菇,清水洗净表面杂质和灰尘,去蒂,挤干水分,切丁。称取150 g食用油,加入炒锅,油热后加入鹿茸菇丁,调至中火不断翻炒,待鹿茸菇中多余水分挥发后,加入鹿茸菇质量20%的豆瓣酱和适量清水,继续翻炒均匀至油分显现,晾凉后装瓶,用盖子封住瓶口,得到鹿茸菇酱[1]。置于25 ℃室温环境保存15 d,收集样品,用于微生物多样性分析和理化指标测定。
以上处理得到的鹿茸菇酱为对照组,花椒组、紫苏组和丁香组分别为对照组中添加4%的花椒粉、紫苏粉和丁香粉。
1.3.2 理化指标测定
pH的测定:称取2 g鹿茸菇酱,加入6 mL去离子水,混匀后静置15 min,用pH直接进行测定;氨基酸态氮的测定:参照国标GB 5009.235—2016《食品安全国家标准 食品中氨基酸态氮的测定》进行测定;酸价的测定:参照国标GB 5009.229—2025《食品安全国家标准 食品中酸价的测定》进行测定;过氧化值的测定:参照国标GB 5009.227—2023《食品安全国家标准食品中过氧化值的测定》进行测定。
1.3.3 DNA提取及高通量测序
参照![]() DNA提取试剂盒中说明书要求对鹿茸菇酱样品中微生物总DNA进行提取,分别采用超微量分光光度计和1%琼脂糖凝胶电泳测定DNA的浓度和完整性[13],利用16S rRNA V3-V4引物对微生物进行聚合酶链式反应(polymerasechainreaction,PCR)扩增,PCR扩增体系(20μL):5×FastPfu缓冲液4 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)(2.5 mmol/L)2 μL,上下游引物(5 μmol/L)各1 μL,DNA聚合酶1 μL,DNA模板(10 ng)1 μL,双蒸水(ddH2O)10 μL[14-15];PCR扩增条件为:95 ℃预变性3 min,95 ℃变性30 s,55 ℃退火20 s,72 ℃延伸30 s,30次循环[14-15]。利用2%琼脂糖凝胶电泳检测扩增结果,切胶回收扩增产物,寄至北京睿博兴科生物技术有限公司,并委托采用Illumina Miseq PE250平台进行高通量测序。
DNA提取试剂盒中说明书要求对鹿茸菇酱样品中微生物总DNA进行提取,分别采用超微量分光光度计和1%琼脂糖凝胶电泳测定DNA的浓度和完整性[13],利用16S rRNA V3-V4引物对微生物进行聚合酶链式反应(polymerasechainreaction,PCR)扩增,PCR扩增体系(20μL):5×FastPfu缓冲液4 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)(2.5 mmol/L)2 μL,上下游引物(5 μmol/L)各1 μL,DNA聚合酶1 μL,DNA模板(10 ng)1 μL,双蒸水(ddH2O)10 μL[14-15];PCR扩增条件为:95 ℃预变性3 min,95 ℃变性30 s,55 ℃退火20 s,72 ℃延伸30 s,30次循环[14-15]。利用2%琼脂糖凝胶电泳检测扩增结果,切胶回收扩增产物,寄至北京睿博兴科生物技术有限公司,并委托采用Illumina Miseq PE250平台进行高通量测序。
1.3.4 高通量测序序列分析
采用Qiime2[16]生信分析软件处理高通量测序数据,具体如下:使用Trimmomatic插件对原始序列进行解复用、条形码识别和长度过滤,得到优质序列,利用DADA2插件切除测序引物片段,并进行双端序列拼接,除去嵌合体,获得扩增子序列变体(amplicon sequence variants,ASV),选取序列相似度为97%的代表性序列,使用Silva 138数据库对代表性序列进行分类学注释,将注释为叶绿体和不能注释为门水平的ASV删除[15]。
1.3.5 数据处理
每个指标重复测定3次,结果以“平均值±标准差”形式表示;采用GraphPad Prism8.0软件绘制图形;使用SPSS 19.0软件对数据进行单因素方差分析(analysis of variance,ANOVA)和Kruskal-Wallis秩和检验分析,P<0.05表示差异显著;利用R 4.0.1软件计算微生物多样性,对微生物群落进行主坐标分析(principal co-ordinates analysis,PCoA)、聚类分析(clustering analysis,CA)、冗余分析(redundancy analysis,RDA)和方差分解分析(variance partitioning analysis,VPA)。
2 结果与分析
2.1 鹿茸菇酱理化特性分析
不同香辛料对鹿茸菇酱pH值和氨基酸态氮含量的影响见图1,对酸价和过氧化值的影响见图2。由图1可知,4种鹿茸菇酱的pH值存在显著差异(P<0.05),添加花椒组(4.62)、紫苏组(4.77)和丁香组(4.55)的pH值均显著低于对照组(4.88)(P<0.05)。鹿茸菇富含可溶性多糖,在微生物作用下被分解为乳酸和乙酸等酸性物质,从而导致pH值下降[17]。然而,香辛料的添加可能激活某些产酸微生物的活性,从而增加酸性物质的生成,导致香辛料组的pH值低于对照组[8]。花椒、紫苏和丁香中的花椒素、紫苏醛和丁香酚等活性物质能抑制有害微生物的生长,防止食品腐败变质[18]。与对照组相比,花椒、紫苏和丁香的添加显著提高了鹿茸菇酱中氨基酸态氮含量,增幅分别为33.33%、9.52%和14.29%。花椒、紫苏和丁香的活性物质通过抑制腐败菌代谢,防止氨基酸态氮分解为氨类和挥发性氮类化合物,从而维持鹿茸菇酱的品质稳定[19]。因此,香辛料的添加可改善鹿茸菇酱的品质特征,但其效果因香辛料种类而异。
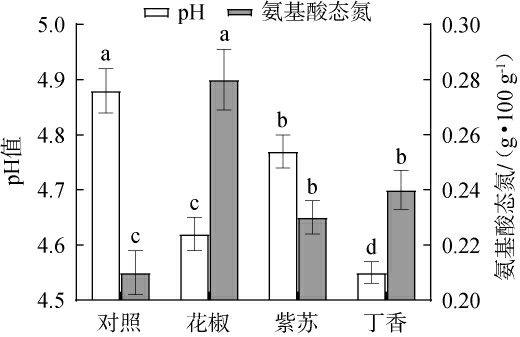
图1 不同香辛料对鹿茸菇酱pH值和氨基酸态氮含量的影响
Fig.1 Effect of different spices on pH values and amino acid nitrogen contents of Lyophyllum decastes sauce
不同小写字母表示差异显著(P<0.05)。下同。
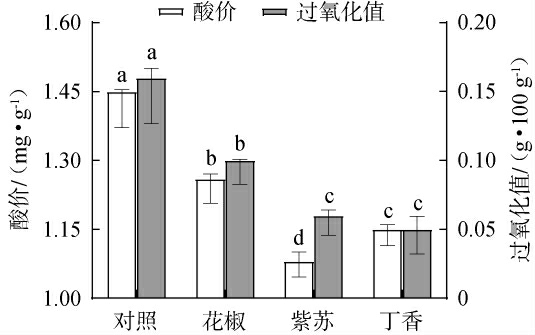
图2 不同香辛料对鹿茸菇酱酸价和过氧化值的影响
Fig.2 Effect of different spices on acid values and peroxide values of Lyophyllum decastes sauce
由图2可知,4种鹿茸菇酱的酸价存在显著差异(P<0.05),且均低于限量值(≤3 mg/g)。添加花椒、紫苏和丁香显著降低了鹿茸菇酱的酸价,降幅分别为13.11%、25.52%和20.69%(P<0.05)。香辛料中的黄酮和多酚类抗氧化物质可延缓鹿茸菇的脂肪氧化,保持产品品质并延长保质期[19]。此外,香辛料中的挥发性精油具有广谱抗菌活性,可抑制腐败菌生长,从而控制酸价升高[20]。4种鹿茸菇酱的过氧化值变化趋势与酸价一致,且均低于限量值(≤0.50 g/100 g)。花椒组(0.10 g/100 g)、紫苏组(0.06 g/100 g)和丁香组(0.05 g/100 g)的过氧化值均显著低于对照组(0.16 g/100 g)。香辛料中的活性物质通过抑制脂肪酶和过氧化物酶活性,减缓过氧化物生成[21]。香辛料中的挥发性成分可能在酱表面形成气相屏障,减少氧气与基质接触,从而抑制脂质氧化,维持品质稳定并延长货架期[19]。因此,添加香辛料能有效抑制脂肪分解与氧化反应,减缓酸价和过氧化值的上升,从而提升鹿茸菇酱的品质稳定性。
2.2 细菌群落多样性分析
2.2.1 α多样性分析
以未添加香辛料鹿茸菇酱为对照,不同香辛料对鹿茸菇酱细菌测序数据和α多样性的影响见表1。
表1 不同香辛料对鹿茸菇酱细菌α多样性的影响
Table 1 Effect of different spices on bacterial α-diversity of Lyophyllum decastes sauce
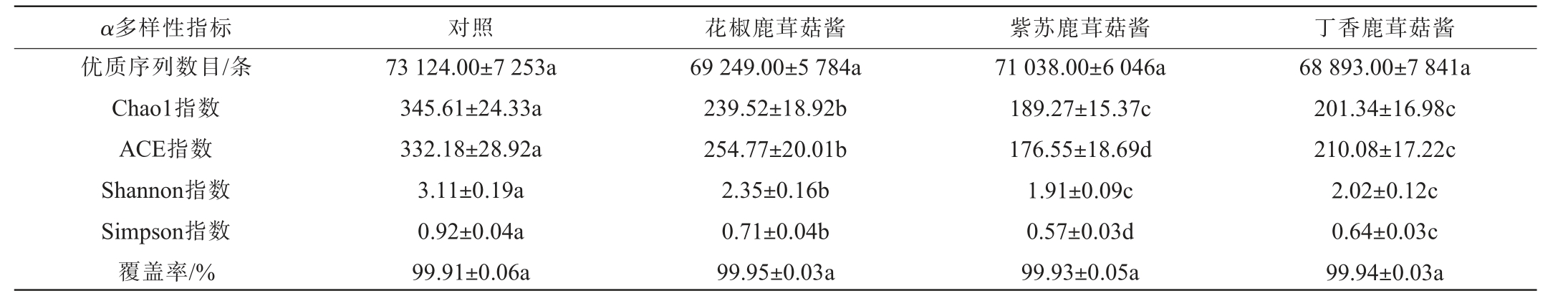
注:同行不同小写字母表示差异显著(P<0.05)。
α多样性指标 对照 花椒鹿茸菇酱 紫苏鹿茸菇酱 丁香鹿茸菇酱优质序列数目/条Chao1指数ACE指数Shannon指数Simpson指数覆盖率/%73 124.00±7 253a 345.61±24.33a 332.18±28.92a 3.11±0.19a 0.92±0.04a 99.91±0.06a 69 249.00±5 784a 239.52±18.92b 254.77±20.01b 2.35±0.16b 0.71±0.04b 99.95±0.03a 71 038.00±6 046a 189.27±15.37c 176.55±18.69d 1.91±0.09c 0.57±0.03d 99.93±0.05a 68 893.00±7 841a 201.34±16.98c 210.08±17.22c 2.02±0.12c 0.64±0.03c 99.94±0.03a
由表1可知,各鹿茸菇酱样品的优质序列数目在68 893~73 124条之间,样品间无统计学差异(P>0.05)。4种鹿茸菇酱的细菌群落覆盖率在99.91%~99.95%之间,表明测序深度充足可靠,可覆盖鹿茸菇酱中的绝大多数微生物,满足后续分析需求[15]。α多样性关注特定生境下的物种数量。通过Chao1指数、ACE指数、Shannon指数和Simpson指数进行α多样性分析,其中Chao1指数越大反映样品物种数越多,ACE指数越大反映物种丰富度越高,Shannon指数和Simpson指数用于衡量物种多样性,前者值越大多样性越高,后者则相反[8]。对照组鹿茸菇酱的Chao1指数和ACE指数分别为345.61和332.18,显著高于添加不同香辛料的各组(P<0.05),表明香辛料的添加抑制了鹿茸菇酱中微生物的生长繁殖。紫苏组鹿茸菇酱的Chao1指数和ACE指数均最低,分别为189.27和176.55,表明紫苏对鹿茸菇酱的抑菌效果要优于花椒和丁香。紫苏含有紫苏醛、紫苏酮和紫苏醇等活性物质,可通过破坏微生物细胞壁和细胞膜完整性实现抑菌作用[22]。花椒组(2.35)、紫苏组(1.91)和丁香组(2.02)的Shannon指数显著低于对照组(3.11)(P<0.05),而对照组的Simpson指数显著高于各香辛料组,说明降低了鹿茸菇酱的物种多样性,其活性物质能有效抑制有害微生物的生长繁殖[18]。综上可知,香辛料的添加会降低鹿茸菇酱细菌群落的丰富度和多样性。
2.2.2 β多样性分析
基于布雷柯蒂斯距离对ASV数据进行PCoA分析,探讨不同香辛料对鹿茸菇酱细菌群落组成的影响,结果见图3。
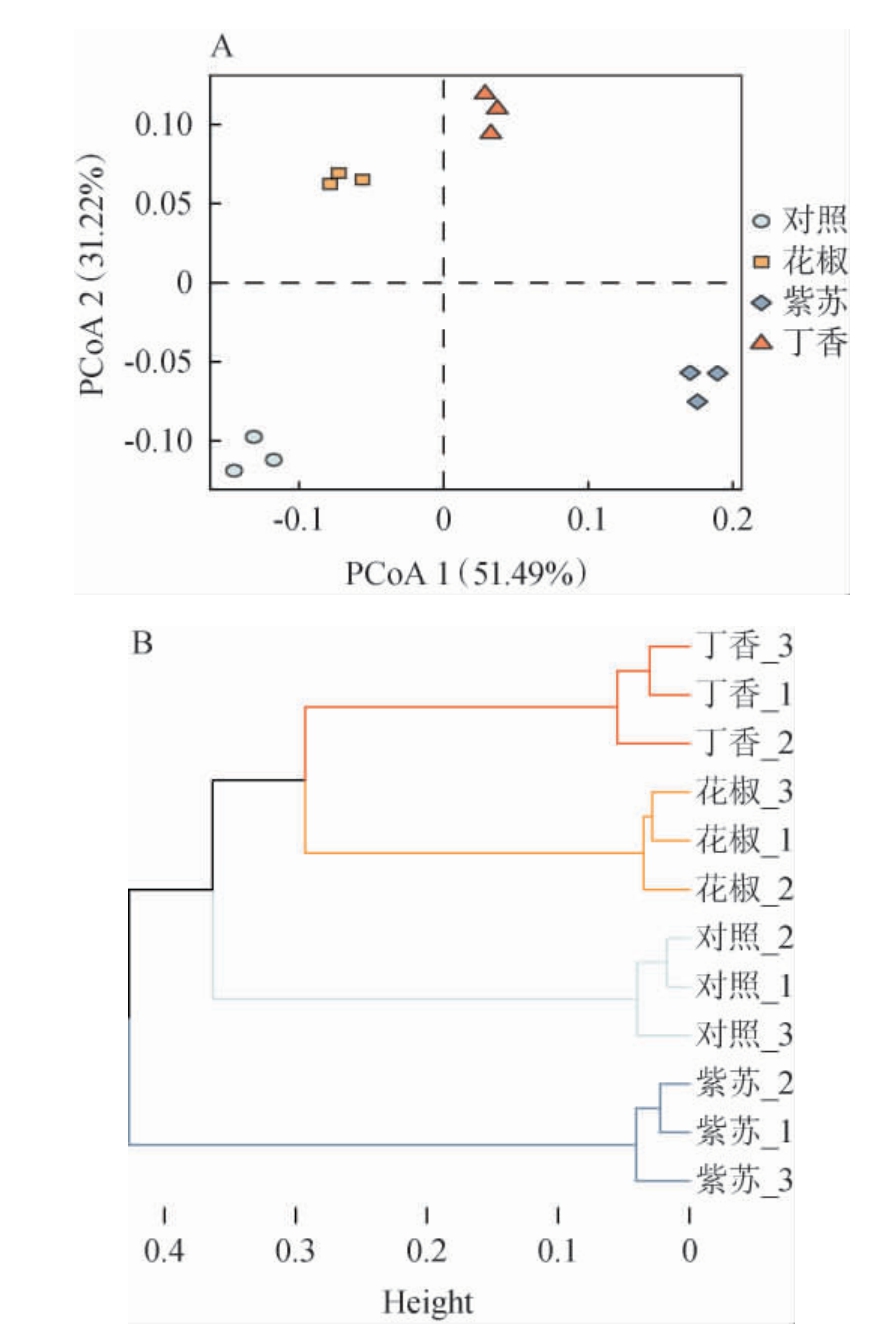
图3 基于扩增子序列变体不同香辛料鹿茸菇酱的主坐标分析(A)及聚类分析(B)
Fig.3 Principal coordinate analysis (A) and clustering analysis (B) of Lyophyllum decastes sauce with different spices based on amplicon sequence variants
由图3A可知,PCoA第一轴解释了51.49%的物种方差变异,第二轴解释了31.22%,累计解释率达82.71%,表明PCoA前两轴能较好地反映鹿茸菇酱细菌群落组成的差异。4种鹿茸菇酱样品分别位于坐标轴的不同象限,明显区分开,表明添加不同香辛料显著影响其细菌群落组成。这与班雨函等[8]研究结果相一致。由图3B可知,根据细菌群落组成的相似性,可明显区分4种鹿茸菇酱样品,且组间差异大于组内差异,表明相同制作工艺下,鹿茸菇酱细菌群落组成具有一定相似性。总体而言,添加香辛料显著改变了鹿茸菇酱的细菌群落组成,不同香辛料的影响存在差异。
2.3 细菌群落结构差异
对4种鹿茸菇酱样品进行了细菌分类鉴定,结果见图4。由图4可知,共检测出3个优势菌门,分别为厚壁菌门(Fir micutes)、变形菌门(Proteobacteria)和放线菌门(Actinobacteria)。厚壁菌门和变形菌门的相对丰度之和在4种鹿茸菇酱中均超过98%,占据绝对优势。花椒组(86.69%)、紫苏组(88.67%)和丁香组(93.74%)中厚壁菌门平均相对丰度均高于对照组(78.87%),而对照组鹿茸菇酱的变形菌门平均相对丰度则高于各不同香辛料组,表明香辛料的添加通过改变厚壁菌门与变形菌门的比例,显著影响了鹿茸菇酱的细菌群落结构,从而引起多样性差异。
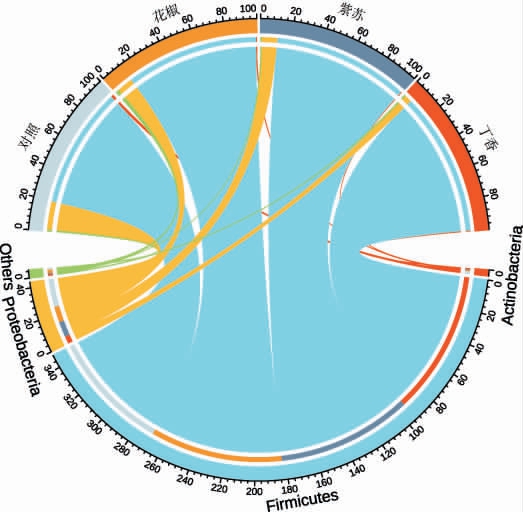
图4 不同香辛料对鹿茸菇酱门水平细菌群落的影响
Fig.4 Effect of different spices on bacterial community of Lyophyllum decastes sauce at the phylum level
为进一步阐明不同香辛料对鹿茸菇酱细菌群落的影响,基于属水平对鹿茸菇酱细菌群落进行了探究,结果见图5。
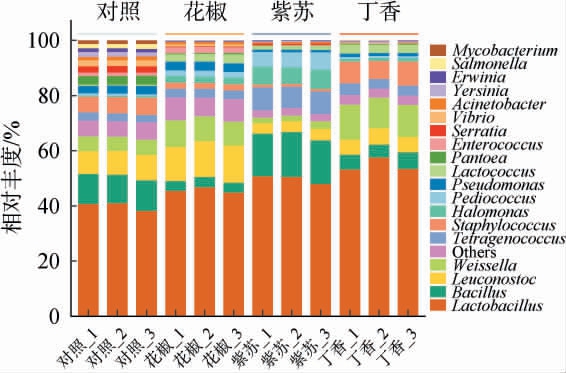
图5 不同香辛料对鹿茸菇酱属水平细菌群落的影响
Fig.5 Effect of different spices on bacterial community of Lyophyllum decastes sauce at the genus level
由图5可知,鹿茸菇酱中相对丰度较高的是乳酸杆菌属(Lactobacillus)、芽孢杆菌属(Bacillus)、明串珠菌属(Leuconostoc)和魏斯氏菌属(Weissella),其相对丰度之和为63.99%~79.18%。乳酸杆菌属是鹿茸菇酱中占比最高的微生物,在对照组中,其平均相对丰度最低,仅为39.86%;而在花椒组、紫苏组和丁香组中分别可达45.59%、49.67%和54.64%,表明香辛料的加入促进了乳酸杆菌属的生长繁殖。香辛料中的多酚类物质和挥发油成分可能促进乳酸杆菌属的生长,增强其代谢活性[8]。此外,乳酸杆菌属能够将鹿茸菇中的可溶性多糖和蛋白转化为酸类物质、短肽和氨基酸,为产品赋予柔和的酸感和独特的鲜味[17,23]。对照组中,芽孢杆菌属的平均相对丰度为10.81%,而花椒组和丁香组分别为3.69%和5.41%,表明花椒和丁香的添加抑制了芽孢杆菌属的增殖。紫苏组鹿茸菇酱中芽孢杆菌属的平均相对丰度可达15.87%,这是由于紫苏富含蛋白质、氨基酸和矿物质等营养成分,为芽孢杆菌属的提供了丰富的营养源和必要的生长因子,从而促进了其增殖[22]。芽孢杆菌属能够产生胞外水解酶、强效抗真菌脂肽和胞外聚合物,从而抑制腐败菌的生长,保持鹿茸菇酱的品质稳定[24]。对照组鹿茸菇酱中明串珠菌属和魏斯氏菌属的平均相对丰度分别为8.62%和5.47%,显著低于花椒组(12.85%和9.13%)(P<0.05),这与SONG H S等[24]研究结果相一致,其发现在泡菜发酵过程中加入花椒、生姜、大蒜等香辛料可促进明串珠菌属和魏斯氏菌属的增殖,促进泡菜成熟[24]。在紫苏组中,明串珠菌属和魏斯氏菌属的平均相对丰度分别仅为3.85%和2.35%;相比之下,丁香组中明串珠菌属和魏斯氏菌属的平均相对丰度分别为5.63%和11.78%。明串珠菌属、魏斯氏菌属和芽孢杆菌属均具有耐盐特征,能够代谢碳水化合物以获取能量支持生长繁殖[25],但三者之间存在竞争关系。明串珠菌属、魏斯氏菌属和芽孢杆菌属与乳酸杆菌属存在共生关系,前者合成的葡萄聚糖和异麦芽低聚糖等低聚糖可促进乳酸杆菌属的增殖,使其成为鹿茸菇酱中丰度最高的优势菌。乳酸杆菌属产生的酸性代谢物质则抑制不耐酸腐败菌的生长,减少对原料营养的竞争[25]。此外,弧菌属(Vibrio)、不动杆菌属(Acinetobacter)、耶尔森菌属(Yersinia)、欧文氏菌属(Erwinia)和沙门氏菌属(Salmonella)等腐败变质致病菌只少量存在于对照组,而添加不同香辛料组几乎检测不到,表明香辛料的添加可通过抑制腐败致病菌的生长繁殖,保持鹿茸菇酱品质稳定,从而延长货架期。香辛料富含天然活性物质,具有显著的抑菌效果,尤其是在抑制致病菌方面表现突出[20-21]。综上,香辛料对鹿茸菇酱的细菌群落结构组成具有选择性影响。
2.4 理化因子与细菌群落相关性分析
为揭示鹿茸菇酱理化因子与细菌群落的相关性,采用RDA方法分析理化因子与相对丰度排名前10的主要优势属之间的关系,当两个向量夹角为锐角时,表示正相关;为钝角时,表示负相关[15],鹿茸菇酱细菌群落与理化因子的冗余分析结果见图6。
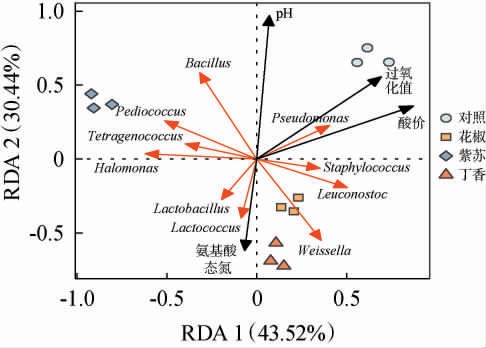
图6 鹿茸菇酱细菌群落与理化因子的冗余分析
Fig.6 Redundancy analysis between bacterial communities and physicochemical factors of Lyophyllum decastes sauce
由图6可知,RDA1和RDA2轴分别解释了理化因子对鹿茸菇酱细菌群落贡献度的43.52%和30.44%,累计解释贡献度达73.96%,表明RDA前两轴能较好地区分4种鹿茸菇酱的细菌群落差异。对照组细菌群落与过氧化值和酸价呈正相关,而花椒组和丁香组细菌群落则与氨基酸态氮含量呈正相关,但与pH值呈负相关。此外,过氧化值和酸价与假单胞菌属(Pseudomonas)、葡萄球菌属(Staphylococcus)和明串珠菌属呈正相关,但与芽孢杆菌属、片球菌属(Pediococcus)、四联球菌属(Tetragenococcus)、盐单胞菌属(Halomonas)、乳球菌属(Lactococcus)和乳酸杆菌属呈负相关;而氨基酸态氮含量则与乳酸杆菌属、乳球菌属、魏斯氏菌属和明串珠菌属呈正相关,但与芽孢杆菌属、片球菌属、四联球菌属和假单胞菌属呈负相关。条件限制分析显示,不同理化因子对鹿茸菇酱细菌群落的影响程度存在差异,其中pH值对细菌群落的影响最大(32.41%),其次分别为酸价(25.49%)、过氧化值(23.94%)和氨基酸态氮含量(18.16%)。这表明多个理化因子共同驱动鹿茸菇酱细菌群落的变化,同时反映出不同香辛料的影响存在显著差异。
为探究理化因子和细菌多样性对细菌群落结构的影响,本研究将理化因子视为非生物因素,细菌多样性指标视为生物因素,基于VPA阐明理化因子和细菌多样性对鹿茸菇酱细菌群落结构变异的贡献[26],结果见图7。由图7可知,非生物因素和生物因素共同解释鹿茸菇酱细菌群落结构57.1%的变异,而非生物因素能单独解释鹿茸菇酱细菌群落结构11.5%的变异,显著高于生物因素(6.8%),表明非生物因素是影响4种鹿茸菇酱细菌群落结构差异的主要驱动因素。此外,仍有24.6%的细菌群落结构变异未能通过上述指标解释,表明存在其他因素可能影响鹿茸菇酱的细菌群落结构。
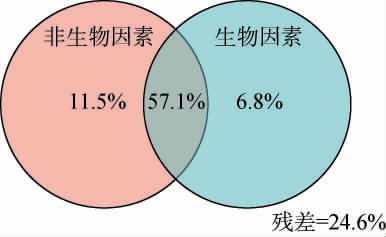
图7 鹿茸菇酱细菌群落与生物因素、非生物因素的方差分解分析
Fig.7 Variance partitioning analysis between bacterial communities and the biotic, abiotic factors of Lyophyllum decastes sauce
3 结论
本研究采用16S rRNA高通量测序技术结合理化分析技术,探究不同香辛料对鹿茸菇酱细菌群落组成结构和理化特性的影响。结果表明,花椒、紫苏和丁香的添加显著降低了鹿茸菇酱的pH值(P<0.05),提高了氨基酸态氮含量。与对照组相比,花椒、紫苏和丁香的添加使鹿茸菇酱的酸价分别降低了13.11%、25.52%和20.69%,过氧化值分别降低了37.50%、62.50%和68.75%。花椒、紫苏和丁香的添加使鹿茸菇酱的细菌多样性降低,导致细菌群落结构组成发生明显变化,尤其是促进了厚壁菌门的相对丰度。在属水平,乳酸杆菌属是鹿茸菇酱中占比最多的微生物,其相对丰度范围为39.86%~54.64%,花椒、紫苏和丁香的添加使乳酸杆菌属的相对丰度分别增加了14.38%、24.61%和37.08%。此外,RDA结果表明,乳杆菌属与氨基酸态氮含量呈正相关,与pH值、过氧化值和酸价呈负相关,且pH值对鹿茸菇酱细菌群落的影响最大。VPA结果表明,非生物因素是影响鹿茸菇酱细菌群落结构差异的主要驱动因素。综上所述,花椒、紫苏和丁香的添加能通过改变细菌群落组成结构,改善鹿茸菇酱的安全性。本研究有助于了解香辛料对鹿茸菇酱微生物组成的影响,为改善鹿茸菇酱的品质和安全提供理论基础。
[1]刘美仑,张心怡,王雨寒,等.香辣鹿茸菇调味酱的工艺及配方优化[J].农产品加工,2023(8):44-47.
[2]BRENNAN M A,DERBYSHIRE E,TIWARI B K,et al.Enrichment of extruded snack products with coproducts from chestnut mushroom(Agro-cybe aegerita) production: Interactions between dietary fiber, physicochemical characteristics,and glycemic load[J].J Agr Food Chem,2012,60(17):4396-4401.
[3]付林.鹿茸菇生态学特性与液体菌种配方的优化研究[J].中国食品,2023(6):129-131.
[4]胡宇欣,林海潞,林晓彤,等.超声处理对鹿茸菇贮藏品质的影响[J].食品科学,2023,44(3):186-193.
[5]ZHAO S,HAO C,NIU C,et al.Insight into the keystones of Chinese broad bean paste fermentation:Brewing techniques,chemosensory characteristics,and microbial community[J].Trend Food Sci Tech,2024,154:104775.
[6]ALAM H,KAUR J,SHARMA S.Impact of Lactobacillus rhamnosus GG fermentation on shelf life of Volvariella volvacea paste[J].Acta Alimentaria,2024,53(4):624-634.
[7]吴宝珠,乔明锋,邓静,等.3种香辛料对糍粑辣椒发酵过程中有机酸的影响研究[J].中国调味品,2024,49(1):59-66.
[8]班雨函,杨兵兵,马爱进,等.不同香辛料对低盐虾酱中微生物群落和理化性质的影响[J].食品科学,2023,44(8):143-151.
[9]陈洪生,潘德胤,马金明,等.丁香提取物对休闲酱卤猪手贮藏期间品质变化的影响[J].食品工业科技,2021,42(24):299-305.
[10]LIÑÁN-ATERO R,AGHABABAEI F,GARCÍA S R,et al.Clove essential oil: Chemical profile,biological activities, encapsulation strategies,and food applications[J].Antioxidants,2024,13(4):488-497.
[11]胡梓晴,刘晓艳,白卫东,等.高通量测序技术在白酒微生物多样性中的研究进展[J].中国酿造,2023,42(5):15-21.
[12]WEN L,YANG L,CHEN C,et al.Applications of multi-omics techniques to unravel the fermentation process and the flavor formation mechanism in fermented foods[J].Crit Rev Food Sci Nutr,2024,64(23):8367-8383.
[13]张睿艺,谢辽辽,田星.辣椒品种对发酵辣椒酱真菌多样性及其理化指标的影响[J].食品科技,2024,49(1):282-289.
[14]全昌彬,姚玉仙,莫光友,等.贵州黔东南侗族不同酸化程度腌鱼的微生物多样性分析[J].食品科技,2024,49(1):121-128.
[15]唐艳平,高秀兵,倪婕,等.白酒发酵副产物黄水原核微生物组成及理化特性研究[J].中国酿造,2024,43(3):72-78.
[16]BOLYEN E,RIDEOUT J R,DILLON M R,et al.Reproducible,interactive,scalable and extensible microbiome data science using QIIME 2[J].Nat Biotechnol,2019,37(8):852-857.
[17]GUO Q, PENG J, ZHAO J, et al.Correlation between microbial communities and volatile flavor compounds in the fermentation of Semen sojae praeparatum[J].LWT-Food Sci Technol,2024,198:116009.
[18]李磊,崔丽伟,张冉,等.3种香辛料精油在牛排涂膜保鲜中的应用研究[J].食品科技,2019,44(2):138-142,151.
[19]ELIZABETH D L T J,GASSARA F,KOUASSI A P,et al.Spice use in food:Properties and benefits[J].Crit Rev Food Sci Nutr,2017,57(6):1078-1088.
[20]LI Y, ERHUNMWUNSEE F, LIU M, et al.Antimicrobial mechanisms of spice essential oils and application in food industry[J].Food Chem,2022,382:132312.
[21]ZHANG J, ZHANG M, BHANDARI B, et al.Basic sensory properties of essential oils from aromatic plants and their applications: A critical review[J].Crit Rev Food Sci Nutr,2024,64(20):6990-7003.
[22]李紫薇,车萍,张颖颖,等.紫苏化学成分及药理作用研究进展[J].山东化工,2024,53(3):111-114.
[23]杨希,武爱群.酸菜发酵过程中理化因子及原核微生物群落结构差异分析[J].食品与发酵工业,2020,46(22):245-251.
[24]SONG H S,WHON T W,KIM J,et al.Microbial niches in raw ingredients determine microbial community assembly during kimchi fermentation[J].Food Chem,2020,318:126481.
[25]孙筱.盐浓度对自制香肠理化因子及原核微生物群落多样性的影响[J].中国酿造,2021,40(9):145-149.
[26]XIONG S,XU X,DU T,et al.Organic acids drove the microbiota succession and consequently altered the flavor quality of Laotan Suancai across fermentation rounds: Insights from the microbiome and metabolome[J].Food Chem,2024,450:139335.