酱香型白酒作为中国传统蒸馏酒的典型代表,其生产过程中产生的副产物丢糟具有显著的资源属性与环境属性矛盾。2022年,茅台集团茅台酒产量约57 800 t,有力推动行业发展[1]。然而,酒业迅猛发展的同时,丢糟产量也随之激增,白酒与丢糟产量比约1∶4[2]。丢糟虽富含营养物质,却因酸度高、含水量大,易腐败霉变,造成二次环境污染[3]。在“双碳”目标引领下,丢糟资源的高效利用,成为白酒产业绿色发展的关键。
抗性淀粉(resistant starch,RS)作为新型功能性碳水化合物,不仅能促进肠道健康,预防疾病[4],最新研究发现其有助于减轻体质量、改善胰岛素抵抗[5-6]。RS分为四类:RS1(包埋淀粉)、RS2(抗性淀粉颗粒)、RS3(老化回生淀粉)和RS4(化学改性淀粉)[7],其中RS3因来源广泛、易制备等特点备受关注。目前国内外对于抗性淀粉的研究尚处起步阶段[8]。在抗性淀粉制备方法上,常用物理法如压热[9]、微波法[10]等,但这些方法制备效率普遍偏低[11]。酶法中,普鲁兰脱支酶效果最佳,搭配压热法可显著提升抗性淀粉得率[12]。酱香型白酒丢糟淀粉结构复杂,经多轮发酵后结晶度降低[13],且含有阻碍抗性淀粉生成的物质[14],而且直链淀粉与支链淀粉的比例、结晶度及颗粒完整性是影响RS得率的关键因素[15]。尽管国内外学者已尝试从苦荞[16]、薯类等[17]多种物质中提取抗性淀粉作为食品增稠剂[18]、健康食品原料[19]等,但针对酱香型白酒丢糟抗性淀粉的研究相对匮乏,仍需不断深入。
本研究以酱香型白酒丢糟为原料,采用酶法与压热法相结合的复合工艺制备抗性淀粉。通过单因素及正交试验,探究淀粉乳含量、酶添加量、酶解时间和酶解温度对抗性淀粉得率的影响,确定最佳工艺参数,并对所得抗性淀粉的理化性质进行分析。该研究不仅能实现丢糟的高值化利用,助力白酒产业绿色转型,还为功能性食品开发提供优质原料,推动抗性淀粉在食品、医药等领域的广泛应用。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
酱香型白酒丢糟:贵州某酱香型酒厂。
1.1.2 试剂
氢氧化钠、氢氧化钾、磷酸氢二钠、氯化钾、氯化钠、3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)、酸性蛋白酶(3 U/mL)、普鲁兰酶(2 000 U/mL)、耐高温α-淀粉酶(20 000 U/mL)、葡萄糖淀粉酶(100 000 U/g)、胃蛋白酶(≥1 200 U/g)、胰蛋白酶(50 000 U/g):国药集团化学试剂有限公司;盐酸、亚硫酸钠:昆山金城试剂有限公司;无水乙醇:太仓沪试试剂有限公司;十二烷基硫酸钠(sodium dodecyl sulfate,SDS):中轻化工股份有限公司。以上试剂均为分析纯。
1.2 仪器与设备
UV2000型紫外可见分光光度计:湘仪仪器有限公司;RTC-2磁力搅拌器:郑州邦博仕仪器设备有限公司;JE2002电子天平:海浦春计量仪器有限公司;YY-20-J移液器:北京华美生科生物技术有限公司;DHG-9140A型电热恒温鼓风干燥箱:常州润华电器有限公司;YXQ-100A高压蒸汽灭菌锅:上海博讯实业有限公司。
1.3 方法
1.3.1 酱香型白酒丢糟抗性淀粉的制备[20]
(1)酱香型白酒丢糟淀粉的提取及条件优化
将酱香型白酒丢糟放入烘干机中110 ℃烘干至恒质量,粉碎后与蒸馏水按液料比1∶10(g∶mL)混合,40目筛过滤,以清除糠壳、高粱皮等杂质,多次水洗3 000 r/min离心20 min得到丢糟混合物,备用。随后采用碱法、酶法及SDS法提取淀粉,具体制备方法见表1。通过比较3种方法所得淀粉的纯度确定最佳的提取工艺。
表1 酱香型白酒丢糟制备抗性淀粉不同提取方法
Table 1 Different extraction methods for the preparation of resistant starch from the sauce-flavor Baijiu distiller's grains

方法 具体方法碱法制备淀粉[21]酶法制备淀粉[22]SDS法制备淀粉[23]用0.1%的NaOH溶液搅拌均匀浸泡5 d后更换浸泡液重复浸泡5 d,用稀盐酸中和后过滤,获得初步的淀粉溶液,收集干燥的丢糟淀粉测量其纯度。配制柠檬酸-柠檬酸钠缓冲液,调节pH=4,加入酸性蛋白酶处理5 d后,过滤。得到丢糟粗淀粉,多次离心洗涤淀粉,收集干燥的丢糟淀粉测量其纯度。配制1%十二烷基硫酸钠溶液,使用前加0.1%亚硫酸钠浸泡丢糟,均匀搅拌,处理12 h,多次更换浸泡溶液。过80目筛。离心洗涤淀粉,得到丢糟淀粉,收集干燥的丢糟淀粉测量其纯度。
(2)酱香型白酒丢糟抗性淀粉的制备
抗性淀粉的制备和纯化[20]:称取表1提取的丢糟淀粉(2.000 0±0.001 0)g,加入适量蒸馏水配制30%的淀粉乳溶液,将淀粉乳溶液置于高压蒸汽灭菌锅中115 ℃处理15 min,冷却至40℃,调节pH为4,加入20U/g普鲁兰酶,55℃酶解15h,取出样品冷却后于4 ℃冷藏12 h后取出,得到丢糟抗性淀粉溶液。利用浓度为0.1 mol/L的盐酸溶液和浓度为0.1 mol/L的氢氧化钠溶液调整丢糟抗性淀粉溶液的pH=5.5,加入耐高温α-淀粉酶1 mL,于90 ℃水浴1.5 h,后在沸水浴中处理10 min,利用95%的乙醇醇沉4 h,3 000 r/min离心15 min,沉淀用体积分数95%的乙醇洗涤,烘干粉碎后,过80目筛,得到丢糟抗性淀粉粉末。
(3)抗性淀粉含量测定
参考文献[24],选取7支刻度试管分别编号1~7,分别加入1 mg/mL的葡萄糖标准溶液0、0.2 mL、0.4 mL、0.6 mL、0.8mL、1.0 mL、1.2 mL和DNS试剂1.5 mL,加水定容到3.5 mL,混匀后放置在沸水锅中水浴5 min,取出后立即冷却,定容至25 mL,于波长540 nm处比色并记录吸光度值,绘制标准曲线,得到葡萄糖标准曲线的回归方程为y=1.463x+0.000 5,相关系数R2=0.999 3。称取(2.000 0±0.001 0)g(2)中粗提的丢糟抗性淀粉粉末于150 mL三角瓶中,添加HCI-KCI缓冲溶液,加入0.1 mL胃蛋白酶,55 ℃水浴1 h后取出调pH至5.4。加1%耐高温α-淀粉酶2 mL,90 ℃水浴1.5 h,冷却至室温后调pH至4.5,加0.01%葡萄糖淀粉酶l.5 mL,40 ℃水浴8 h,加入乙醇进行醇沉,3 000 r/min离心20 min,所得沉淀用体积分数80%乙醇洗涤,离心去除上清液,沉淀即为抗性淀粉。利用浓度为2 mol/LKOH使沉淀溶解,调pH至4.5,加0.01%葡萄糖淀粉酶1 mL,40 ℃恒温酶解45 min,在沸水浴中进行加热处理5 min,冷却,离心,然后利用100 mL容量瓶定容。用DNS法测定还原糖含量[25],根据公式(1)得抗性淀粉的得率。
式中:F为抗性淀粉得率,%;M为还原糖的质量,g;M0为丢糟淀粉质量,g。
1.3.2 酱香型白酒丢糟抗性淀粉制备工艺优化
(1)单因素试验:准确称取(2.000 0±0.001 0)g酱香型白酒丢糟,分别探究淀粉乳质量分数(10%、20%、30%、40%、50%)、普鲁兰酶添加量(10 U/g、20 U/g、30 U/g、40 U/g、50 U/g)、酶解温度(45 ℃、50 ℃、55 ℃、60 ℃、65 ℃)和酶解时间(6 h、9 h、12 h、15 h、18 h)对酱香型白酒丢糟抗性淀粉得率的影响,每个试验重复3次。
(2)正交试验:在单因素试验的基础上,以酱香型白酒丢糟抗性淀粉得率为评价指标,淀粉乳质量分数(A)、酶添加量(B)、酶解时间(C)、酶解温度(D)4个因素为自变量,采用SPSS Statistics 20.0软件设计4因素3水平正交试验,试验因素和水平设计见表2。
表2 抗性淀粉制备工艺优化正交试验因素与水平
Table 2 Factors and levels of orthogonal experiments for preparation process optimization of resistant starch

水平 A 淀粉乳质量分数/%B 酶添加量/(U·g-1)C 酶解温度/℃ D 酶解时间/h 1 2 3 25 30 35 15 20 25 50 55 60 11 12 13
1.3.3 酱香型白酒丢糟抗性淀粉理化指标测定
(1)酱香型白酒丢糟淀粉和抗性淀粉溶解度与膨胀度的测定
称取丢糟淀粉及丢糟抗性淀粉样品各(0.200±0.005)g,加入5 mL蒸馏水,分别在50 ℃、60 ℃、70 ℃、80 ℃、90 ℃水浴锅中水浴30 min,取出试管离心得沉淀,称量溶胀的淀粉或抗性淀粉质量。将上清液干燥至恒质量,称量溶解的淀粉或抗性淀粉质量。通过公式(2)和(3)计算膨胀度和溶解度[26]。

式中:M0为丢糟淀粉或抗性淀粉样品质量,g;M1为溶解后丢糟淀粉或抗性淀粉样品质量,g;M2为丢糟淀粉或抗性淀粉沉淀物质量,g。
(2)酱香型白酒丢糟淀粉和抗性淀粉体外模拟人工胃液和人工肠液消化试验
人工胃液的配制:准确称取8.0 mL稀盐酸,加入少量水,均匀搅拌,混匀后加入5 g胃蛋白酶,然后用容量瓶定容至500 mL。人工肠液的配制:准确称取胰蛋白酶5 g,磷酸二氢钾3.5 g,加入少量水,搅拌溶解,用1 mol/L氢氧化钠调节pH=6.5,加水定容至500 mL[27]。抗性淀粉体外消化试验方法见表3。通过公式(4)计算消化率。
表3 抗性淀粉体外消化试验方法
Table 3 Experimental methods for in vitro digestion of resistant starch

试管编号 抗性淀粉/g 人工胃液/mL 人工肠液/mL 水浴处理 测定1 2 3 0.200±0.005 0.200±0.005 0.200±0.005 5—5—5 5分别37 ℃恒温水浴0、30 min、60 min、120 min、180 min先在人工胃液中37 ℃恒温水浴120 min,后再在人工肠液中水浴60 min、100 min和200 min离心,蒸馏水清洗沉淀后,与上清液混合后定容至50 mL,测葡萄糖含量[28],计算消化率
式中:M0为葡萄糖质量,g;M1为丢糟淀粉或抗性淀粉质量,g。
1.3.4 数据处理
采用Excel 2019、SPSS Statistics 20.0和Origin 2021处理数据并绘图,所有试验均设置3组平行。
2 结果与分析
2.1 酱香型白酒丢糟淀粉提取条件优化
通过碱法、酶法和SDS法制得的丢糟淀粉纯度分别为48.26%、56.81%和50.31%,其中酶法制备丢糟淀粉的纯度最高,故后续试验采用酶法提取丢糟中的淀粉。
2.2 酱香型白酒丢糟抗性淀粉制备工艺条件优化单因素试验
2.2.1 淀粉乳质量分数对丢糟抗性淀粉得率的影响
由图1可知,随着淀粉乳质量分数的增加,RS得率呈先上升后下降的趋势。当淀粉乳质量分数为30%时,RS得率最高,为19.87%。淀粉乳质量分数<30%时,体系中淀粉质量分数较低,导致体系糊化分子较少,难以形成稳定的晶体结构[29]。当淀粉乳液质量分数过大,会导致反应体系缺乏水分,淀粉无法充分糊化,此时酶在体系中的活动受限,酶无法对所有支链淀粉脱支,同时直链淀粉分子的活动也会受阻,不利于RS的形成[30]。因此,确定最适淀粉乳质量分数为30%。
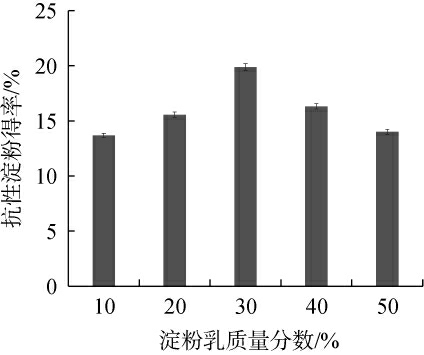
图1 淀粉乳质量分数对丢糟抗性淀粉得率的影响
Fig.1 Effect of starch milk mass concentration on the yield of resistant starch from distiller's grains
2.2.2 普鲁兰酶添加量对丢糟抗性淀粉得率的影响
由图2可知,随着普鲁兰酶添加量的增加,RS得率呈先上升后下降的趋势。当普鲁兰酶添加量为20%时,RS得率最高,为17.85%。当酶添加量<20 U/g时,酶解作用不充分,体系中难以生成更多的短链分子,导致抗性淀粉分子难以形成稳定的晶体结构,不利于RS的生成。当普鲁兰酶添加量>20 U/g时,酶水解了大量的淀粉分子,生成大量较短的直链分子,不利于双螺旋结构的接近,从而影响抗性淀粉的生成[31]。因此,确定最适普鲁兰酶添加量为20 U/g。
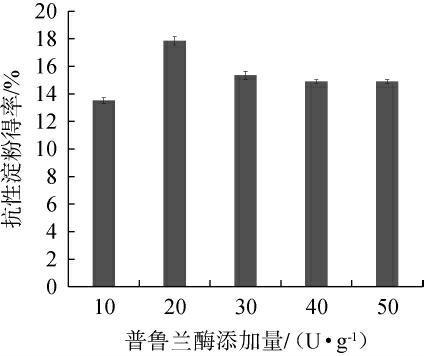
图2 普鲁兰酶添加量对丢糟抗性淀粉得率的影响
Fig.2 Effect of pullulanase addition on the yield of resistant starch from distiller's grains
2.2.3 酶解温度对丢糟抗性淀粉得率的影响
由图3可知,随着酶解温度的升高,RS得率呈先上升后下降的趋势。当酶解温度为55 ℃时,RS的得率最高,为18.95%,此温度能加速酶在体系中的脱支作用,促进抗性淀粉的生成。而当温度偏低或偏高时,酶的活性变弱,导致淀粉脱支程度不高,大大降低抗性淀粉的生成。因此,确定最适酶解温度为55 ℃。
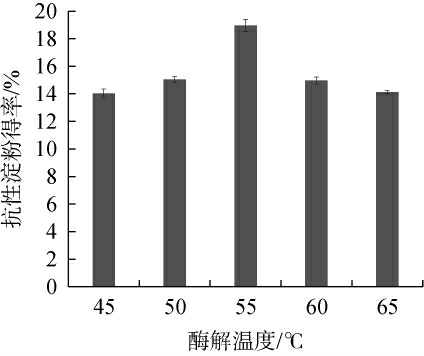
图3 酶解温度对丢糟抗性淀粉得率的影响
Fig.3 Effect of enzymatic temperature on the yield of resistant starch from distiller's grains
2.2.4 酶解时间对丢糟抗性淀粉得率的影响
由图4可知,随着酶解时间的延长,RS得率呈先上升后下降的趋势。当酶解时间在12 h时RS得率最高,为21.69%。若酶解时间<12 h,酶作用时间太短,淀粉脱支效果不理想,脱下的短链分子不足以形成更多的抗性淀粉晶体结构。若脱支酶作用时间过长,淀粉完全被脱支,导致体系中游离的短链分子太多,使反应体系中直链淀粉与支链淀粉的比例不协调,不利于抗性淀粉形成。直链淀粉与支链淀粉分子比例对抗性淀粉的形成有很大的影响[32],而分子比例与酶的作用息息相关[33],因此,确定最适的酶解时间为12 h。
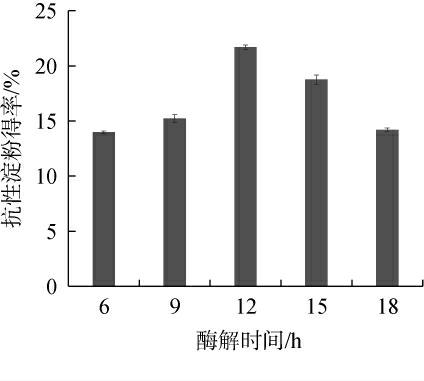
图4 酶解时间对丢糟抗性淀粉得率的影响
Fig.4 Effect of enzymatic time on the yield of resistant starch from distiller's grains
2.3 酱香型白酒丢糟抗性淀粉制备工艺优化正交试验结果与分析
酱香型白酒丢糟抗性淀粉制备工艺优化的正交试验结果见表4。
表4 抗性淀粉制备工艺优化正交试验设计与结果
Table 4 Design and results of orthogonal experiment for preparation process optimization of resistant starch
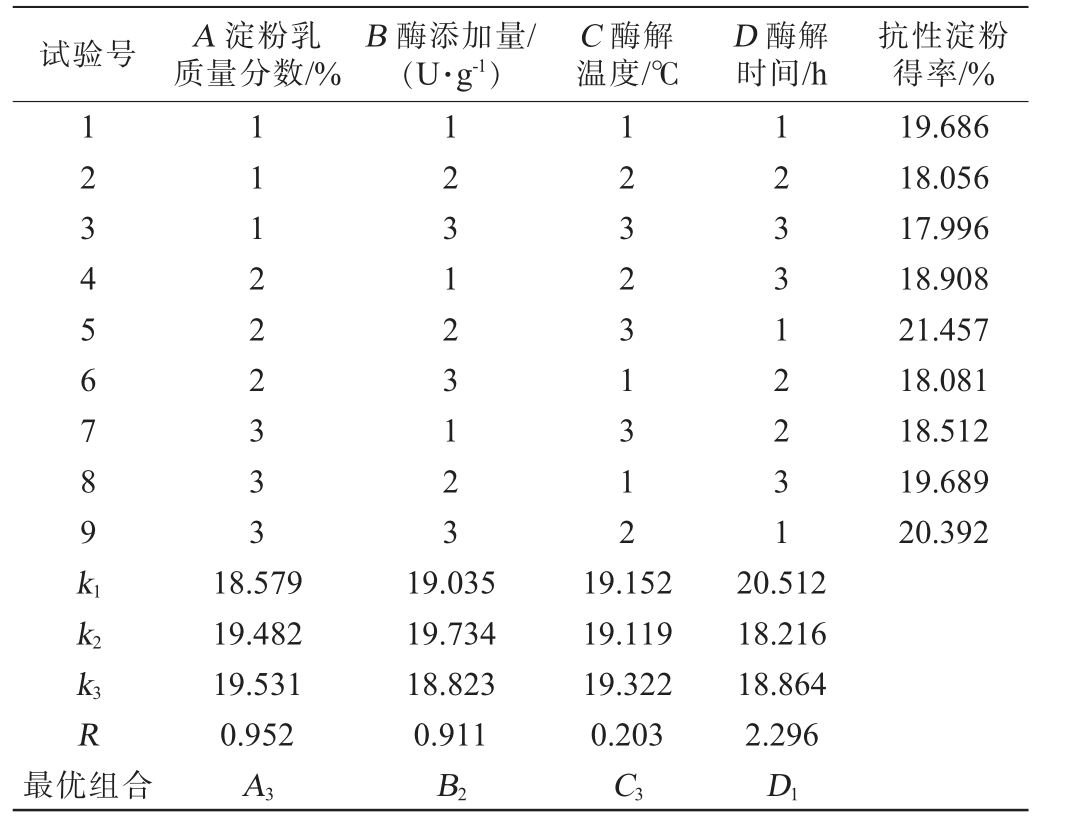
试验号 A 淀粉乳质量分数/%B 酶添加量/(U·g-1)C 酶解温度/℃ D 酶解时间/h抗性淀粉得率/%123456789k1 111222333 123123123 123231312 123312231 19.686 18.056 17.996 18.908 21.457 18.081 18.512 19.689 20.392 k2 k3R最优组合18.579 19.482 19.531 0.952 A3 19.035 19.734 18.823 0.911 B2 19.152 19.119 19.322 0.203 C3 20.512 18.216 18.864 2.296 D1
由表4可知,根据极差R值大小得到影响酱香型白酒丢糟抗性淀粉得率因素的主次顺序是:酶解时间(D)>淀粉乳质量分数(A)>酶添加量(B)>酶解温度(C)。由K值可知,酱香型白酒丢糟制备抗性淀粉的最优组合是A3B2C3D1,即淀粉乳质量分数35%,普鲁兰酶添加量20 U/g,酶解温度60 ℃,酶解时间11 h。在此条件下,抗性淀粉得率为22.15%,均高于其他正交组合。
2.4 抗性淀粉的理化指标测定结果与分析
2.4.1 抗性淀粉溶解度测定结果
淀粉的溶解和膨胀与淀粉的晶体结构以及直链、支链淀粉分子的分子量所占的比例有关[34]。由图5可知,随着酶解温度的升高,RS的溶解度明显升高,当温度达到80 ℃时溶解度最大,达到26.24%。因此可以推测RS高温糊化,因其改性后结构较为疏松,体系中直链分子量增加,有利于水分子与之结合,从而增大了RS的溶解速率[35]。丢糟淀粉的溶解度也随着温度的增加而增加,但总体变化不明显,90 ℃时溶解度最大,为5.19%。可能是淀粉颗粒不溶于冷水,当温度逐渐增加,淀粉结构中的直链分子从被破坏的晶体结构中脱出,开始溶解在水中,而RS由于经酶脱支导致支链淀粉被降解,产生更多的直链淀粉溶解于水分子[36],所以总体RS的溶解度大于丢糟淀粉。
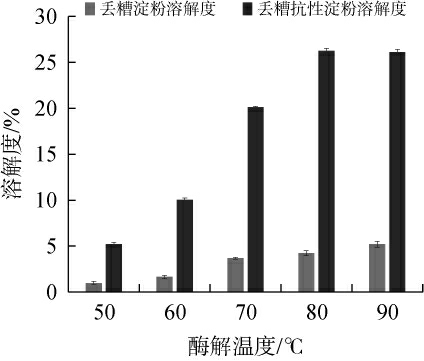
图5 酱香型白酒丢糟淀粉和抗性淀粉的溶解度
Fig.5 Solubility of the distiller's grains starch and resistant starch in the sauce-flavor Baijiu
2.4.2 抗性淀粉膨胀度测定结果
由图6可知,RS的膨胀度没有明显变化,只是缓慢增加后趋于平稳,酶解温度90 ℃时,膨胀度为7.99%。其原因可能是丢糟淀粉经脱支酶的作用,大量支链分子被脱支转化成短链的直链分子[37-38],而丢糟抗性淀粉随着温度的升高,其膨胀度显著上升,酶解温度90 ℃时,膨胀度为15.86%。其原因是淀粉结构因高温出现破损,直链分子脱出,剩下的支链分子大量吸收水分子而膨胀,导致淀粉的膨胀度显著增加。当温度<70 ℃时,RS膨胀度比淀粉大,原因可能是淀粉不溶于冷水,内部结构还没有完全被破坏,导致吸收水分子速度减缓。
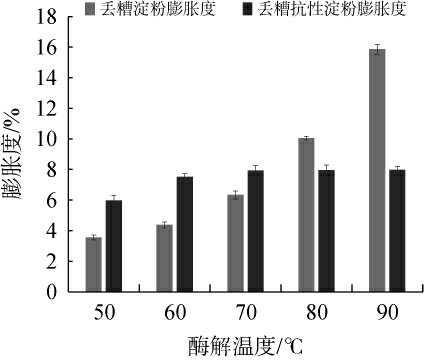
图6 酱香型白酒丢糟淀粉和抗性淀粉的膨胀度
Fig.6 Expansion of the distiller's grains starch and resistant starch in the sauce-flavor Baijiu
2.4.3 抗性淀粉模拟人工胃、肠液消化率测定结果
丢糟淀粉与RS的胃液消化率、肠液消化率和胃、肠液复合消化率见图7。由图7可知,随着消化时间在30~180 min增加,丢糟淀粉与RS在人工胃液的消化率均逐渐增加,分别为5.75%~7.98%、1.52%~2.71%,在人工肠液中的消化率也逐渐增加,分别为10.21%~14.62%、3.45%~4.65%。不管是胃液、肠液还是胃、肠液复合消化,RS的消化率均明显低于丢糟淀粉,且RS在人工肠液的消化率高于人工胃液,可见胰蛋白酶对抗性淀粉的作用更强。相比人工胃、肠液单个消化率,人工胃肠液对丢糟淀粉的复合消化率显著增加(34.55%~46.31%),而对RS的消化率升幅不大(4.44%~9.32%)。总之,丢糟淀粉的消化率始终高于RS,RS的消化率普遍低于10%,由此说明RS确实不易被人体胃和小肠消化,属于抗消化淀粉,可能的原因是普通淀粉的结构较疏松,暴露出的结合位点更易与酶相结合,使其消化率增加。而RS因其经过脱支酶的作用,淀粉结构经过折叠、弯曲等变化从而更加稳定[27]。胃蛋白酶很难和RS上的结合位点相结合,所以总体消化水平不高,属于抗消化淀粉。
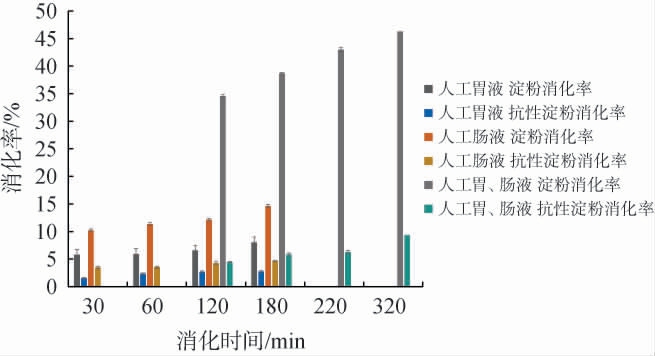
图7 酱香型白酒丢糟淀粉和抗性淀粉的消化率
Fig.7 Digestibility of the distiller's grains starch and resistant starch in the sauce-flavor Baijiu
3 结论
本研究首先考察了不同方法提取酱香型白酒丢糟所得淀粉的纯度,再利用单因素及正交试验优化了丢糟抗性淀粉的制备工艺,并对其理化特性进行测定分析。结果表明,采用酶法制备的丢糟淀粉纯度最高,达56.81%。酱香型白酒丢糟制备抗性淀粉的最佳工艺条件为淀粉乳质量分数35%、酶添加量20 U/g、酶解温度60 ℃、时间11 h,在此条件下抗性淀粉得率为22.15%。此外,丢糟淀粉和抗性淀粉的溶解度和膨胀度均随酶解温度的升高而增加,抗性淀粉膨胀度升幅相对较低。体外消化试验表明,抗性淀粉在胃液、肠液及胃肠复合液中的消化率均低于普通淀粉,分别为2.71%、4.65%和9.32%,抗消化能力更强。后续可进一步探索不同类型酶组合对丢糟抗性淀粉品质与得率的影响,推动酱香型白酒丢糟抗性淀粉制备技术革新,助力其在食品、医药等领域大规模应用。
[1]李欣.酱香型白酒酒糟资源化利用分析研究[J].酿酒科技,2023(8):128-131.
[2]杨文鹃,王晓丹,蒋文,等.酱香型白酒副产物酒糟窖底水综合利用的研究进展[J].中国酿造,2024,43(3):6-12.
[3]卢皓,田金平,吕一铮,等.白酒酿造固体废弃物资源化利用新进展[J].环境工程,2022,40(11):231-236,250.
[4]刘静.板栗淀粉老化特性及抗性淀粉的制备[D].秦皇岛:河北科技师范学院,2020.
[5]LI H T, ZHANG L, LI J, et al.Resistant starch intake facilitates weight loss in humans by reshaping the gut microbiota[J].Nat Metab,2024,6:578-597.
[6]ZENG X,CHEN L,ZHENG B.Extrusion and chlorogenic acid treatment increase the ordered structure and resistant starch levels in rice starch with amelioration of gut lipid metabolism in obese rats[J].Food Funct,2024,15(1):3425-3426.
[7]卞科,李雅楠,关二旗.甘薯抗性淀粉的制备工艺及应用研究进展[J].河南工业大学学报(自然科学版),2017,38(2):122-128.
[8]陈瑜.利用CRISPR/Cas9技术编辑粳稻中淀粉分支酶SBE3基因的研究[D].上海:上海师范大学,2023.
[9]王则徐,周文菊,陈正行,等.不同制备方法对青稞抗性淀粉消化性的影响[J].食品与发酵工业,2024,50(1):189-195.
[10]祝水兰,周巾英,刘光宪,等.超声波辅助酸酶法提取碎米抗性淀粉工艺的优化[J].南方农业学报,2019,50(8):1814-1821.
[11]林晓丽.山药抗性淀粉性质的研究及其在面条加工中的应用[D].福州:福建农林大学,2023.
[12]王琨.豌豆抗性淀粉粉丝的制备及其特性研究[D].济南:齐鲁工业大学,2022.
[13]聂永增.对于酒糟综合利用现状及创新应用的思考[J].轻工科技,2021,37(9):11-12.
[14]程宇.利用黄豌豆淀粉酶法制备抗性淀粉的研究[D].哈尔滨:哈尔滨商业大学,2014.
[15]祁瑜婷.高粱淀粉制备及其功效评价研究[D].济南:山东大学,2018.
[16]郑发英,赵梓娴,曾姗姗,等.响应面法优化黑苦荞抗性淀粉制备工艺研究[J].中国粮油学报,2023,38(12):99-105.
[17]尹秀华,谭瑶瑶,吴亨,等.不同酸法制备木薯抗性淀粉的比较[J].食品工业科技,2013,34(21):107-110,114.
[18]龙琳,韦金娜,朱宝生,等.紫薯的营养价值与加工应用[J].轻工科技,2024,40(4):22-24,76.
[19]BECKER A, SCHMARTZ G P, GRÖGER L, et al.Effects of resistant starch on symptoms, fecal markers, and gut microbiota in Parkinson's disease-The RESISTA-PD Trial[J].Genomics, Proteomics & Bioinformatics,2022,20(2):274-287.
[20]KOKSEL H,CAKMAK T H Z,OZKAN K,et al.A novel high-amylose wheat-based functional cereal soup (tarhana) with low glycemic index and high resistant starch[J].J Cereal Sci,2024,117:3911.
[21]郭晓冬,李颖.小米淀粉提取方法的比较[J].中国粮油学报,2011,26(5):26-29.
[22]葛云飞.高粱抗性淀粉介导肠道菌群调节绝经大鼠脂代谢[D].大庆:黑龙江八一农垦大学,2020.
[23]NY/T 4358—2023 植物源性食品中抗性淀粉的测定 分光光度法[S].2023.
[24]王淑,武悦,王鹏.3,5-二硝基水杨酸比色法测定番茄中可溶性糖[J].现代农业科技,2025(1):142-144.
[25]高贯威,匡立学,李银萍,等.基于3,5-二硝基水杨酸比色法探究苹果中可溶性糖测定方法及其含量[J].中国果树,2021(7):74-77.
[26]许佳玉.枇杷核抗性淀粉制备工艺优化及其结构和特性研究[D].扬州:扬州大学,2022.
[27]廖金贤,赵瑞璇,刘倩楠,等.马铃薯淀粉糊化度对乳液凝胶稳定性的影响及机理[J].食品科学,2025,46(7):107-118.
[28]高嫚,贾健辉,周迅,等.基于AOAC 法对Englyst法测定粳米淀粉消化特性的优化[J].食品工业科技,2023,44(10):264-269.
[29]刘青.基于挤压技术调控的抗性淀粉制备及形成机制探究[D].无锡:江南大学,2023.
[30]BANGAR S P,ASOGBON A D,SING H A,et al.Enzymatic modification of starch: A green approach for starch applications[J].Carbohydr Polym,2022,287:119265.
[31]曾红华,谢涛,杨莉,等.几种薯类与豆类抗性淀粉的抗消化性及其益生效应[J].中国粮油学报,2012,27(11):30-33.
[32]谢影影.鹰嘴豆抗性淀粉的制备及其功能特性与应用的研究[D].郑州:河南工业大学,2023.
[33]常蕾,王杰儒,杨敏,等.西米品质特性研究[J].食品与机械,2021,37(2):28-33.
[34]FANG G H,LIU K,GAO Q Y.Effects of heat-moisture treatment on the digestibility and physicochemical properties of waxy and normal potato starches[J].Foods,2022,12(1):68.
[35]王春俭.OCC二次淀粉溶解特性研究及其资源化利用[D].南京:南京林业大学,2019.
[36]赵云龙,文红花,杨菁杰,等.响应面法优化微波辅助酶解制备木薯抗性淀粉的工艺研究[J].中国食品添加剂,2023,34(3):114-124.
[37]WANG Z, GAO M, KAN J, et al.Resistant starch from purple sweet potatoes alleviates dextran sulfate sodium-induced colitis through modulating the homeostasis of the gut microbiota[J].Foods, 2024, 13(7):1028.
[38]陈金玉,胡方洋,吉芷芮,等.豌豆抗性淀粉对肌原纤维蛋白乳液凝胶特性及蛋白质体外消化率的影响[J].食品科学,2024,45(24):26-35.