贵州省是酱香型白酒的发源地和核心产区,得天独厚的气候条件,使其成为生产白酒优势的生态环境[1]。贵州省酱香型白酒酒厂主要分布于毕节市、贵阳市和遵义市[2]。
在酱香型白酒的多轮次发酵过程中,中间轮次(特别是第四轮次)被视为整个酿造周期的“黄金阶段”与“稳态期”。此阶段酿造微生态系统中的温度、酸度、水分、乙醇浓度及营养成分等关键参数趋于动态平衡,微生物群落结构与功能处于高度活跃和相对稳定的状态。在酱香型白酒发酵过程中,大曲为酒醅发酵提供了微生物和相关酶,是白酒酿造的糖化发酵剂,亦是白酒香气来源之一[3]。酱香型白酒采用开放式固态发酵,且发酵周期长,堆积发酵和窖池发酵是此过程中两个不同的发酵方式。由于发酵场和物态、生态环境的差异性,这两种发酵方式中的微生物群结构会有显著的不同[4]。堆积发酵的主要功能是促进大曲微生物的呼吸繁殖,同时也能在空气中网络微生物,使它们在堆积过程中迅速生长繁殖,逐步进行糖化发酵,为下窖继续发酵奠定基础[5]。窖池发酵可以进一步促进酱香风味化合物的生成,并抑制有害微生物的繁殖[6]。近年来,高通量测序技术突破了传统微生物纯培养方法的限制,已被广泛应用于微生物群落结构的研究中[4,7-9]。
酱香型白酒采用开放式的固态酿造工艺,其发酵过程微生物种类繁多,一直是研究的热点与难点。细菌作为酱香型白酒堆积和窖内发酵过程中产酶、生香的功能微生物菌群,对酱香型白酒风味的形成具有重要意义[10]。GE D Y等[11]应用高通量测序技术对湖北襄阳地区第四轮次酱香型白酒堆积发酵过程中的细菌群落演替规律进行分析,结果表明,热放线菌属(Thermoactinomyces)(63.95%)和芽孢杆菌属(Bacillus)(11.77%)为主要的细菌属。WANG L M等[12]研究发现,在贵州省的赤水河畔,泛菌属(Pantoea)、芽孢杆菌属(Bacillus)、蔓生芽胞杆菌属(Lentibacillus)和海洋杆菌属(Oceanobacillus)分别为四季代表性功能菌属。邹恬杏等[13]应用高通量测序技术探究贵州洞酿酱香酒第四轮次微生物群落,结果发现枝芽胞杆菌属(Virgibacillus)、海洋芽孢杆菌属(Oceanobacillus)、乳杆菌属(Lactobacillus)等7个优势细菌属。截至目前,酱香型白酒的微生物群落研究大多是发酵过程中的某一阶段,没有完整的对酿造过程有一个综合性的探究。
本研究以贵州具有代表性的不同产地酱香型白酒第四轮次的摊晾样品、堆积发酵酒醅、窖池发酵酒醅以及大曲为研究对象,基于高通量测序技术阐明发酵过程细菌群落演变规律及不同地区大曲中细菌的群落结构,并进一步采用QIIME2对大曲中细菌群落的京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)代谢功能进行预测,以期为解析贵州酱香型白酒酿造过程特征性微生物和提高传统工艺质量水平提供数据支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
大曲样品(E)和酒醅样品(A、B、C)均于2023年度采自贵州省贵阳市(G)、贵州省金沙县(J)和贵州省茅台镇(M)的酱香型白酒厂生产车间四轮次生产。其中酒醅样品A、B、C分别为摊晾、堆积发酵结束时和窖池发酵结束后的酒醅样品。采用五点法采样,样品保存于-80 ℃。
1.1.2 化学试剂
Zymo Research BIOMICS脱氧核糖核酸(deoxyribonu cleic acid,DNA)Microprep Kit:美国Zymo Research公司;KOD-Plus-Neo DNA Polymerase:日本TOYOBO(东洋纺)公司;NovaSeq 6000 SP Reagent Kit V1.5:美国Illmina公司。
1.2 仪器与设备
Applied![]() 9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国Thermo Fisher Scientific公司;Illumina NovaSeq 6000测序仪:美国Illumina公司;
9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国Thermo Fisher Scientific公司;Illumina NovaSeq 6000测序仪:美国Illumina公司;![]() F200 PRO多功能酶标仪:瑞士Tecan公司。
F200 PRO多功能酶标仪:瑞士Tecan公司。
1.3 方法
1.3.1 样品中细菌菌群基因组DNA的提取
所有样品均用0.1 mol/L无菌磷酸盐缓冲液(phosphate buffer solution,PBS)预处理,然后以10000r/min离心10 min,弃去上清,收集沉淀。采用Zymo Research BIOMICS DNA Microprep Kit提取细菌菌群的基因组DNA,使用0.8%琼脂糖凝胶电泳检测基因组DNA的完整性,随后使用Tecan F200进行核酸浓度检测。
1.3.2 PCR扩增及高通量测序
以提取的基因组DNA为模板,采用带有索引序列的特异引物515F(5'-GTGYCAGCMGCCGCGGTAA-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')对细菌菌群16SrDNA基因的V4区域基因序列进行PCR扩增。PCR扩增条件:94 ℃预变性1 min;94 ℃变性20 s,54 ℃退火30 s,72 ℃延伸30 s,25~30个循环;72 ℃再延伸5 min。PCR扩增体系:10×PCR Buffer for KOD-Plus-Neo 5 μL,2 mmol/L脱氧核糖核苷三磷酸(deoxy-ribonucleosidetriphosphates,dNTPs)5μL,25mmol/L MgSO4 3 μL,上下游引物各1.5 μL,KOD-Plus-Neo(1 U/μL)1 μL,模板DNA 40 ng,用双蒸水(ddH2O)补充至50 μL。使用![]() UltraTM II DNA Library Prep Kit for
UltraTM II DNA Library Prep Kit for![]() 建库。基于NovaSeq 6000平台以及PE250测序方式,使用NovaSeq6000SPReagentKitV1.5对构建好的文库进行测序。
建库。基于NovaSeq 6000平台以及PE250测序方式,使用NovaSeq6000SPReagentKitV1.5对构建好的文库进行测序。
1.3.3 数据处理与统计分析
测序得到的原始下机数据经过拼接、过滤得到可供后续分析的高质量目标序列。使用QIIME2软件完成序列降噪和嵌合体去除,生成扩增子序列变异体特征表和特征序列。采用SILVA数据库进行对扩增子序列变异体特征序列进行物种注释。使用SPPS 26.0软件处理数据并进行单因素方差分析,结果以“平均值±标准差”表示,运用R语言、Origin 2025、Tbtools-Ⅱv2.310等软件绘制韦恩图、丰度图、稀释曲线等。采用PICRUSt2软件预测细菌菌群的KEGG代谢功能。
2 结果与分析
2.1 不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中细菌群落α多样性分析
从贵州省不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中细菌菌群测序结果中随机抽取一定量的序列,并统计它们所代表的操作分类单元(operational taxonomic unit,OTU)数,以抽取的一系列序列数和相应的OTU数构建稀释曲线,结果见图1。由图1可知,随着测序深度的增加,基于细菌群落OTU数的稀释曲线呈先升高后趋于平缓的趋势,当序列数>10 000条时趋于稳定,表明测序结果已足以反映样品微生物多样性,能满足生物信息学后续分析要求。
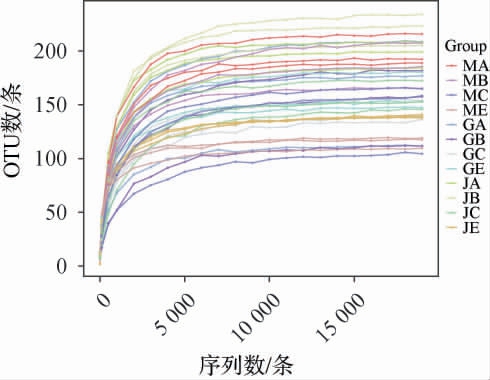
图1 基于操作分类单元数贵州不同产地大曲及酱香型白酒第四轮次酒醅样品发酵过程中细菌菌群的稀释曲线
Fig.1 Dilution curves of bacterial communities in Daqu and fermented grains samples of sauce-flavor Baijiu from different production areas in Guizhou during fermentation based on the operational taxonomic units
贵州不同产区大曲及酱香型白酒第四轮次酒醅发酵过程中细菌菌群的α多样性见表1。
表1 贵州不同产地大曲及酱香型白酒第四轮次酒醅样品发酵过程中细菌群落的α多样性指数
Table 1 Alpha diversity indices of bacterial communities in Daqu and fermented grains samples of sauce-flavor Baijiu from different production areas in Guizhou during fermentation
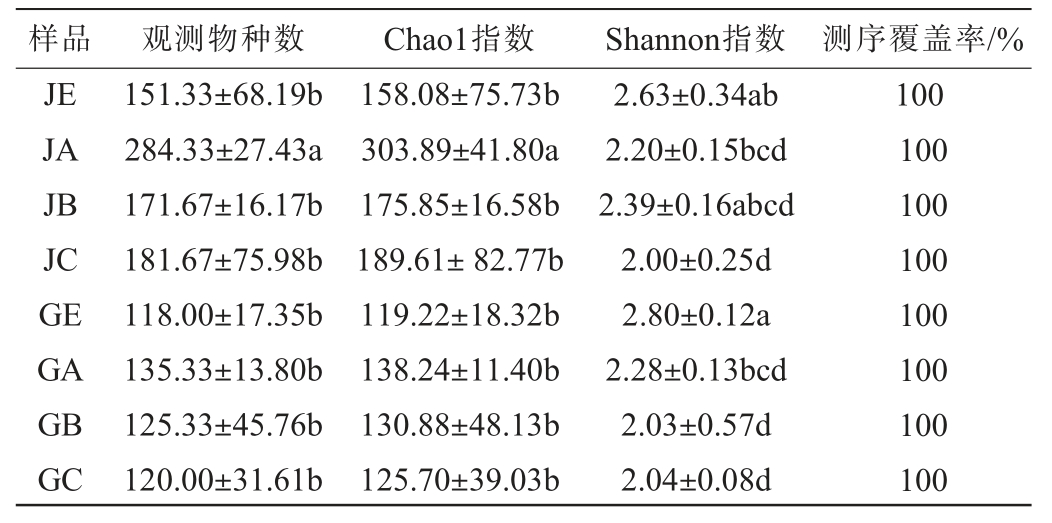
样品 观测物种数 Chao1指数 Shannon指数 测序覆盖率/%JE JA JB JC GE GA GB GC 151.33±68.19b 284.33±27.43a 171.67±16.17b 181.67±75.98b 118.00±17.35b 135.33±13.80b 125.33±45.76b 120.00±31.61b 158.08±75.73b 303.89±41.80a 175.85±16.58b 189.61±82.77b 119.22±18.32b 138.24±11.40b 130.88±48.13b 125.70±39.03b 2.63±0.34ab 2.20±0.15bcd 2.39±0.16abcd 2.00±0.25d 2.80±0.12a 2.28±0.13bcd 2.03±0.57d 2.04±0.08d 100 100 100 100 100 100 100 100
续表
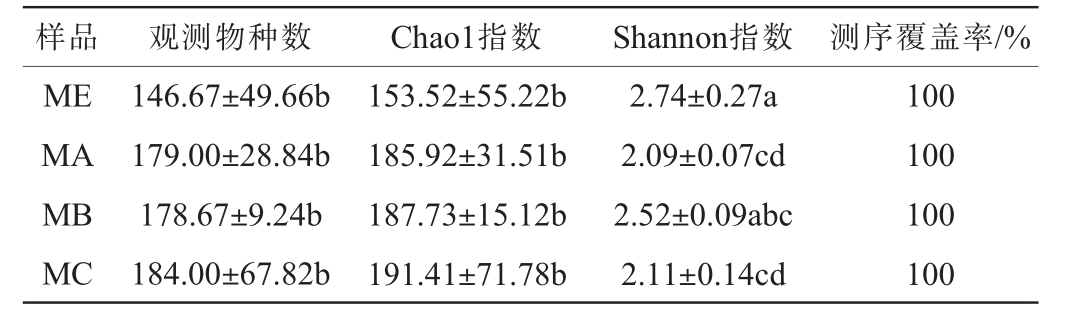
注:同列间不同字母表示差异显著(P<0.05)。
样品 观测物种数 Chao1指数 Shannon指数 测序覆盖率/%ME MA MB MC 146.67±49.66b 179.00±28.84b 178.67±9.24b 184.00±67.82b 153.52±55.22b 185.92±31.51b 187.73±15.12b 191.41±71.78b 2.74±0.27a 2.09±0.07cd 2.52±0.09abc 2.11±0.14cd 100 100 100 100
由表1可知,所有样本的测序覆盖率均为100%,表明本次测序结果能够代表所有样品中微生物的真实情况,结果与稀释曲线一致。由表1亦可知,在不同产地的酱香型白酒大曲中细菌菌群的观测物种数和Chao1指数均低于酒醅样品,然而其Shannon指数均高于酒醅样品,说明相较于大曲而言,酒醅发酵过程中细菌群落的丰富度有所增加,但多样性有所下降。金沙产地的摊晾酒醅样品中观测物种数和Chao1指数均显著高于其他产地和其他发酵阶段的酒醅样品(P<0.05),表明在本次采样中金沙产地环境中的细菌菌群丰富度相对较高。
2.2 不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中细菌群落结构分析
2.2.1 基于门水平细菌群落结构分析
基于门水平,贵州不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中的细菌群落结构见图2。由图2可知,在大曲和酒醅样品中共鉴定出33个细菌门,包括5个优势细菌门(相对丰度>1%),分别为厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、拟杆菌门(Bacteroidetes)和梭杆菌门(Fusobacteria)。其中,厚壁菌门(Firmicutes)和变形菌门(Proteobacteria)是大曲和酒醅中共有的优势细菌门。在金沙和茅台产地的酒醅发酵过程中厚壁菌门的相对丰度明显增加(15.65%~51.35%、21.90%~56.45%),而变形菌门的相对丰度明显降低(78.42%~45.60%、74.38%~41.90%)。变形菌门是酱香型白酒生产过程中的常见菌[14]。不同产地大曲中共有的优势细菌门还包括放线菌门(Actinobacteria),其在酱香型白酒的酿造过程中对有害杂菌具有一定的抑制作用[15],但是在发酵过程中放线菌门未成为酒醅中的优势细菌门。陈卓等[16]的研究表明,在贵州洞酿酱香型白酒堆积发酵过程中放线菌门的相对丰度下降显著,与本研究结果相一致。此外,不同产地酒醅样品中的优势细菌门具有一定的差异,拟杆菌门(Bacteroidetes)是金沙和茅台产地摊晾酒醅样品和堆积发酵酒醅样品的优势细菌门,WANG L M等[12]的研究表明,拟杆菌门是茅台镇酿造环境中的主要优势细菌门之一。梭杆菌门(Fusobacteria)(1.14%)为金沙产地摊晾酒醅样品特有的优势菌门。王琳等[17]从贵州茅台镇1~7轮次堆积发酵期的酿造环境中检测出4个优势细菌门,分别为变形菌门、厚壁菌门、拟杆菌门和放线菌门。整体来看,不同产地酱香型白酒大曲的优势细菌在门水平上具有较大的相似性,但细菌菌群相对丰度存在一定的差异。
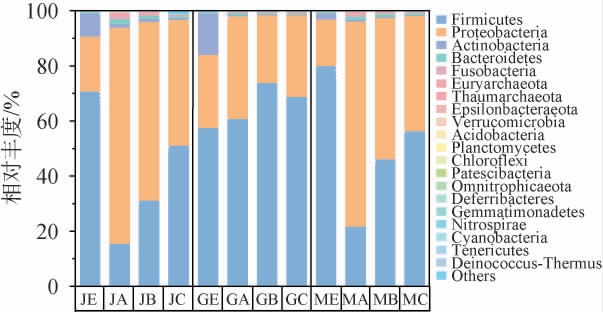
图2 基于门水平贵州不同产地大曲及酱香型白酒第四轮次酒醅样品发酵过程中的细菌群落结构
Fig.2 Bacterial community structures in Daqu and fermented grains samples of sauce-flavor Baijiu from different production areas in Guizhou during fermentation at phylum level
Others表示平均相对丰度排名20之后的其他所有门。
2.2.2 基于属水平细菌群落结构分析
从贵州不同地区酱香型白酒四轮次发酵大曲和酒醅样品中共鉴定出412个细菌属,包括19个优势细菌属,其中平均丰度排名前50的细菌属见图3。厚壁菌门在属水平上的优势微生物(相对丰度>1%)主要有乳酸杆菌属(Lactobacillus)(0.96%~49.86%)、克罗彭斯特菌属(Kroppenstedtia)(0.45%~42.58%)、枝芽胞杆菌属(Virgibacillus)(0.16%~24.75%)、芽孢杆菌属(Bacillus)(0.64%~10.29%)、高温放线菌属(Thermoactinomyces)(0.08%~12.13%)、火山渣芽孢杆菌属(Scopulibacillus)(0.06%~3.86%)和大洋芽孢杆菌属(Oceanobacillus)(0.01%~4.44%)等15个属;变形菌门在属水平上的优势微生物是假单胞菌属(Pseudomonas)(0.50%~51.10%)、大肠埃希氏菌属-志贺氏菌属(Escherichia-Shigella)(6.24%~26.07%)、醋杆菌属(Acetobacter)(0~2.03%)和泛生菌属(Pantoea)(0~1.34%)。这些优势细菌属组成与黄廷财等[5,13,18-20]对贵州地区酱香型白酒酿造过程中的优势细菌属的研究结果基本一致。
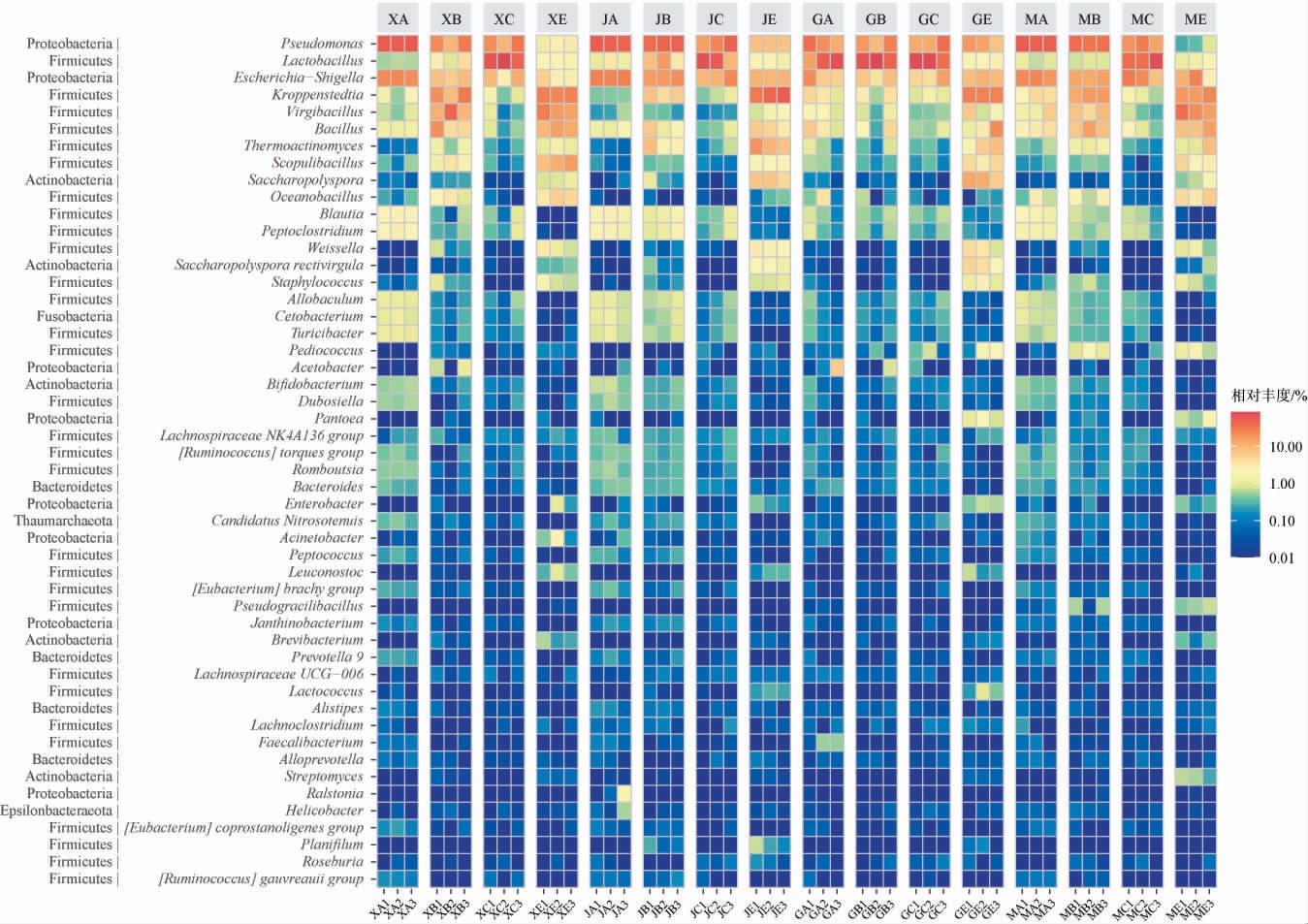
图3 基于属水平贵州不同产地大曲及酱香型白酒第四轮次酒醅样品发酵过程中的细菌群落结构
Fig.3 Bacterial community structures in Daqu and fermented grains samples of sauce-flavor Baijiu from different production areas in Guizhou during fermentation based on genus level
不同产地成品大曲在属水平上的细菌群落结构较为相似,乳酸菌杆菌属、埃希氏菌属、克罗彭斯特菌属、枝芽胞杆菌属、芽孢杆菌属、高温放线菌属、火山渣芽孢杆菌属和糖多孢菌属(Saccharopolyspora)共8个属是共有的优势细菌属。在金沙和贵阳产地的大曲细菌群落中均以克罗彭斯特菌属占绝对优势(42.58%和26.17%),它是一种嗜热菌,这也与丁芳等[8]对特级高温大曲细菌群落的结果一致。枝芽胞杆菌属是茅台产地大曲样品中相对丰度最高的细菌属(24.75%),DU Y K等[21]的研究表明它能够促进吡嗪类风味物质的形成。此外,金沙产地和贵阳产地共有的优势细菌属包括假单胞菌属和魏斯氏菌属(Weissella)。贵阳产区和茅台镇产地共有的优势菌属包括片球菌属(Pediococcus)和泛生菌属。大洋芽孢杆菌属是茅台产地大曲中特有的优势细菌属。
不同产地的摊晾酒醅样品中,金沙和茅台产地的主要优势细菌属均是假单胞菌属(49.38%、51.10%)和埃希氏菌属(26.07%、22.34%),贵阳产地的主要优势细菌属是假单胞菌属(23.43%)、乳酸杆菌属(45.58%)和埃希氏菌属(11.25%)。
经过堆积发酵后,金沙产地的主要优势细菌属未发生改变,假单胞菌属和埃希氏菌属的相对丰度只有略微的下降,在此过程中克罗彭斯特菌属(5.77%)和高温放线菌属(4.32%)成为优势细菌属。在茅台产地,相较于摊晾酒醅样品,克罗彭斯特菌属的相对丰度(15.54%)提高了约5倍,成为主要优势细菌属,而假单胞菌属和埃希氏菌属的相对丰度分别降低了29.82%和36.66%。在贵阳产地,优势细菌属中只有乳酸杆菌属的相对丰度在增加,其余优势细菌属的相对丰度均降低,可能是乳酸杆菌属对其生物性抑制所致[4]。堆积发酵是淀粉糖化过程中的关键步骤,其中微生物代谢活动产生的水解酶对淀粉糖化起着重要作用[22]。在高温堆积阶段,温度需维持在约50 ℃,这一条件促进了耐热微生物成为优势菌群[23]。在此过程中酱香和酱香前体物质持续积累,对酱香型白酒的风味品质形成起着重要作用[24]。
不同产地窖池发酵结束后的酒醅中乳酸杆菌属成为相对丰度最大的优势细菌属(45.44%~62.73%)。胡小霞等[4,13,25]的研究表明,乳酸杆菌属是贵州省酱香型白酒核心产区各轮次酒醅的优势菌,是一种厌氧微生物,且入窖发酵后,氧气浓度较低,所以乳酸杆菌大量繁殖成为酱香型白酒堆积糟醅中主要优势菌群[26]。乳酸杆菌属可以通过分泌细菌素带代谢酸并控制腐败菌,作为有益菌群参与酱香型白酒的堆积发酵并可以调节发酵过程中其他微生物[6]。此外,它在生长过程中能够产生乳酸、乙酸等有机酸,乳酸能够和乙醇生成乳酸乙酯,这是贵州酱香型白酒中主要的酯类物质[27]。其次,假单胞菌属在此阶段样品中也保持着较高的相对丰度(21.13%~29.52%)。贵州地区酿造酱香型白酒主要采用本地种植的红缨子高粱,且具有相似的工艺条件,推测不同产地环境中的细菌组成及相对丰度差异,是导致每个产地酿造出的酱香型酒体风味不同的重要原因之一。
2.3 不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中细菌群落结构多样性的差异分析
基于bray-curtis距离矩阵对不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中的细菌OTU数进行主坐标分析(principal coordinates analysis,PCoA),结果见图4。由图4可知,PCo1的方差贡献率为43.5%,PCo2的方差贡献率为32.9%,PCo1和PCo2的累计方差贡献率为76.4%,说明前两个主坐标成分可以较好地反映不同产地大曲和不同发酵阶段酒醅样品的细菌群落结构。所有大曲样本都分布在第一象限,说明不同产地大曲样品中细菌群落组成具有一定的相似性。各地区的摊晾酒醅样品散布在不同象限,但均与窖池发酵结束后的酒醅样品存在明显分离。窖池发酵结束后的酒醅品中的细菌群落仍然具有一定差异性的同时,绝大多数都聚集到了一起,表明其细菌群落结构已趋于相似。结果表明,大曲的添加以及窖池发酵可能是驱动酒醅细菌群落趋同、促进贵州酱香型白酒稳定品质形成的关键因素。然而,不同产地生产过程中的环境微生物差异,可能导致最终窖池发酵酒醅的微生物结构仍保有地域性特征,这或许是造成贵州不同产地酱香型白酒风格存在细微差别的原因之一。
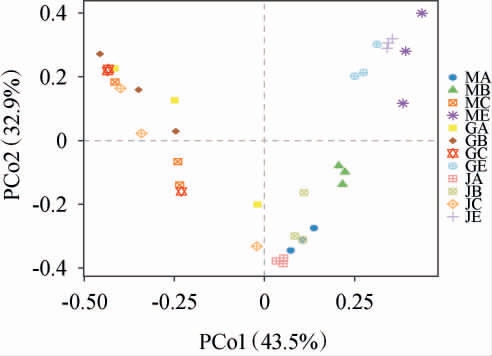
图4 基于细菌操作分类单元贵州不同产地大曲及酱香型白酒第四轮次酒醅发酵过程的主坐标分析结果
Fig.4 Principal coordinate analysis results of Daqu and fermented grains samples of sauce-flavor Baijiu from different production areas in Guizhou during fermentation based on the operational taxonomic units
2.4 不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中细菌群落功能预测
大曲在酱香型白酒酿造过程中扮演着发酵剂的角色,上述研究表明,大曲的添加及窖池发酵可能是驱动酒醅细菌群落趋同、促进贵州酱香型白酒稳定品质形成的关键因素之一。为了进一步了解大曲中细菌的作用,基于KEGG,采用PICRUSt2预测贵州不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中细菌菌群的功能基因,结果见图5。由图5可知,在贵州3个不同产地的大曲样品细菌菌群中预测的1级KEGG代谢通路包括细胞过程、环境信息处理、遗传信息处理、人类疾病、新陈代谢和生物体系统,表明大曲样本中存在旺盛的微生物代谢。在2级代谢通路中,与风味物质形成相关的氨基酸代谢和脂质代谢等途径表现出较高丰富度,这与WANG L M等[12]对茅台镇的大曲研究结果相一致。研究表明,在风味物质代谢和原料降解中,大曲中的细菌群落扮演着重要作用[28]。细菌通过分泌胞外酶催化酒醅中大分子物质的水解,为发酵过程提供可代谢底物,进而促进风味化合物的生物转化。如芽孢杆菌属可以通过分泌淀粉酶、蛋白酶、脂肪酶等多种酶水解蛋白质和淀粉等大分子物质,进而促进各种芳香物质的转化形成[29];王西等[29]研究发现,枯草芽孢杆菌(Bacillus subtilis)的接种能够通过产生中性蛋白酶协同其他微生物,增加酒醅的出酒率并增加吡嗪类风味物质的含量,对酒的品质形成有积极的作用。克罗彭斯特菌属具有较高的α-淀粉酶生产能力,这一特性能够增强淀粉转化为麦芽糖和葡萄糖的过程,从而改善液化过程[30]。此外,克罗彭斯特菌属能参与脂肪酸生物合成活动且与萜烯和各种氨基酸的合成呈正相关[31-33]。高温大曲中苯丙氨酸代谢代谢具有普遍性,芽孢杆菌、克罗彭斯特菌属、糖多孢菌属均可进行苯丙氨酸代谢[34]。这些途径与香气形成密切相关,且微生物酶在这些代谢过程中起着关键作用。

图5 基于京都基因与基因组百科全书贵州不同产地大曲及酱香型白酒第四轮次酒醅样品发酵过程中细菌菌群的1级(A)和2级(B)代谢通路分析结果
Fig.5 Analysis results of the first-level (A) and second-level (B) metabolic pathways of bacterial communities in Daqu and fermented grains samples of sauce-flavor Baijiu from different production areas in Guizhou during fermentation based on Kyoto Encyclopedia of Genes and Genomes
图b中仅展示丰度排名前10的代谢通路。
3 结论
本研究采用高通量测序技术结合PCoA研究贵州不同产地(金沙、贵阳和茅台)大曲及酱香型白酒第四轮次酒醅发酵过程中细菌群落的多样性及其动态变化规律,结果表明,各产地大曲样品中的细菌菌群丰富度均低于酒醅样品,而多样性则高于酒醅样品,且金沙产地摊晾酒醅样品中的细菌菌群丰富度最高。从不同产地大曲和酒醅样品中共注释到5个优势细菌门(相对丰度>1%)和19个优势细菌属。在属水平上,不同产地大曲样品群落结构相似,含有Lactobacillus、Escherichia-Shigella等8个共有优势细菌属;虽摊晾酒醅样品中的细菌群落结构差异较大,但经大曲添加及窖池发酵后,其细菌群落结构呈现趋同现象,窖池发酵结束,乳酸杆菌属(45.44%~62.73%)占据主导地位。结果表明,大曲的添加与窖池发酵是驱动微生物群落结构趋同、保障酱香型白酒品质稳定的关键因素。因此,进一步采用PICRUSt2软件对大曲中细菌群落的KEGG代谢功能进行预测,结果发现,大曲中的细菌群落积极参与氨基酸代谢、脂质代谢等途径,与风味物质形成密切相关。本研究结果为解析贵州不同产地酱香型白酒微生物群落结构提供了理论依据,对传统白酒工艺的优化与品质控制具有参考意义。
[1]WANG L, HUANG Y G, HU X X, et al.The impact of environmental factors on the environmental bacterial diversity and composition in the jiang-flavoured Baijiu production region[J].LWT-Food Sci Technol,2021,149:111784.
[2]郄广平,白旭,卜建东,等.贵州打造酱香型白酒金三角产区构想及策略[J].中国酿造,2024,43(8):281-285.
[3]薄涛,吕娜,杨凯环,等.白酒大曲发酵过程中微生物群落及功能研究进展[J].食品科学,2023,44(19):385-393.
[4]胡小霞,黄永光,涂华彬,等.酱香型白酒1轮次酿造细菌的菌群结构[J].食品科学,2020,41(14):175-182.
[5]黄廷财,柴丽娟,时伟,等.酱香型白酒第2、3轮次堆积发酵有机酸代谢规律与菌群结构及其相关性解析[J].食品科学,2024,45(18):106-115.
[6]LI K M,CHEN Y R,LIU T,et al.Analysis of spatial distribution of bacterial community associated with accumulation of volatile compounds in Jiupei during the brewing of special-flavor liquor[J].LWT-Food Sci Technol,2020,130:109620.
[7]WANG W H,XU Y Q,HUANG H Q,et al.Correlation between microbial communities and flavor compounds during the fifth and sixth rounds of sauce-flavor Baijiu fermentation[J].Food Res Int,2021,150:110741.
[8]丁芳,张原頔,蒋英丽,等.不同等级高温大曲微生物群落和代谢物的特征分析[J].中国酿造,2022,41(11):24-30.
[9]HU X L, WANG K L, CHEN M G, et al.Profiling the composition and metabolic activities of microbial community in fermented grain for the Chinese strong-flavor Baijiu production by using the metatranscriptome,high-throughput 16S rRNA and ITS gene sequencings[J].Food Res Int,2020,138:109765.
[10]谭壹,晏培,李冰冰,等.酱香型白酒功能微生物的应用研究进展[J].中国酿造,2024,43(3):1-5.
[11]GE D Y,WANG Y R,CAI W C,et al.Correlation analysis of microbial groups and sensory quality in the fourth round of the stacked fermentation of sauce-flavor liquor[J].Food Biosci,2024,59:103958.
[12]WANG L M,CHENG Y X,HU X X,et al.Analysis of bacterial diversity and functional differences of Jiang-flavored Daqu produced in different seasons[J].Front Nutr,2023,9:1078132.
[13]邹恬杏,苏伟,母应春,等.洞酿酱香酒第四轮次酒醅发酵过程中微生物群落与挥发性代谢物分析[J].中国酿造,2023,42(6):64-71.
[14]李大鹏,牟明月,朱治宇,等.酱香型白酒不同轮次细菌资源结构多样性的研究[J].酿酒科技,2023(8):112-117,140.
[15]袁再顺.“破堆移位”对酱香型白酒冬季堆积发酵的影响研究[D].贵阳:贵州大学,2019.
[16]陈卓,苏伟,母应春,等.洞酿酱香型白酒第三轮次酒醅发酵过程中微生物与挥发性风味物质相关性分析[J].中国酿造,2024,43(5):32-40.
[17]王琳,胡小霞,黄永光.茅台镇酱香型白酒不同生产轮次酿造环境的细菌菌群结构特征[J].食品科学,2021,42(22):185-192.
[18]朱安然,汪地强,胡建锋,等.酱香型白酒一轮次糟醅微生物群落结构及溯源分析[J].食品科学,2025,46(4):117-125.
[19]WANG H,HUANG Y G,HUANG Y L.Microbiome diversity and evolution in stacking fermentation during different rounds of jiang-flavoured Baijiu brewing[J].LWT-Food Sci Technol,2021,143:111119.
[20]QIAN W, LU Z M, CHAI L J, et al.Cooperation within the microbial consortia of fermented grains and pit mud drives organic acid synthesis in strong-flavor Baijiu production[J].Food Res Int,2021,147:110449.
[21]DU Y K,XIN W,XIA Y,et al.Analysis of fermentation control factors on volatile compounds of primary microorganisms in Jiang-flavor Daqu[J].J Food Biochem,2022,46(10):e14277.
[22]何艾莲,冯珊,程华峰,等.酱香型白酒酿造过程中微生物的多样性研究[J].中国食品工业,2024(19):137-139.
[23]孙利林,李立郎,胡萍,等.酱香型白酒第四轮次酒酿造过程中细菌多样性分析[J].中国酿造,2020,39(5):35-39.
[24]ZHAO X X, LIU Y H, SHU L, et al.Study on metabolites of bacillus producing soy sauce-like aroma in Jiang-flavor Chinese spirits[J].Food Sci Nutr,2020,8(1):97-103.
[25]王玉荣,侯强川,田龙新,等.酱香白酒第五轮次窖池发酵不同分层酒醅微生物群落与感官理化性质差异分析[J].食品科学,2023,44(22):250-256.
[26]吕锡斌,吴耀领,郝飞,等.高通量测序技术分析酱香型白酒下造沙轮次的微生物多样性[J].酿酒科技,2019(3):52-58,64.
[27]许忠平,梁明锋,张娇娇,等.不同地区酱香型白酒风格特征及风味物质构成差异相关性研究[J].中国酿造,2024,43(2):35-42.
[28]邹铨,张敏,李擎,等.河套地区中温大曲细菌菌群多样性解析及其风味品质评价[J].中国酿造,2023,42(10):73-79.
[29]王西,沈毅,张亚东,等.产香枯草芽孢杆菌在酱香型白酒生产中的应用[J].酿酒科技,2018(7):70-75.
[30]ZHU Q,CHEN L Q,PENG Z,et al.The differences in carbohydrate utilization ability between six rounds of sauce-flavor Daqu[J].Food Res Int,2023,163:112184.
[31]ZHANG J, DU R B, NIU J, et al.Daqu and environmental microbiota regulate fatty acid biosynthesis via driving the core microbiota in soy sauce aroma type liquor fermentation[J].Int J Food Microbiol,2024,408:110423.
[32]YANG L,FAN W L,XU Y.Chameleon-like microbes promote microecological differentiation of Daqu[J].Food Microbiol,2023,109:104144.
[33]ZHU C T, CHENG Y X, SHI Q L, et al.Metagenomic analyses reveal microbial communities and functional differences between Daqu from seven provinces[J].Food Res Int,2023,172:113076.
[34]WANG L C,ZHONG K,LUO A M,et al.Dynamic changes of volatile compounds and bacterial diversity during fourth to seventh rounds of Chinese soy sauce aroma liquor[J].Food Sci Nutr, 2021, 9(7): 3500-3511.