白酒是我国具有独特风味特征的传统蒸馏酒[1]。酯类化合物是白酒中最重要的一类风味物质,它们不仅赋予白酒特有的香气和口感,还对酒体整体风味平衡起决定性作用。在已知风味成分中,乳酸乙酯(ethyl lactate,EL)、乙酸乙酯(ethyl acetate,EA)、丁酸乙酯(ethyl butanoate,EB)和己酸乙酯(ethyl hexanoate,EH)普遍被认为是白酒四大关键酯类[2],其含量及比例可直接影响白酒香型的分类,构成酒体风味特征的“骨架”[1]。白酒种类和品牌较多,不同酒体乙醇含量差异较大(体积分数一般在30%~60%之间),乙醇作为酒体主要成分,不仅影响整体口感,还能调控酒体中风味物质的挥发性与呈香特性[3-5]。
近年来,一些研究分析了乙醇对风味化合物的影响。BOOTHROYD E L等[6]采用大气压化学电离质谱法测定威士忌模型中14种酯类、醇类等化合物在体积分数5%~40%乙醇水溶液中的顶空浓度,发现乙醇对它们的挥发性均产生抑制作用,且对弱极性物质抑制更强。KARLSSON B C G等[7]通过分子动力学模拟分别分析了威士忌中的愈创木酚、正辛烷和辛酸等物质在体积分数0~100%乙醇水溶液中的分布,研究发现,低体积分数乙醇能促进这些物质在气液界面分布,而高体积分数促使它们分布于溶液中心。然而,以上研究多采用实验或分子模拟方法分析乙醇对威士忌风味成分的影响,但在白酒体系中,从分子层面深入解析乙醇对风味物质调控机制的研究尚显不足。
目前,分子动力学模拟与量子化学技术为研究复杂物理化学体系中实验难以观测的微观行为提供了新途径。分子动力学模拟通过构建原子或分子的动态模型,能够有效解析复杂体系中分子的运动轨迹与相互作用;而量子化学方法,如密度泛函理论,则可精确量化溶解自由能、活化能及分子间弱相互作用等热力学参数。两种理论计算方法已广泛应用于食品研究领域,如分析风味物质在溶剂中的分布[7-9],风味组分之间的相互作用[10-13],功能组分与受体蛋白结合[14-17]等。这些方法为解析乙醇水混合体系中酯类挥发性的分子机制提供了有力工具。
综上,该研究以白酒中的乳酸乙酯、乙酸乙酯、丁酸乙酯和己酸乙酯为研究对象,分析乙醇对关键酯类物质挥发性抑制作用的分子机制。首先采用顶空固相微萃取-气相色谱-质谱联用技术(headspace solid-phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)分 析不同乙醇体积分数对关键酯类挥发性的影响;然后通过量子化学计算与分子动力学模拟分析乙醇对酯类物质的抑制机制;最后通过感官品评分析乙醇对酯类物质的实际感知影响,旨在为白酒的科学勾调与风味调控提供理论依据。
1 材料与方法
1.1 材料与试剂
乳酸乙酯、乙酸乙酯、丁酸乙酯、己酸乙酯、乙醇、氯化钠(均为分析纯):国药集团化学试剂有限公司;实验用水:杭州娃哈哈瓶装纯净水。
1.2 仪器与设备
8890-7000气相色谱-质谱联用仪(配有PAL3全自动固相微萃取机械臂及Quant-My-Way数据处理系统)、Arrow DVB/Carboxen/PDMS三相萃取针:美国安捷伦公司。
1.3 方法
1.3.1 溶液制备
分别将乳酸乙酯、乙酸乙酯、丁酸乙酯和己酸乙酯四种酯类单体溶解于体积分数分别为30%、40%、53%和60%的乙醇水溶液中。每种酯类在各个乙醇体积分数下,均配制6种不同质量浓度的溶液,质量浓度依次为50mg/L、100mg/L、250 mg/L、500 mg/L、1 000 mg/L和2 000 mg/L。样品配制完储存于-20 ℃备用。
1.3.2 顶空固相微萃取-气相色谱-质谱条件
HS-SPME条件:取7 mL样品(酯类乙醇水溶液)注入20 mL顶空瓶,加氯化钠至溶液饱和后加盖密封以待分析。使用PAL3自动固相微萃取装置,于45 ℃先平衡5 min后,再在相同温度下萃取40 min,萃取针在气相色谱进样口于250 ℃解吸附1 min,之后在老化端口于250 ℃老化5 min,完成一次萃取。
气相色谱条件:DP-FFAP色谱柱(60m×0.25mm,0.5μm);升温程序为50 ℃保持3min,以3 ℃/min升至80 ℃,保持2 min,以5 ℃/min升至240 ℃,保持3 min;载气(N2)流速1 mL/min,设置分流比为20∶1。
质谱条件:质谱分析采用多反应监测模式(multiple reaction monitoring,MRM),离子源温度230 ℃,四极杆温度150 ℃,具体MRM参数见表1。
表1 四种酯类物质的多反应监测模式参数
Table 1 Multi reaction monitoring mode parameters of four ester substances

酯类 保留时间/min 监测离子(m/z)碰撞能量/eV EL EA EB EH 20.2 5.7 8.5 15.6 45→29 88→43 88→60 88→61 20 25 15 15
定量方法:在获得各样品的色谱图后,记录四种酯类物质的色谱峰面积,并以此表征其在溶液液面上方顶空中的浓度。每个样品重复测定5次,取其平均值。为比较不同体积分数乙醇对酯类挥发性的影响,通过计算顶空色谱峰面积的相对比值来分析其挥发性变化。对于每种酯类,均以其在体积分数30%乙醇水溶液中的峰面积为基准,分别计算其在体积分数30%、40%、53%及60%乙醇水溶液中的峰面积与此基准的比值(即以乙醇体积分数30%条件下的值为1)。所得色谱峰面积比值用于后续的数据可视化分析。
1.3.3 量子化学计算
几何结构优化:为了确定分子在能量最低时的稳定构型,需对目标分子进行几何结构优化。使用Gaussian View软件构建酯类及乙醇分子初始结构,通过Molclus软件和Gaussian 16软件进行构象搜索,采用B3LYP-D3(BJ)/6-31G*理论计算方法完成几何结构优化。B3LYP-D3(BJ)/6-31G*是一种常用的量子化学计算方法,适用于中小型有机分子的几何结构优化[18-19]。
溶解自由能计算:溶解自由能(ΔGsolv)是指溶质分子从气相(Ggas)转移至溶剂(Gsol)的吉布斯自由能的差值,计算公式为:
ΔGsolv=Gsol-Ggas
式中:Gsol表示溶质分子在溶液中的单点能(kcal/mol),该单点能的计算采用Solvation Model Based on Density(SMD)溶剂模型[20],基于M05-2X/6-31G*理论方法[21]计算所得,该方法在描述溶剂化效应方面具有较高的精度[22];Ggas表示溶质分子在气体中的单点能,同样基于M05-2X/6-31G*理论方法计算所得。
1.3.4 分子动力学模拟
分子动力学模拟使用Gromacs[23]软件(版本2022.4),采用全原子通用安伯力场(general amber force field,GAFF)[24]结合RESP2电荷[25]进行。通过Gaussian程序B3LYP/def2TZVP理论方法计算RESP2电荷,sobtop软件生成乙醇及酯类力场参数,水分子采用扩展简单点电荷模型(simple point charge/extended,SPC/E)模型[26]。
分子模拟过程参考相关研究[7-8,12],具体流程如下:
(1)为模拟酯类物质在不同体积分数乙醇水溶液中的运动行为,使用Packmol软件[27]构建了一个尺寸为(100×100×100)Å3的立方体空间,并按照表2所示的分子数量和比例在该空间中填充分子。
表2 分子模拟过程各种体系中酯类、乙醇和水的分子数
Table 2 Molecular numbers of ester, ethanol and water molecules in various systems during molecular simulation process
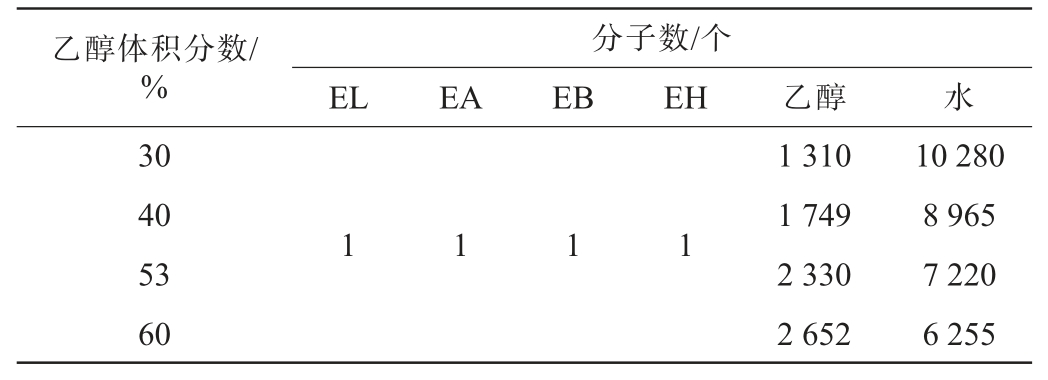
乙醇体积分数/%30 40 53 60分子数/个EL EA EB EH 乙醇 水1 1 1 1 1 310 1 749 2 330 2 652 10 280 8 965 7 220 6 255
(2)能量最小化:采用共轭梯度法(conjugate gradient,cg)进行能量最小化,以消除初始构型中可能存在的不合理原子接触或高能量构象,使体系达到更稳定的低能量状态。
(3)平衡阶段(逐步控温控压):系统在0~500 ps由0升温至498.15 K,在500~1 000 ps内由498.15 K降温至298.15 K,并在298.15 K下平衡2 ns。采用velocity-rescale热浴控温,采用Berendsen压浴控压(可压缩性=4.5×105 bar-1),在各方向同等条件下维持。
(4)生产阶段(温度体积恒定):平衡后,将模拟体系的尺寸调整为Lx=Ly=80 Å,Lz=160 Å。采用velocity-rescale热浴控温,并在298.15 K下模拟5 ns,每2 ps收集一次数据。
在平衡与生产阶段,采用LINCS算法约束氢键振动,同时施加全方向周期性边界条件,并基于(particle-mesh ewald,PME)方法处理长程静电相互作用(12 Å),范德华力则通过截断半径(12 Å)进行计算。
每组体系重复模拟5次,通过Gromacs内置程序分析化合物沿z轴密度分布,取5次模拟均值作为最终结果。体系可视化采用可视化分子动力学(visual molecular dynamics,VMD)程序。
1.3.5 香气阈值测定
从贵州仁怀茅台学院酿酒工程系挑选无吸烟史和味觉障碍的学生,按照国标GB/T 33404—2016《白酒感官品评导则》中所述方法,进行一个月的白酒风味物质(重点为EL、EA、EB、EH)闻香训练,最终选择其中10人(19~23岁,3男,7女)组建感官品评小组。
阈值测定参照GB/T 33406—2016《白酒风味物质阈值测定指南》和相关文献[4,28],采用最优估计阈值法测定不同体积分数乙醇水溶液中酯类香气阈值。配制相应酯类溶液,按酯类浓度上升次序依次进行三点选配法品评,计算每位评价员评价结果中判断错误的最大浓度与相邻更高一级浓度(判断正确)的几何平均值作为该品评员的测得阈值,最终取10人品评结果的算术均值作为化合物香气阈值。
1.3.6 统计分析
使用EPIWEB4.1软件计算酯类油水分配系数(logP),使用Origin 9.0软件制图,使用SPSS 25.0进行单因素方差分析。
2 结果与分析
2.1 乙醇对四种酯类挥发性影响
为了考察乙醇对白酒风味物质的影响,实验以白酒中四种关键酯类(EL、EA、EB、EH)为研究对象,基于白酒实际酒精度和四种酯类的浓度,设置30%、40%、53%、60%四个乙醇体积分数梯度以及50 mg/L、100 mg/L、250 mg/L、500 mg/L、1 000 mg/L、2 000 mg/L六个酯类质量浓度梯度,采用HS-SPME-GC-MS技术分析乙醇体积分数对四种关键酯类挥发性的影响,结果见图1。
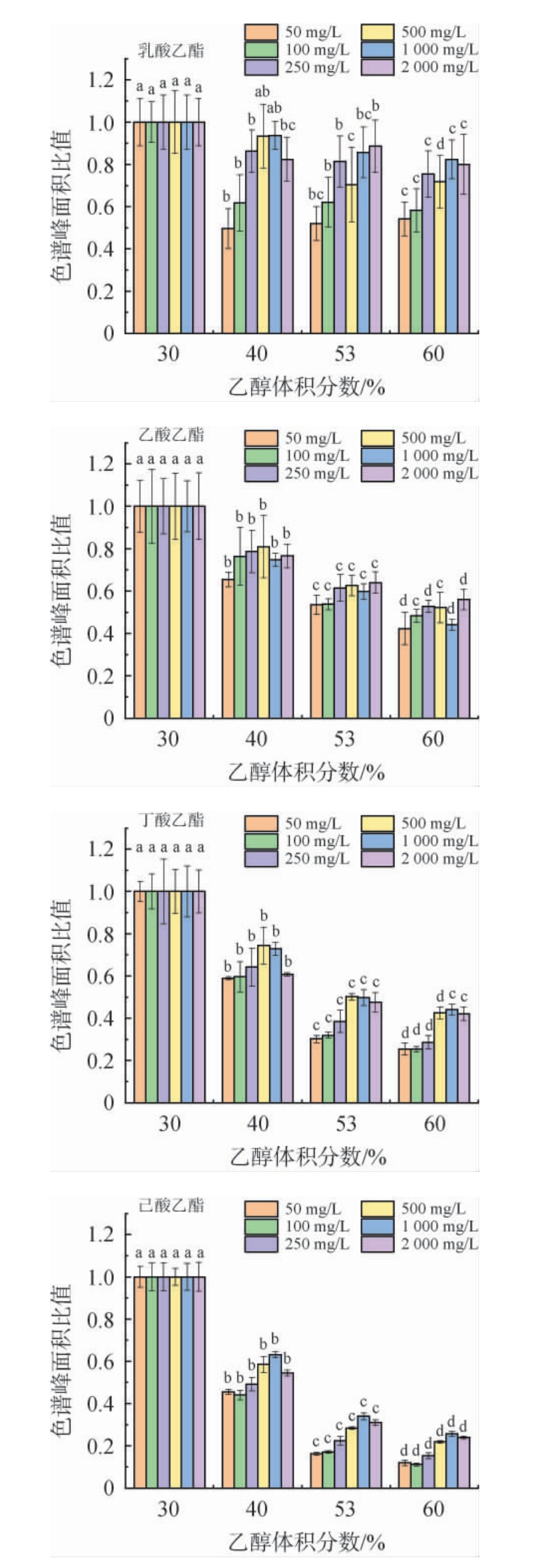
图1 不同体积分数乙醇对不同质量浓度的四种关键酯类挥发性的影响
Fig.1 Effect of different ethanol volume fractions on the volatility of four key esters with different mass concentrations
不同字母表示在不同乙醇体积分数下差异显著(P<0.05)。下同。
由图1可知,随着乙醇体积分数升高,四种酯类的含量(由相对色谱峰面积表征)均显著降低(P<0.05),且下降幅度也有较大差异。以质量浓度为50 mg/L的酯类为例,当乙醇体积分数从30%升至60%时,EL、EA、EB和EH的相对峰面积分别由1降至0.54、0.42、0.25和0.12。结合由EPIWEB4.1软件计算得出的油水分配系数(logPEL=-0.18,logPEA=0.73,logPEB=1.85,logPEH=2.83)可知,具有较高logP值的酯类受乙醇抑制作用更显著,该实验现象与之前研究结果一致[6]。推测原因是高体积分数乙醇使高logP值化合物更易溶入乙醇水溶液从而降低了挥发性。
进一步研究发现,随着酯类质量浓度升高,乙醇的抑制作用有减弱趋势。以EL为例,当其质量浓度从50 mg/L增至2 000 mg/L时,EL的相对峰面积由在体积分数30%乙醇水溶液中的1降至在体积分数60%乙醇水溶液中的0.54、0.58、0.75、0.71、0.82、0.80。参考KARLSSON B C G等[7]的研究,推测上述实验现象的成因可能包括以下两方面:①酯类物质在低浓度时更易溶于乙醇水溶液,随着酯类质量浓度增加,其溶解性能下降,因此容易释放;②酯类物质沸点相对较低,容易挥发。在其向顶空挥发过程中,乙醇与酯类分子竞争进入气相。随着酯类浓度增加,更多酯类分子进入气相,使顶空中挥发性物质的浓度趋于饱和,从而削弱了乙醇的抑制效果。
尽管酯类质量浓度的增加可在一定程度上削弱乙醇的抑制效果,但乙醇对酯类物质挥发性的抑制作用仍占主导地位。为深入探讨其机理,采用量子化学和分子动力学模拟方法进行解析。
2.2 乙醇对四种酯类抑制作用的机理分析
根据已有研究表明,乙醇对风味组分的抑制作用与其在溶液中的溶解性能密切相关[3]。为了深入分析该结论的理论机制,实验通过量子化学方法计算四种关键酯类物质分别在乙醇和水溶液中的溶解自由能,结果见表3。溶解自由能表征溶质与溶剂的亲合度,该负值数值越大表明溶质与溶剂之间的亲和性越高。
表3 四种关键酯类物质的在乙醇和水中的溶解自由能
Table 3 Solvation free energy of four key esters in ethanol and water

酯类 乙醇中ΔGsolv/(kcal·mol-1)水中ΔGsolv/(kcal·mol-1)两相ΔGsolv差值EL EA EB EH-7.55-5.25-6.28-7.31-5.67-3.17-2.77-2.40-1.88-2.07-3.52-4.92
由表3可知,在四种酯类中,EL在乙醇和水中的溶解自由能分别为-7.55 kcal/mol和-5.67 kcal/mol,说明其在两种溶剂中的溶解性能较好。EH在水中的溶解自由能最低,仅为-2.40 kcal/mol,表现出较强的疏水性。进一步计算它们在乙醇和水中溶解自由能的差值,得出EL、EA、EB和EH的两相ΔGsolv分别为-1.88、-2.07、-3.52和-4.92。该负值数值越大,表明酯类在两种溶剂中的溶解度差异越大。由此可知,在四种酯类中,EL在乙醇和水中的溶解度差异最小,因此乙醇体积分数的增加对其溶解性影响最小,抑制效果最弱;其次是EA和EB;相比之下,EH的溶解度差异最大,说明其在乙醇中溶解性能显著优于水中,因此乙醇体积分数的增加对其溶解性影响最大,抑制效果最强。
为了进一步分析乙醇对4种关键酯类的抑制机理,实验采用分子动力学模拟考察四种酯分子在体积分数30%、40%、53%、60%乙醇水溶液中的密度分布。分子模拟采用GAFF力场与SPC/E水模型,为验证力场准确性,实验首先对四种酯类单体以及不同体积分数的乙醇水溶液进行模拟(298.15 K),通过轨迹分析得到模拟密度,将它们与PubChem数据库和工具书籍[29]中实验值进行比较,并计算相对误差,结果见表4。由表4可知,相对误差<1.5%,表明GAFF+RESP2力场组合可较为准确地描述目标体系的物理性质。
表4 四种关键酯类单体与不同体积分数乙醇水溶液的模拟密度与实验密度对比
Table 4 Comparison of simulated and experimental densities of four key ester monomers and ethanol-water solutions at different volume fractions
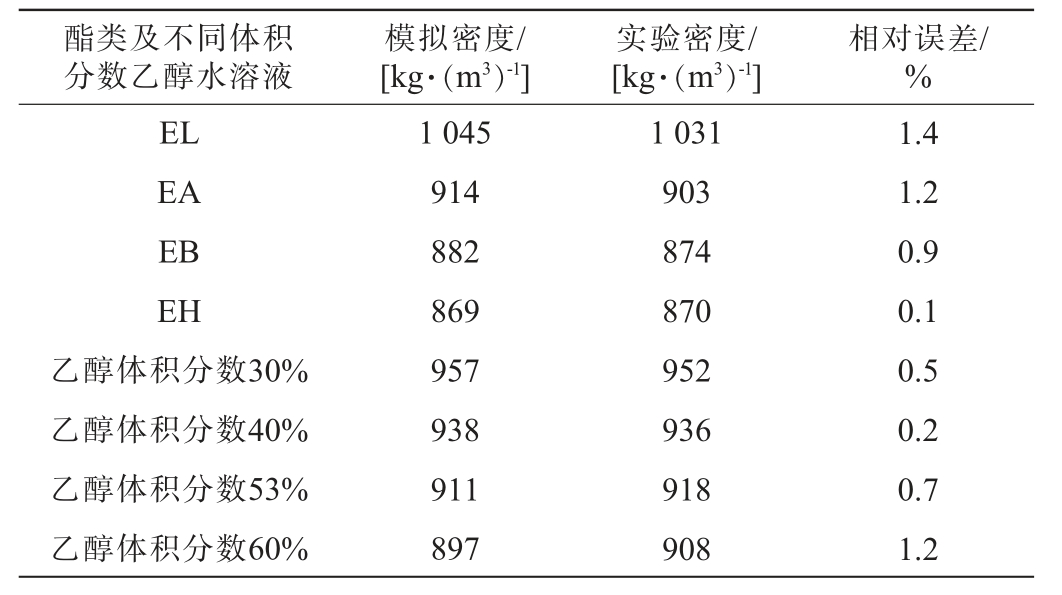
酯类及不同体积分数乙醇水溶液模拟密度/[kg·(m3)-1]实验密度/[kg·(m3)-1]相对误差/%EL EA EB EH乙醇体积分数30%乙醇体积分数40%乙醇体积分数53%乙醇体积分数60%1 045 914 882 869 957 938 911 897 1 031 903 874 870 952 936 918 908 1.4 1.2 0.9 0.1 0.5 0.2 0.7 1.2
基于上述力场验证结果,按表2所述分子数构建四种酯类溶解在不同体积分数乙醇水溶液中的混合体系,模拟体系初始体积为(100×100×100)Å3,经平衡后将体系压缩至(80×80×80)Å3。为了模拟风味物质挥发,将该体系沿z轴方向扩展至160 Å建立真空区域,使其体积为(80×80×160)Å3,形成气液界面。气液界面位于Lz=±40 Å,溶液中心位于Lz=0 Å,并在温度体积恒定条件下进行模拟,以EA为例,具体动力学模拟结果见图2。图2A展示了EA在体积分数53%乙醇水溶液中的分子模拟,图2B为EA、乙醇和水分子沿z轴的密度分布。由图2B可见,EA和乙醇在界面处(Lz=±40 Å)密度较高,表明二者主要富集于气液界面。这归因于EA和乙醇沸点较低,易于向气相区域迁移,从而在界面处形成高密度分布。
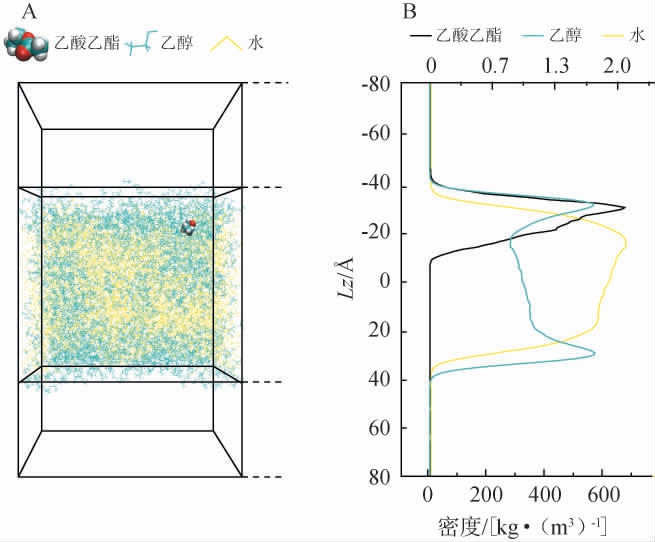
图2 体积分数53%乙醇水溶液在温度体积恒定条件下的全原子分子动力学模拟(以乙酸乙酯为例)
Fig.2 Full-atomic molecular dynamics simulation of volume fraction 53% ethanol aqueous solution under constant temperature and volume conditions (exemplified by ethyl acetate)
A:乙酸乙酯分子以范德华力(VDW)模型表示,乙醇与水分子以线型模型表示;B:乙酸乙酯、乙醇及水分子沿z轴的分子分布;左图模拟体系尺寸与气液界面位置对应于右图z轴坐标。
完成四种酯类在不同体积分数乙醇水溶液中的分子模拟后,获得了各组分沿z轴的密度分布曲线,如图3所示。
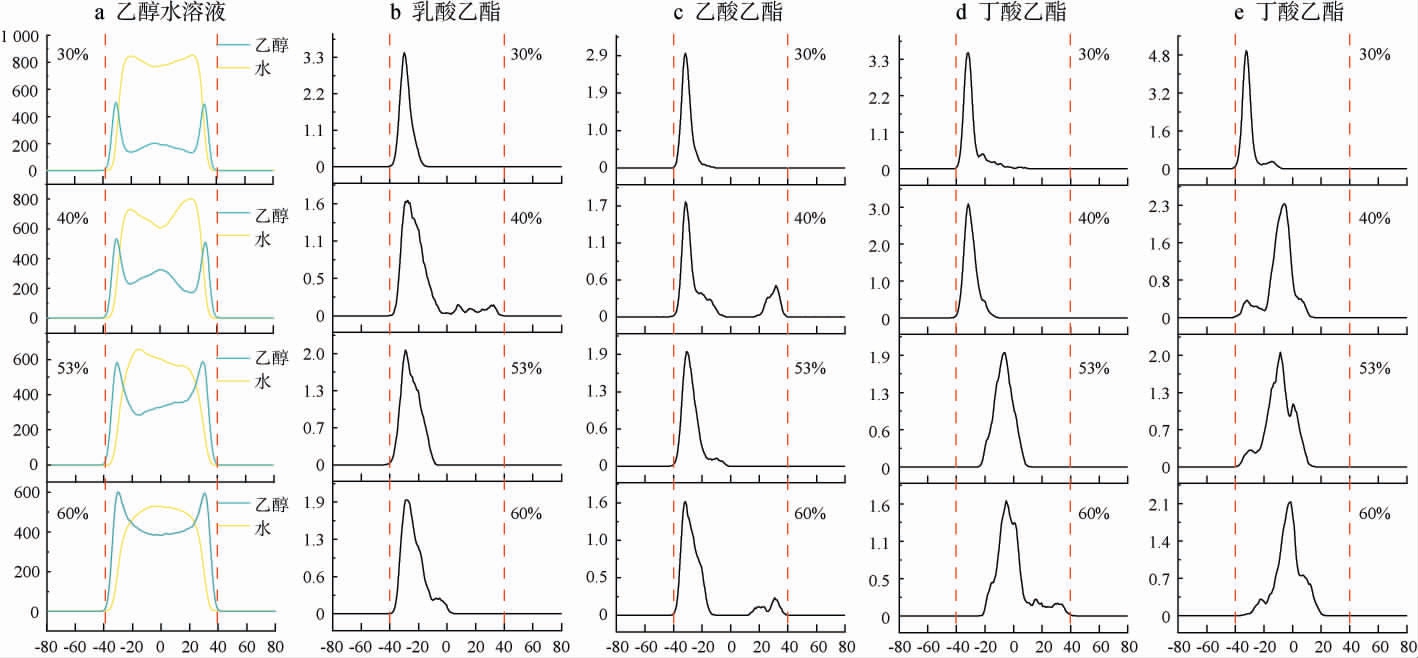
图3 不同体积分数乙醇水溶液中乙醇与水分子(a)及四种关键酯类(b~e)沿z轴的密度分布曲线
Fig.3 Density distribution curves of ethanol and water molecules (a) and four key esters (b-e) along the z-axis in the ethanol water solutions with different volume fractions
红色虚线表示气液界面。所有纵坐标为密度/(kg·m-3),所有横坐标为Lz=0Å。
由图3a可知,乙醇水溶液中由于每个模拟体系中仅含一个酯类分子,其存在对乙醇和水的分布影响可忽略,因此不同酯类体系中的乙醇和水分布曲线无明显差异。模拟结果表明,随着乙醇体积分数增加,其在z轴中心区域(Lz=0 Å)的密度显著上升,从乙醇体积分数30%时的近200 kg/m3增至乙醇体积分数60%时的近400 kg/m3,表明乙醇分子逐渐向溶液内部富集(图3a),该变化趋势与KARLSSON B C G等[7-8]的研究研究相符。由图3b~e可知,由于每个体系中仅有一个酯类分子,其在模拟过程中随机趋向于某一气液界面,因此分布曲线关于Lz=0 Å不对称。当乙醇体积分数为30%时,四种酯类分子均主要富集于气液界面附近(Lz=-40 Å)。随着乙醇体积分数增至60%,EL和EA仍主要分布于界面处,而EB和EH则逐渐从界面迁移至溶液中心区域(Lz=0 Å),其密度分布曲线呈现较宽峰型,变化趋势与乙醇分子向溶液内部富集的趋势一致。
进一步结合表3中四种关键酯类的溶解自由能差值分析其密度分布,由于EL和EA在乙醇和水的溶解度差异较小,它们对溶解于乙醇或水没有明显的倾向性,因此,乙醇体积分数的增加没有明显影响EL和EA在溶液中的分布,它们仍分布于易于化合物挥发的气液界面,乙醇对其挥发性抑制效果相对较弱。而EB和EH在乙醇和水的溶解度差异较大,它们更倾向于溶于乙醇,因此,随着乙醇体积分数的增加,EB和EH的分布逐渐从易于化合物挥发的气液界面迁移至较难挥发的溶液中心区域,导致其挥发性受到显著抑制。以上研究表明,同系化合物在乙醇和水溶液中的溶解自由能差值,可作为评估其挥发性受乙醇抑制效果强弱的潜在指标。
2.3 乙醇对四种酯类的香气阈值影响
上述研究分别从实验和理论计算角度分析了乙醇对酯类物质挥发性的抑制作用,实验进一步通过感官品评考察乙醇对四种酯类物质香气强度的具体影响。不同酯类物质在不同溶剂中的香气阈值存在显著差异,因此,该研究在乙醇体积分数为30%、40%、53%和60%的水溶液中测定了四种关键酯类的香气阈值,结果见表5。
表5 四种关键酯类物质在不同体积分数乙醇水溶液中的香气阈值
Table 5 Aroma threshold four key esters in ethanol aqueous solutions with different volume fractions
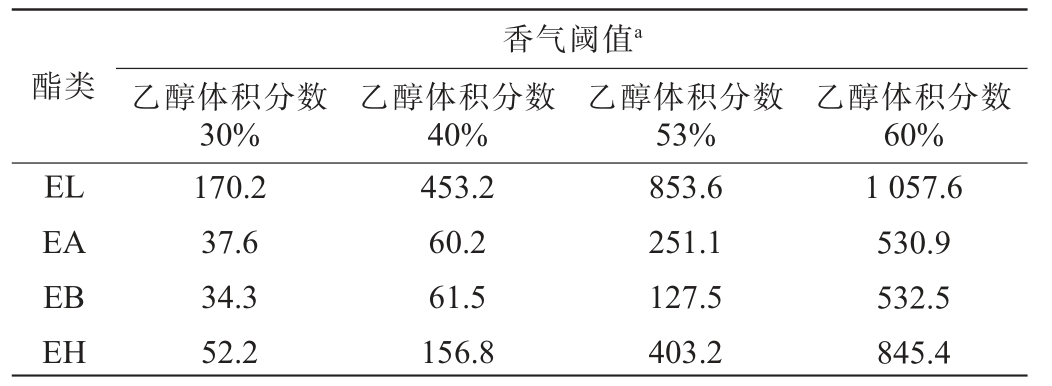
注:a表示EL和EA的香气阈值单位为mg/L,EB和EH的香气阈值单位为μg/L。
酯类香气阈值a乙醇体积分数30%乙醇体积分数40%乙醇体积分数53%乙醇体积分数60%EL EA EB EH 170.2 37.6 34.3 52.2 453.2 60.2 61.5 156.8 853.6 251.1 127.5 403.2 1 057.6 530.9 532.5 845.4
由表5可知,四种关键酯类物质的香气阈值随着乙醇体积分数的增加而逐步增加。在体积分数60%乙醇水溶液中,EL、EA、EB及EH的阈值较体积分数30%乙醇水溶液分别增加约6倍、14倍、15倍和16倍,表明乙醇通过抑制酯类物质的释放,减弱了气味强度,这可能是导致香气阈值升高的重要原因之一。同时,实验也发现香气阈值的增加倍数与乙醇对酯类的抑制效果之间并未表现出明显相关性。例如,EL和EA均表现出相对较弱的乙醇抑制效应,但它们的香气阈值增加倍数却存在明显差异(分别为6倍和14倍),由此可知风味物质的挥发性并不是影响其香气阈值的唯一因素。
3 结论
该研究采用实验、理论计算和感官品评,深入探讨了不同体积分数乙醇对白酒中四种关键酯类(乳酸乙酯、乙酸乙酯、丁酸乙酯和己酸乙酯)挥发性抑制作用的分子机制。结果表明,乙醇能抑制酯类物质的挥发性,而随着酯类物质质量浓度的增加,能相对减弱乙醇的抑制效果;通过量子化学与分子动力学模拟,将酯类物质溶解自由能与它们在乙醇水溶液中的分布相结合,讨论乙醇的抑制机制,解释了酯类在乙醇和水中的溶解度差异越大,其受到乙醇的抑制作用就越显著的原因;感官品评结果表明,乙醇体积分数的升高明显提升了四种酯类物质的香气阈值,表明乙醇通过抑制酯类物质的释放而降低了其香气强度。然而,该实验仅聚焦于4种酯类化合物,尚未分析醇类、酸类等其它风味组分,因此,乙醇对不同种类物质的抑制作用是否存在差异,以及溶解自由能差值能否表征乙醇对不同类别化合物抑制效果的通用指标,仍需进一步的研究。
[1]JIN G, ZHU Y, XU Y.Mystery behind Chinese liquor fermentation[J].Trends Food Sci Tech,2017,63:18-28.
[2]LIU H L, SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].J Agr Food Chem,2018,66(22):5425-5432.
[3]ICKES C M,CADWALLADER K R.Effects of ethanol on flavor perception in alcoholic beverages[J].Chemosen Percept,2017,10(4):119-134.
[4]LU J,ZHENG J,ZHAO D,et al.The effect of ethanol on the compound thresholds and aroma perception in Chinese Baijiu[J].Molecules, 2025,30(4):933.
[5]YANG X,ZHENG J,LUO X,et al.Ethanol-water clusters determine the critical concentration of alcoholic beverages[J].Matter,2024,7(5):1724-1735.
[6]BOOTHROYD E L,LINFORTH R S T,COOK D J.Effects of ethanol and long-chain ethyl ester concentrations on volatile partitioning in a Whisky model system[J].J Agr Food Chem,2012,60(40):9959-9966.
[7]KARLSSON B C G, FRIEDMAN R.Dilution of whisky-the molecular perspective[J].Sci Rep,2017,7(1):6489.
[8]SHUTTLEWORTH E E, APÓSTOLO R F, CAMP P J, et al.Molecular dynamics simulations of flavour molecules in scotch whisky[J].J Mol Liquid,2023,383:122152.
[9]QIN D,DUAN J,SHEN Y,et al.Flavor perception and formation mechanism of empty cup aroma in soy sauce aroma Type Baijiu[J].J Agr Food Chem,2024,72(30):16955-16965.
[10] 黄张君,张文华,曾运航,等.白酒贮存过程中主要成分间氢键相互作用的量子化学计算[J].食品科学,2021,42(12):45-51.
[11]ZHANG Q,SHI J,WANG Y,et al.Research on interaction regularities and mechanisms between lactic acid and aroma compounds of Baijiu[J].Food Chem,2022,397:133765.
[12]LIU Q R,LIN X L,LU Z M,et al.Influence on the volatilization of ethyl esters: Nonnegligible role of long-chain fatty acids on Baijiu flavor via intermolecular interaction[J].Food Chem,2024,436:137731.
[13]LIU Y,XI H,FU Y,et al.Effects of organic acids on the release of fruity esters in water: An insight at the molecular level[J].Molecules, 2022,27(9):2942.
[14]XIAO Z,QU H,MAO C,et al.Study on the sweetening mechanism of aroma compounds in yangshan peach using sensory analysis,molecular docking,and molecular dynamics simulation techniques[J].LWT-Food Sci Technol,2024,191:115562.
[15]ZHENG X, PAN F, ZHAO S, et al.Phenolic characterization, antioxidant and α-glycosidase inhibitory activities of different fractions from Prinsepia utilis Royle seed shell using in vitro and in silico analyses[J].Eur Food Res Technol,2023,249(2):375-386.
[16]CHEN L,YANG Y,HU X,et al.Unraveling the role of peanut protein in Baijiu-peanut pairing flavor complexity: A focus on ethanol-induced denaturation[J].Food Chem,2025,463:141181.
[17]XIAO Z, SHEN T, KE Q, et al.Identification of characteristic aroma compounds of Longjing tea and their molecular mechanisms of interaction with olfactory receptors using molecular docking[J].Eur Food Res Technol,2024,250(5):1363-1378.
[18]GRIMME S,ANTONY J,EHRLICH S,et al.A consistent and accurate ab initio parametrization of density functional dispersion correction(DFT-D)for the 94 elements H-Pu[J].J Chem Phys,2010,132(15).
[19]KRISHNAN R, BINKLEY J S, SEEGER R, et al.Self-consistent molecular orbital methods.XX.A basis set for correlated wave functions[J].J Chem Phys,1980,72(1):650-654.
[20]MARENICH A V,CRAMER C J,TRUHLAR D G.Universal solvation model based on the generalized born approximation with asymmetric descreening[J].J Chem Theory Comput,2009,5(9):2447-2464.
[21]ZHAO Y,TRUHLAR D G.A new local density functional for main-group thermochemistry, transition metal bonding, thermochemical kinetics,and noncovalent interactions[J].J Chem Phys,2006,125(19):194101.
[22]MARENICH A V,CRAMER C J,TRUHLAR D G.Universal solvation model based on solute electron density and on a continuum model of the solvent defined by the bulk dielectric constant and atomic surface tensions[J].J Phys Chem B,2009,113(18):6378-6396.
[23]ABRAHAM M J,MURTOLA T,SCHULZ R,et al.GROMACS: High performance molecular simulations through multi-level parallelism from laptops to supercomputers[J].Software X,2015,1:19-25.
[24]WANG J,WOLF R M,CALDWELL J W,et al.Development and testing of a general amber force field[J].J Comput Chem,2004,25(9):1157-1174.
[25]SCHAUPERL M,NERENBERG P S,JANG H,et al.Non-bonded force field model with advanced restrained electrostatic potential charges(RESP2)[J].Commun Chem,2020,3(1):44.
[26]BERENDSEN H J,GRIGERA J R,STRAATSMA T P.The missing term in effective pair potentials[J].J Phys Chem,1987,91(24):6269-6271.
[27]MARTÍNEZ L,ANDRADE R,BIRGIN E G,et al.PACKMOL:A package for building initial configurations for molecular dynamics simulations[J].J Comput Chem,2009,30(13):2157-2164.
[28]WANG L, ZHU L, ZHENG F, et al.Determination and comparison of flavor(retronasal)threshold values of 19 flavor compounds in Baijiu[J].J Food Sci,2021,86(5):2061-2074.
[29]王福荣.酿酒分析与检测(第二版)[M].北京:化学工业出版社,2012:320-330.