乳酸菌是一类革兰氏阳性菌,因其“非致病性”被归类为“公认安全”(generally recognized as safe,GRAS)的微生物,是食品工业中最重要的细菌类群之一,传统发酵食品如酸奶、泡菜、豆豉、酸浆等是乳酸菌的主要来源[1]。乳酸菌具有改善消化和肠道健康、降低炎症水平、降低胆固醇水平、抗氧化、抗癌等多重有益功能,近年来随着营养健康理念深入人心,乳酸菌也备受关注,被广泛用作益生菌添加到食品中[2-3]。
酸浆是豆类或薯类等农作物加工过程中,自然发酵形成的一种乳白色、酸性浆状产物,微生物多样性组成丰富。范鑫诺等[4]利用高通量测序技术探究了6家洛阳传统绿豆酸浆的微生物群落组成,共鉴定出8个细菌门,涉及75个属和106个种,其中乳杆菌属和乳球菌属为优势菌属;吴鹏宇等[5]从9份洛阳传统绿豆酸浆中分离鉴定得到24株乳酸菌,涉及10个属,12个种,其中发酵乳杆菌分离株数量最多;李璇等[6]探究了绿豆酸浆发酵过程中氨基酸、有机酸等物质的变化,结果表明,发酵过程中的游离氨基酸总量最高可达1 718.56 mg/mL,甘氨酸、谷氨酸和亮氨酸是含量较高的三种氨基酸。
胞外多糖是乳酸菌生长代谢过程中分泌到细胞壁外的一类糖类化合物,乳酸菌的益生功能大多与其分泌的胞外多糖相关。ZHANG M等[7]研究发现,高产胞外多糖的植物乳杆菌(Lactobacillus plantarum)YW11通过调节肠道微生物群中的关键门,成功改善衰老小鼠模型中的氧化应激表型。LIU Y等[8]研究表明,在衰老小鼠模型中,摄入瑞士乳杆菌(Lactobacillus helveticus)KLDS1.8701产生的胞外多糖后,显著减轻了肝损伤和氧化应激,同时肠道微生物群中氧化应激相关细菌减少,证实了胞外多糖的抗氧化活性与肠道微生物群调节的相关性。胞外多糖还可通过增强小鼠肝细胞和红细胞中超氧化物歧化酶、谷胱甘肽过氧化物酶和过氧化氢酶的活性,并降低丙二醛水平,提高机体的抗氧化能力[9]。由此可见,挖掘高产胞外多糖的乳酸菌资源并促进其在食品工业中的广泛应用具有重要意义。
本研究从河南省洛阳市收集了120余份传统发酵酸浆原料,从中筛选高产胞外多糖的乳酸菌,对筛选菌株进行形态学观察及分子生物学鉴定,并评价其耐胃液、耐胆盐、抑菌、抗生素敏感性和抗氧化等益生功能,旨在为益生菌在食品工业中的开发利用提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 原料
洛阳传统酸浆原料(120余份):收集自洛阳市及周边县区农户家中。金黄色葡萄球菌(Staphylococcus aureus):河南省食品微生物工程技术研究中心保存。
1.1.2 试剂
无水乙醇、硫酸、苯酚、过氧化氢溶液、水杨酸、三氯乙酸、维生素C(vitamin C,VC)、硫酸亚铁、过硫酸钾(均为分析纯):天津市德恩化学试剂有限公司;细菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒、20000 DNA Marker、1,1-二 苯 基-2-三 硝 基 苯 肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)、2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)、牛胆盐(均为分析纯)、胃蛋白酶(酶活250 U/mg)、阿莫西林、头孢氨苄:北京索莱宝科技有限公司。
1.1.3 培养基
MRS液体培养基:蛋白胨10 g/L,牛肉膏10 g/L,酵母浸粉5 g/L,葡萄糖20 g/L,无水醋酸钠5 g/L,磷酸氢二钾2 g/L,七水硫酸镁0.5 g/L,四水硫酸锰0.25 g/L,柠檬酸二胺2 g/L,吐温-80 1 mL,蒸馏水1 000 mL。
MRS固体培养基:MRS液体培养基中加入20 g/L琼脂粉。
初筛培养基:MRS固体培养基中添加0.5%碳酸钙。
LB液体培养基:胰蛋白胨10 g/L、NaCl 10 g/L、酵母提取物5 g/L。
上述培养基均于121 ℃条件下灭菌20 min。
1.2 仪器与设备
SW-CJ-2FD超净工作台:苏州安泰空气技术有限公司;YXQ-LS-50S11高压蒸汽灭菌锅、BSD-YX2200立式双层智能精密摇床:上海博讯实业有限公司医疗设备厂;SPX-TW生化培养箱:上海仙象仪器仪表有限公司;HR/T20M台式高速冷冻离心机:湖南赫西仪器装备有限公司;JY300E电泳仪:北京君意东方电泳设备有限公司;Biometra Tone 96G基因扩增仪:德国耶拿分析仪器有限公司;SPARK多功能酶标仪:Tecan集团奥地利有限责任公司。
1.3 方法
1.3.1 乳酸菌初筛
分别取不同发酵酸浆原液样品100 μL,用无菌生理盐水依次进行10倍梯度稀释,得到10-1~10-6六个稀释度的稀释液,每个稀释度吸取100 μL涂布到初筛培养基上,将涂布后的平板置于37 ℃恒温培养箱中培养24~48 h,期间观察菌落的形态特征。乳酸菌产生的酸性物质可与培养基中的碳酸钙反应使碳酸钙溶解,菌落周围形成可见的溶钙圈。根据是否有溶钙圈初步筛选乳酸菌,挑选乳酸菌单菌落至MRS液体培养基中,摇床过夜培养,待培养基浑浊后进行平板划线,得到单一菌落的平板。
1.3.2 高产胞外多糖乳酸菌复筛
胞外多糖的提取参照乔少婷等[10]的方法进行。将初筛各菌株接种至50 mL MRS液体培养基中,37 ℃条件下培养24 h后离心(5 000 r/min,15 min)除去菌体,上清经沸水浴10 min,冷却至室温后加入质量分数为80%的三氯乙酸溶液至终质量分数为6%,4 ℃静置12 h后离心(5 000 r/min,20 min),除去蛋白沉淀,然后向上清液中加入3倍体积的无水乙醇,于4 ℃静置12 h,离心(5 000 r/min,20 min)收集粗多糖沉淀。将沉淀溶解于5 mL蒸馏水中,使用截留分子质量为8 000~14 000 Da的透析袋透析72 h,期间每隔8 h换水一次,将得到的胞外多糖透析液4 ℃保存备用。
1.3.3 胞外多糖产量测定
胞外多糖产量测定采用硫酸-苯酚法[11]。以葡萄糖含量(x)为横坐标,吸光值(y)为纵坐标,绘制葡萄糖标准曲线,得到标准曲线回归方程y=1.036 2x+0.000 4,相关系数R2为0.999 1。
分别取1 mL胞外多糖透析液,加入1 mL 5%的苯酚溶液及5 mL浓硫酸,静置反应20~30 min,于波长490 nm处测量吸光度值,按照葡萄糖标准曲线回归方程计算各菌株胞外多糖产量。
1.3.4 筛选菌株鉴定
(1)形态学观察
根据胡此海等[12]的方法对乳酸菌进行形态学观察,取适量菌液进行革兰氏染色,于显微镜下观察菌株形态。
(2)分子生物学鉴定
采用细菌基因组DNA提取试剂盒提取复筛得到的乳酸菌基因组DNA,具体操作按照说明书进行。采用琼脂糖凝胶电泳法检测所提基因组DNA的纯度,点样量5 μL,电泳条件100 V、30 min。将提取的基因组DNA作为聚合酶链式反应(polymerase chain reaction,PCR)扩增模板,上、下游引物分别选择通用引物27F和1492R。PCR扩增体系(25 μL):Mix-Taq酶12.5 μL,模板DNA 1.0 μL,正向引物(27F)0.5 μL,反向引物(1492R)0.5 μL,双蒸水(ddH2O)10.5 μL。PCR扩增程序:94 ℃预变性3 min;98 ℃变性10 s,62℃退火30s,72℃延伸45s,共35个循环;72℃再延伸5 min。将PCR产物送至生工生物工程(上海)股份有限公司测序。测序所得16S rDNA基因序列提交至美国国家生物技术信息中心(National Center of Biotechnology Information,NCBI)的GenBank数据库中进行基本局部比对搜索工具(basic local alignment search tool,BLAST)比对同源性分析,采用MEGA 7.0软件分析,通过邻接(neighbor-joining,NJ)法构建系统发育树。
1.3.5 筛选菌株益生特性评价
(1)耐受模拟胃液能力
取1 mol/L HCl溶液20 mL,用NaOH溶液调pH至2.0,加入胃蛋白酶使其终质量浓度为1 g/100 mL,经0.22 μm微孔滤膜过滤除菌制成模拟胃液。将所筛选的乳酸菌接种至MRS液体培养基培养至对数期后,取1 mL菌悬液,利用平板计数法测定初始活菌数,另取1 mL菌悬液加入9 mL模拟胃液中,振荡摇匀,放入摇床中培养3 h,用平板计数法测定3 h的活菌数,与初始活菌数相比计算菌株在模拟胃液培养3 h时的存活率[13]。
(2)耐受胆盐能力
配制牛胆盐含量分别为0、0.015%、0.030%、0.060%的MRS液体培养基,115 ℃高压蒸汽灭菌30 min,将复筛乳酸菌分别接种至不同梯度胆盐质量浓度的MRS液体培养基中,培养24 h后测定波长600 nm处的吸光度值,对比各菌株在不同含量牛胆盐环境下存活率[14]。
(3)体外抑菌能力
将金黄色葡萄球菌(Staphylococcus aureus)按1%(V/V)的比例接种于LB液体培养基中,摇瓶培养(37 ℃、180 r/min)6 h至对数期,取100 μL金黄色葡萄球菌菌液涂布在MRS固体培养基上,将牛津杯分散放置在MRS固体培养基上,将所筛选的乳酸菌单菌落接种至MRS液体培养基培养至对数期后,分别取200 μL菌液注入牛津杯中,37℃培养48 h后测量抑菌圈直径,以评估待测菌株的体外抑菌能力,抑菌圈直径越大代表菌株的抑菌能力越强[15]。
(4)抗生素敏感性
将阿莫西林和头孢氨苄分别用无菌水稀释得到5μg/mL、10 μg/mL、15 μg/mL、20 μg/mL、25 μg/mL和30 μg/mL的两种药品溶液。将所筛选的乳酸菌单菌落接种至MRS液体培养基培养至对数期后,分别取100 μL待测菌液涂布于MRS固体培养基上,然后将两张圆形滤纸片放置在培养基两侧,分别滴加10 μL不同质量浓度的两种药品溶液到滤纸片上,于37 ℃培养箱中培养48 h后测定抑菌圈直径,以评估待测菌株的抗生素敏感性,抑菌圈直径越大代表菌株的抗生素敏感性越高[16]。
(5)菌株发酵液的体外抗氧化能力
DPPH自由基清除率测定:将所筛选的乳酸菌接种至MRS液体培养基培养至对数期后,5 000 r/min离心10 min,取上清1 mL,加入1 mL 0.2 mmol/L DPPH自由基-乙醇溶液,在室温下避光反应30 min后离心(5 000 r/min,10 min),于波长517 nm处测定吸光度值,以2 mg/mL的抗坏血酸作为阳性对照[17]。DPPH自由基清除率计算公式如下:
式中:Ai为DPPH自由基-乙醇溶液与样品溶液反应的吸光度值;Aj为无水乙醇与样品溶液反应的吸光度值;Ac为蒸馏水与DPPH自由基-乙醇溶液反应的吸光度值。
ABTS自由基清除率测定:称取0.115 2 g ABTS溶于磷酸盐缓冲液(phosphate buffer solution,PBS)(pH 7.4)中,将20 mg的K2SO8添加到ABTS溶液中并避光反应12 h,制成ABTS储备液,使用前用PBS将ABTS溶液稀释至波长734 nm处吸光度值为0.700±0.020,制成ABTS工作液。将所筛选的乳酸菌接种至MRS液体培养基培养至对数期后,5 000 r/min离心10 min,取上清200 μL,加入800 μL ABTS工作液,在黑暗中反应5 min,在波长734 nm处测定吸光度值,以2 mg/mL的抗坏血酸作为阳性对照[17]。ABTS自由基清除率计算公式如下:
式中:Ai为ABTS与样品溶液反应的吸光度值;Aj为蒸馏水与样品溶液反应的吸光度值;Ac为ABTS与蒸馏水反应的吸光度值。
羟自由基清除率测定:将所筛选的乳酸菌接种至MRS液体培养基培养至对数期后,5 000 r/min离心10 min,取上清1 mL,加入1 mL 6 mmol/L的硫酸亚铁溶液,1 mL 1%的过氧化氢溶液,混匀静置15 min,再加入2 mL 6 mmol/L的水杨酸溶液,混匀,于37 ℃反应30 min,3 000 r/min离心10 min,取上清于波长510 nm处测定吸光度值。以2 mg/mL的抗坏血酸作为阳性对照[17]。羟自由基清除率计算公式如下:
式中:A0为以纯水代替样品的吸光度值;Ai为样品溶液的吸光度值;Aj为不含样品和过氧化氢的吸光度值。
1.3.6 数据处理与统计分析
所有试验均设3次平行,数值以“平均值±标准差”表示。采用SPSS 25.0软件对试验数据进行分析,选择描述性单因素方差分析(analysis of variance,ANOVA),在均值95%的置信区间对数据进行显著性分析,P<0.05表示差异显著。采用Graph-Pad Prism 8.0软件绘图。
2 结果与分析
2.1 高产胞外多糖乳酸菌菌株筛选与鉴定
2.1.1 乳酸菌初筛
从洛阳传统发酵酸浆中筛选乳酸菌,根据菌落“溶钙圈”特征初筛,得到20余株疑似乳酸菌,经胞外多糖产量测定,进一步筛选得到5株高产胞外多糖的乳酸菌,编号分别为L01~L05,菌株L01~L05的菌落及细胞形态见图1。由图1a可知,5株菌的菌落形态均为椭圆形或圆形,乳白色,凸起,湿润有光泽,边缘整齐,菌落周围形成透明“溶钙圈”。由图1b可知,菌株细胞形态均为杆状,且分散不相连,符合乳酸菌的典型特征。
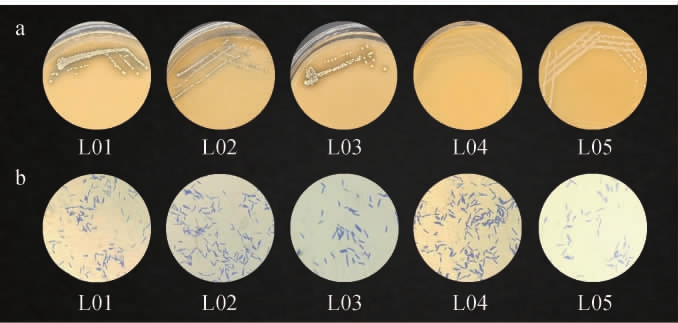
图1 5株筛选乳酸菌的菌落(a)和细胞(b)形态
Fig.1 Colony (a) and cell (b) morphology of 5 screened strains of lactic acid bacteria
2.1.2 筛选菌株胞外多糖产量
5株筛选菌株胞外多糖产量测定结果见图2。由图2可知,五株乳酸菌的胞外多糖产量均>0.45 g/L,且存在显著差异(P<0.05)。其中,菌株L04的胞外多糖产量最高,为0.73g/L,其次是菌株L01和L05,胞外多糖产量分别为0.56g/L和0.50 g/L,菌株L02和L03胞外多糖产量较低,为0.46 g/L左右。李悦等[18]从四川传统发酵腊肉和泡菜中分离得到3株高产胞外多糖乳酸菌,多糖产量最高为0.14 g/L。陈靖等[19]从湖南山区牧场的牛乳中筛选得到10株高产胞外多糖乳酸菌,产量均在0.6 g/L左右,与本实验筛选乳酸菌胞外多糖产量相当。
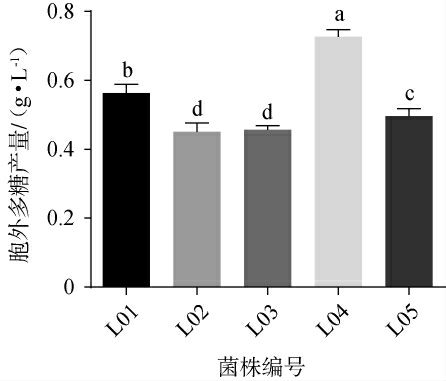
图2 5株筛选乳酸菌胞外多糖产量测定结果
Fig.2 Determination results of exopolysaccharide yield of 5 screened strains of lactic acid bacteria
不同字母表示差异显著(P<0.05)。下同。
2.1.3 筛选菌株分子生物学鉴定
5株乳酸菌的系统发育树构建结果见图3。由图3可知,菌株L01与植物乳植杆菌(Lactiplantibacillus plantarum)JCM1149相似度最高且与菌株L02、L03属同一分支,菌株L04与发酵粘液乳杆菌(Limosilactobacillus fermentum)NBRC15885相似度最高,菌株L05与鼠李糖乳杆菌(Lacticaseibacillus rhamnosus)NBRC3425相似度最高。因此,菌株L01、L02、L03被鉴定为植物乳植杆菌(Lactiplantibacillus plantarum),菌株L04被鉴定为发酵粘液乳杆菌(Limosilactobacillus fermentum),菌株L05被鉴定为鼠李糖乳杆菌(Lacticaseibacillus rhamnosus)。
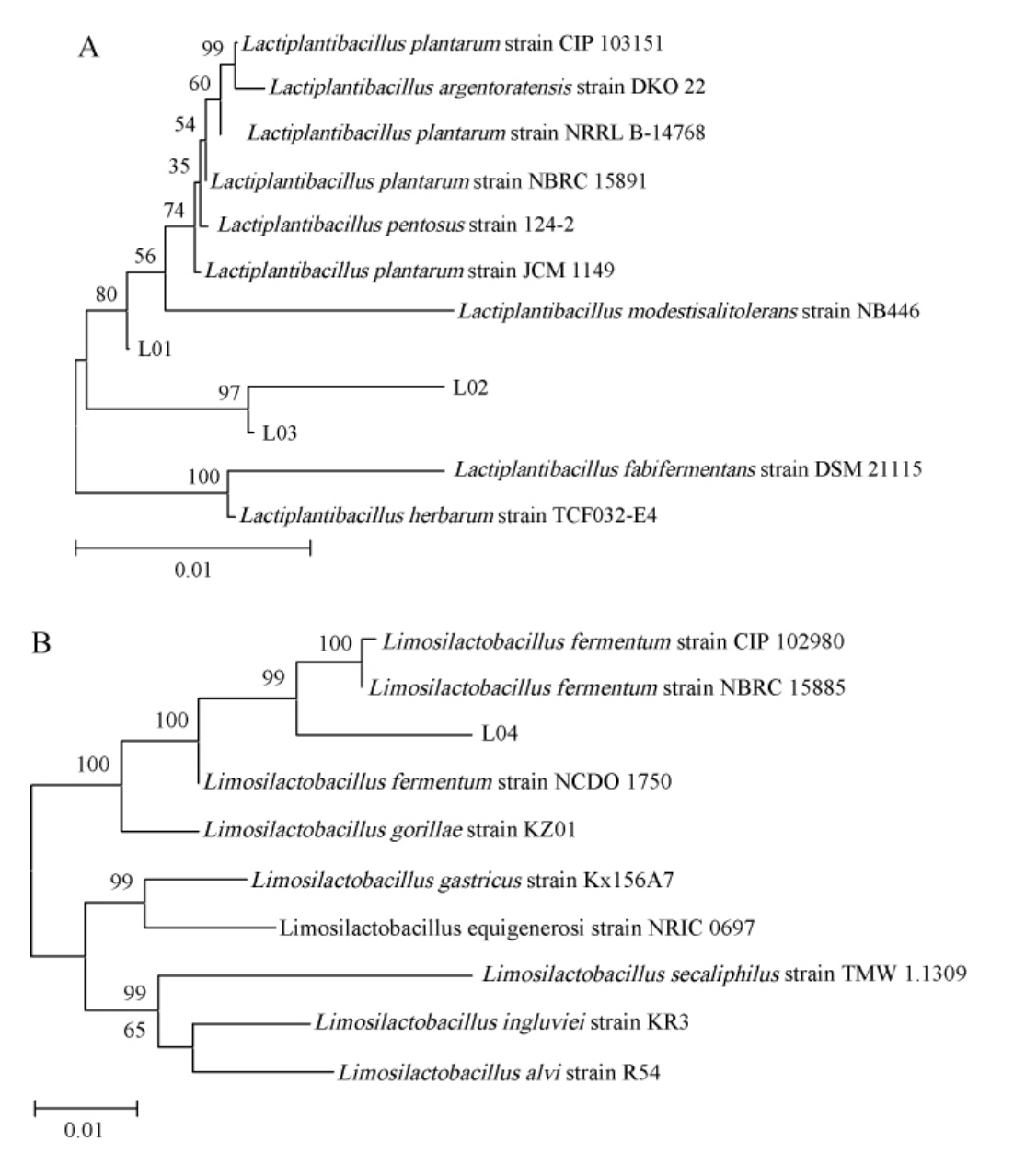

图3 5株筛选乳酸菌基于16S rDNA基因序列的系统发育树
Fig.3 Phylogenetic tree of 5 screened strains of lactic acid bacteria based on 16S rDNA gene sequences
2.2 益生特性评价
2.2.1 模拟胃液耐受能力
胞外多糖具有诸多有益功能,但也与产生菌的益生性质紧密相关。益生菌进入人体后,通常在胃部停留1~3 h,胃液具有强酸性,能够耐受胃液严苛环境是评价益生菌益生性质的重要指标[20]。本研究评估了所筛选5株高产胞外多糖乳酸菌的模拟胃液耐受能力,结果见图4。
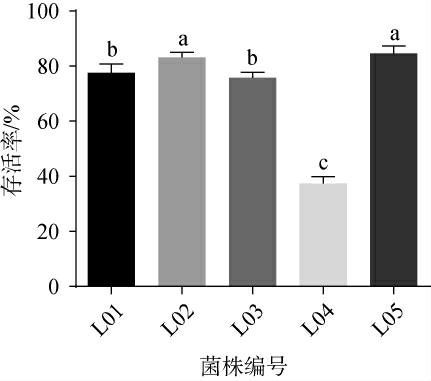
图4 5株筛选乳酸菌在模拟胃液中的存活率
Fig.4 Survival rates of 5 screened strains of lactic acid bacteria in simulated gastric juice
由图4可知,在模拟胃液环境胁迫3 h后,经平板菌落计数,菌株L04的存活率为37.44%,菌株L05、L02、L01和L03的存活率均>75%,尤其是菌株L05,模拟胃液胁迫3 h的存活率最高,为84.55%。据报道,陈欢等[21]对分离到的乳酸菌菌株的耐模拟胃液能力进行测定,发现所有菌株均具有很好的耐酸性,pH 3.0时的存活率均在70%左右。因此,除菌株L04外,本研究筛选到的其余4株乳酸菌均具有较强的模拟胃液耐受能力。
2.2.2 胆盐耐受能力
胆盐可通过破坏细菌的细胞膜脂质层、引起蛋白质变性,威胁细菌的生存。益生菌在经过胃部严苛环境胁迫后,进入肠道发挥作用,在此过程中还需要耐受高渗透压的胆盐环境[22]。5株高产胞外多糖乳酸菌的胆盐耐受能力测定结果见图5。由图5可知,菌株L03、L04和L05的整体耐胆盐能力要强于菌株L01和L02。当胆盐含量为1.5%时,菌株L03、L04和L05的存活率均>90%,菌株L01和L02的存活率分别为50.58%和58.30%;当胆盐含量为3%时,菌株L03和L05的存活率并没有明显变化,但菌株L04的存活率下降为70.03%。当胆盐含量为6%时,尽管5株菌的存活率均出现下降,但是菌株L03和L05的存活率仍维持在80%以上。菌株L03和L05在低浓度和高浓度胆盐环境中的存活率都维持在较高水平,说明两株菌具有极强的胆盐耐受能力。
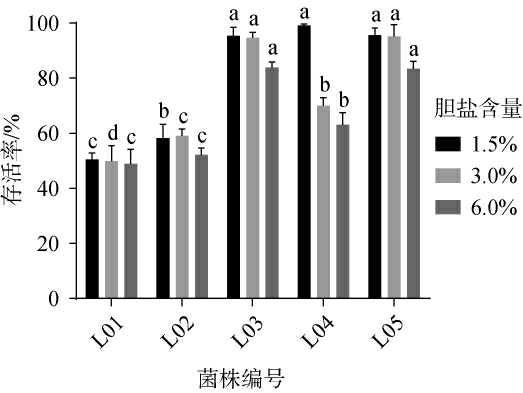
图5 5株筛选乳酸菌在不同牛胆盐含量下的存活率
Fig.5 Survival rates of 5 screened strains of lactic acid bacteria under different bile salt contents
2.2.3 体外抑菌能力
能够抑制肠道中病原微生物生长繁殖是益生菌能够避免胃肠道感染的重要特性,也是评价菌株益生功能的重要指标[23]。5株乳酸菌的体外金黄色葡萄球菌抑菌效果见表1。由表1可知,金黄色葡萄球菌在MRS固体培养基上生长良好,5个牛津杯周围均出现了明显的抑菌圈,说明5株乳酸菌均对金黄色葡萄球菌有一定的抑制能力。菌株L02对金黄色葡萄球菌的抑菌圈直径最小,为(0.50±0.06)cm,菌株L03和L04的抑菌圈直径较大,均为(1.30±0.02)cm,且菌株L01、L03、L04和L05对金黄色葡萄球菌的抑菌圈直径均>1.10cm,说明这4株乳酸菌对金黄色葡萄球菌的抑制作用要强于菌株L02。
表1 5株乳酸菌对金黄色葡萄球菌的抑菌圈直径测定结果
Table 1 Determination results of inhibition zone diameters of 5 strains of lactic acid bacteria on Staphylococcus aureus
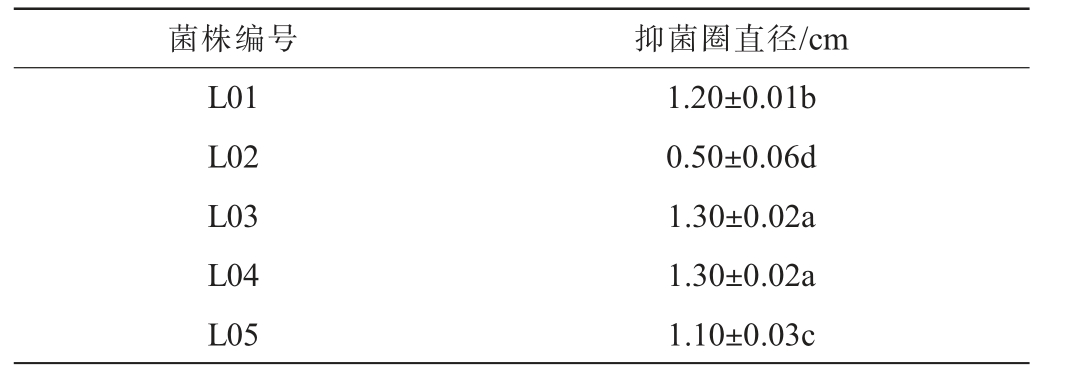
注:同一列中不同字母表示差异显著(P<0.05)。下同。
菌株编号L01 L02 L03 L04 L05抑菌圈直径/cm 1.20±0.01b 0.50±0.06d 1.30±0.02a 1.30±0.02a 1.10±0.03c
2.2.4 抗生素敏感性
在临床治疗中,益生菌常与与抗生素类药物联用,若菌株存在耐药基因,则可能会转移给致病菌,影响治疗效果,危害人体健康[11]。5株乳酸菌对阿莫西林、头孢氨苄抑菌圈直径测定结果见表2。
表2 5株乳酸菌对两种抗生素的抑菌圈直径测定结果
Table 2 Determination results of inhibition zone diameters of 5 strains of lactic acid bacteria against two antibiotics

菌株编号 阿莫西林抑菌圈直径/cm 头孢氨苄抑菌圈直径/cm L01 L02 L03 L04 L05 1.5±0.04c 1.4±0.03d 1.4±0.13d 3.2±0.02a 2.0±0.15b 1.2±0.01c 1.3±0.22c 1.3±0.16c 3.2±0.03a 2.5±0.14b
由表2可知,阿莫西林和头孢氨苄两种常见抗生素均能对这5株乳酸菌产生抑制效果,表明5株乳酸菌具有抗生素敏感性。两种抗生素对菌株L04的抑菌圈直径最大,分别为(3.2±0.02)cm和(3.2±0.03)cm,其次是菌株L05,其两种抗生素的抑菌圈直径分别为(2.0±0.15)cm和(2.5±0.14)cm,两种抗生素对菌株L01、L02和L03的抑菌圈直径均≤1.5 cm。结果表明,5株乳酸菌均具有抗生素敏感性,但不同菌株之间的抗生素敏感性具有显著性差异,其中菌株L04对两种抗生素最为敏感,其次是菌株L05,而菌株L01、L02和L03对两种抗生素的敏感性相对较低。
2.2.5 抗氧化能力
随着现代生活节奏加快,氧化应激问题日益严重,当机体内源性抗氧化剂和修复系统不能有效抵消氧化应激带来的损伤时,必须依靠外源抗氧化剂的补充。研究报道,多种乳酸菌菌种具有抗氧化功能,可作为天然抗氧化剂来源[24-25]。评价乳酸菌抗氧化能力的方法有很多,目前最常用的是通过化学法测定DPPH、ABTS和羟自由基清除能力等指标[26-27],清除率越高,抗氧化能力越强。5株乳酸菌对DPPH、ABTS及羟自由基清除能力测定结果见图6。
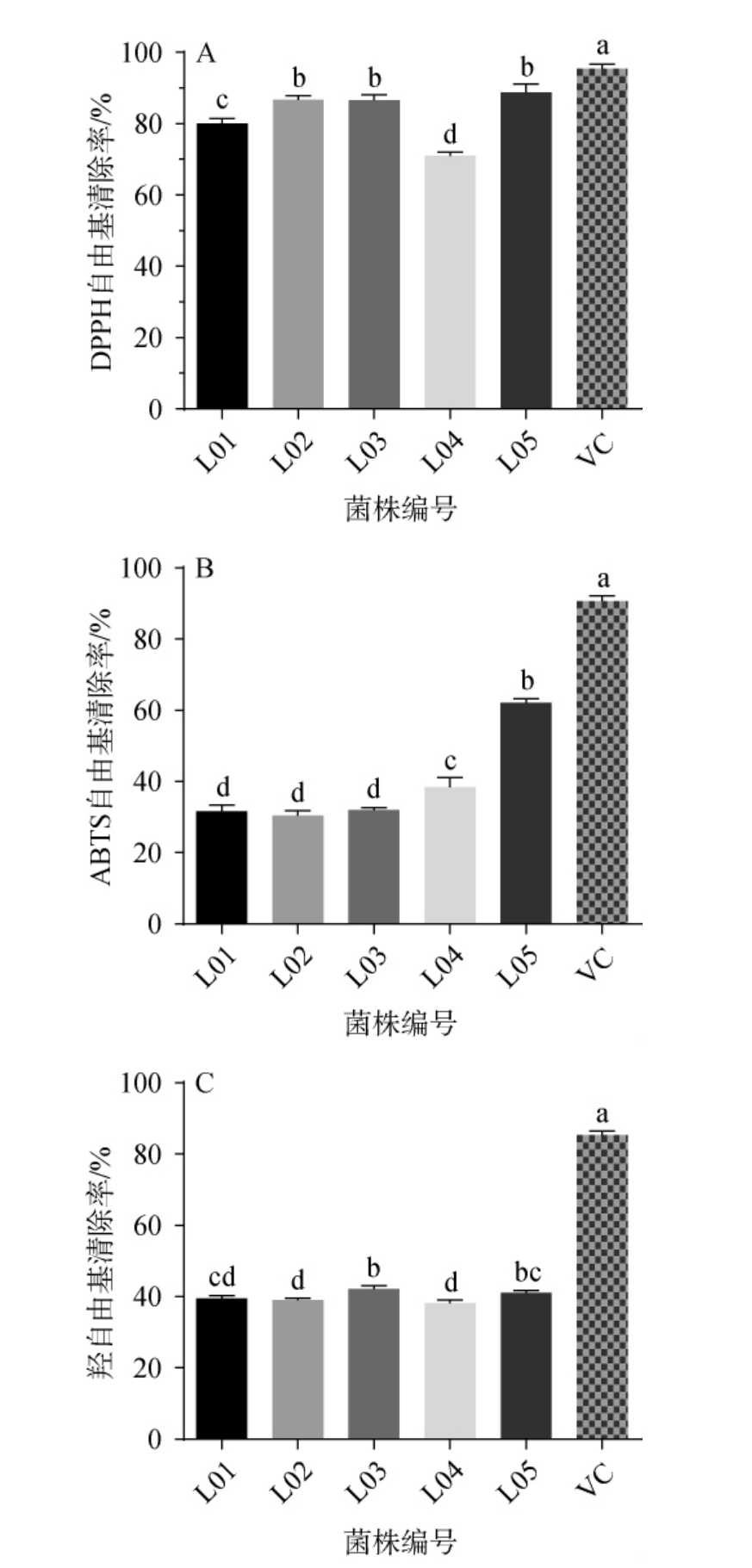
图6 5株乳酸菌的体外抗氧化能力测定结果
Fig.6 Determination results of antioxidant ability in vitro of 5 strains of lactic acid bacteria
A:DPPH自由基清除率;B:ABTS自由基清除率;C:羟自由基清除率。
DPPH自由基清除率是评估菌株抗氧化能力的经典指标,DPPH是一种稳定的自由基,其分子中的氮中心自由基能与抗氧化剂中的氢原子结合,通过测定菌株或其发酵液清除DPPH自由基的能力,可直接反映其抗氧化活性[28]。由图6A可知,5株乳酸菌对DPPH自由基清除率低于阳性对照VC(95.41%),但菌株L01、L02、L03和L05对DPPH自由基清除率均>80%,其中菌株L05对DPPH自由基清除率最高,为88.76%,对DPPH自由基清除率最低的是L04菌株,为71.01%。
ABTS自由基能与抗氧化剂发生电子转移反应而被还原,ABTS自由基清除率可反映菌株的广谱抗氧化能力,适用于菌株培养液、发酵上清液或粗提物等复杂样品的抗氧化能力评估[29]。由图6B可知,5株乳酸菌对ABTS自由基清除率均显著低于阳性对照VC(90.66%)。菌株L05对ABTS自由基清除率最高,为62.09%,菌株L04对ABTS自由基清除率为38.38%,菌株L01、L02和L03对ABTS自由基清除率分别为31.66%、30.44%和31.96%,三者之间没有显著差异(P>0.05)。尉洁等[30]从长白山区发酵酱菜中分离的三株高产胞外多糖乳酸菌对ABTS自由基的清除率分别为51.67%、47.07%、49.92%,均低于本研究中的菌株L05,表明菌株L05具有较强的ABTS自由基清除能力。
羟自由基是活性氧簇(reactive oxygen species,ROS)中最具破坏性的自由基之一,可引发脂质过氧化、蛋白质/DNA损伤,加速细胞衰老和疾病发生[31]。菌株若能有效清除羟自由基,表明其具有显著的抗氧化活性,可用于功能性食品或益生菌开发。由图6C可知,5株乳酸菌对羟自由基清除率在40%左右,均显著低于阳性对照VC(85.27%)。其中,菌株L03和L05对羟自由基清除率>40%,分别为42.18%和41.01%,菌株L01、L02和L04对羟自由基清除率分别为39.55%、38.96%和38.08%。
综上,5株乳酸菌对DPPH自由基清除能力与阳性对照VC相当,对ABTS自由基和羟自由基清除能力低于阳性对照VC,说明5株乳酸菌均具有一定的抗氧化能力,菌株间差异分析表明,菌株L05的抗氧化能力最强。
3 结论
本研究从采集自洛阳地区的自然发酵酸浆中共筛选到了5株高产胞外多糖的乳酸菌,经鉴定,菌株L01~L03为植物乳植杆菌(Lactiplantibacillus plantarum),菌株L04为发酵粘液乳杆菌(Limosilactobacillus fermentum),菌株L05为鼠李糖乳杆菌(Lacticaseibacillus rhamnosus)。菌株L04胞外多糖产量最高,菌株L01、L02、L03和L05具有较强的模拟胃液耐受能力,菌株L03和L05具有极强的胆盐耐受能力,菌株L05还表现出较强的抑菌能力、抗生素敏感性和抗氧化能力,可作为潜在益生菌株。本研究为食品源乳酸菌的筛选和利用提供了参考,对挖掘洛阳地区益生菌资源和促进地区特色食品的开发具有重要意义。
[1]谢佳琪,赵洁.发酵乳中乳酸菌菌株间互作机制及其对产品特性影响的研究进展[J].食品工业科技,2023,44(17):1-7.
[2]曾国庆,蔡昀洁,盛华洋,等.具有降胆固醇功能乳酸菌的筛选及其生物学特性评价[J].中国微生态学杂志,2024,36(5):540-548.
[3]刘辉,刘悦,章检明.产酸乳酸菌筛选、鉴定及其后生元抗氧化活性比较[J].食品研究与开发,2025,46(1):202-209.
[4]范鑫诺,李海阳,郑毅恒,等.洛阳传统绿豆酸浆细菌群落组成分析和功能预测[J].中国食品学报,2024,24(6):369-379.
[5]吴鹏宇,单乾铜,娄娅娟,等.洛阳传统酸浆中乳酸菌分离鉴定及菌种性能测定[J].中国酿造,2025,44(6):130-140.
[6]李璇,李中雨,舒林焱,等.洛阳传统绿豆酸浆工艺优化及发酵特性分析[J].中国粮油学报,2024,39(6):76-85.
[7]ZHANG M, HAO X N, AZIZ T, et al.Exopolysaccharides from Lactobacillus plantarum YW11 improve immune response and ameliorate inflammatory bowel disease symptoms[J].Acta Biochim Pol,2020,67(4):485-493.
[8]LIU Y,ZHENG S J,CUI J L,et al.Alleviative effects of exopolysaccharide produced by Lactobacillus helveticus KLDS1.8701 on dextran sulfate sodium-induced colitis in mice[J].Microorganisms,2024,206(9):389.
[9]CHEGINI P,SALIMI F,PIRBODAGH Z A.Antilisterial and antioxidant exopolysaccharide from Enterococcus faecium PCH.25 isolated from cow butter:characterization and probiotic potential[J].Arch Microbiol,2024,206(9):389.
[10]乔少婷,解敏,代安娜尔,等.嗜热链球菌MGB80-7所产胞外多糖的表型结构及其抗氧化活性[J].微生物学通报,2022,49(7):2686-2699.
[11]覃忠意,周杰,谢霞婷,等.巴马地区产胞外多糖益生乳酸菌的筛选及鉴定[J].中国酿造,2024,43(6):133-140.
[12]胡此海,杨絮,郭全友,等.萝卜泡菜母水中乳酸菌分离鉴定与发酵特性比较[J].食品与发酵工业,2023,49(23):111-119.
[13]DE CARVALHO B T,SUBOTIC′ A,VANDECRUYS P,et al.Enhancing probiotic impact: engineering Saccharomyces boulardii for optimal acetic acid production and gastric passage tolerance[J].Appl Environ Microb,2024,90(6):e00325-24.
[14]ZHANG J,LIU M M,XU J N,et al.First insight into the probiotic properties of ten Streptococcus thermophilus strains based on in vitro conditions[J].Curr Microbiol,2020,77(3):343-352.
[15]李嘉文,刘达,刘党生,等.乳酸菌胞外多糖产生菌的筛选与初步研究[J].中国微生态学杂志,2019,31(9):1027-1033.
[16]王磊,高宗露,宗丽娜,等.酸乳用乳酸菌抗生素耐药性研究[J].食品研究与开发,2021,42(6):162-169.
[17]刘潇婕,黄青巧,刘秀宇,等.灵芝-刺梨双向发酵工艺及发酵产物抗氧化活性评价[J].现代食品科技,2025,41(7):125-132.
[18]李悦,陈静,张晓雨,等.产胞外多糖乳酸菌的筛选与体外益生特性评价[J].现代食品,2023,29(14):188-192.
[19]陈靖,周佳豪,毛琪琪,等.产胞外多糖乳酸菌的筛选及鉴定[J].食品与机械,2023,39(4):26-31,169.
[20]LI X F, PAN Q, LUO H T, et al.Isolation, identification and probiotic potential evaluation of microorganisms from traditional fermented sour meat[J].Food Sci,2024,45(14):75-84.
[21]陈欢,王斌,史学伟,等.新疆哈萨克族传统奶酪中潜在益生乳酸菌的筛选[J].中国调味品,2019,44(12):50-54.
[22]ZHAO M D, LI Y Y, ZHANG Y Y, et al.Genomic analysis and functional properties of Lactobacillus johnsonii GJ231 isolated from healthy beagles[J].Front Microbiol,2024,15(1):1437036.
[23]檀茜倩,程笑笑,崔方超,等.泡菜中产β-葡萄糖苷酶植物乳杆菌的益生和酶学特性[J].中国食品学报,2024,24(9):69-79.
[24]KOHAN A, KESHTMAND Z.Ameliorating effects of Lactobacillus probiotics on cadmium-induced hepatotoxicity, inflammation, and oxidative stress in Wistar rats[J].Comp Clin Pathol,2024,33(4):653-664.
[25]冯怡婷,何洋,安琪尔,等.云南甜米酒中乳酸菌的分离鉴定及其发酵甜米酒的抗氧化活性、挥发性成分研究[J/OL].食品工业科技,1-16[2025-07-14].https://doi.org/10.13386/j.issn1002-0306.2024110265.
[26]OBIANWUNA U E,KALU N A,WANG J,et al.Recent trends on mitigative effect of probiotics on oxidative-stress-induced gut dysfunction in broilers under necrotic enteritis challenge:a review[J].Antioxidants,2023,12(4):911.
[27]蒋光阳,田永强.乳酸菌产胞外多糖的发酵条件优化及其抗氧化活性研究[J].中国酿造,2023,42(4):187-195.
[28]JI K,JANG N Y,KIM Y T.Isolation of lactic acid bacteria showing antioxidative and probiotic activities from kimchi and infant feces[J].J Microbiol Biotechn,2015,25(9):1568-1577.
[29]范洪臣,茜琳,韩雪,等.黏豆包发酵液中乳酸菌分离鉴定及其益生性能[J].食品研究与开发,2023,44(23):161-167.
[30]尉洁,张玲芳,胡顺安,等.长白山区发酵酱菜中高产胞外多糖乳酸菌的筛选及多糖抗氧化性分析[J].食品工业科技,2024,45(2):110-117.
[31]延莎,范亚芳,郑龙华,等.乳酸菌发酵茶花粉所得提取物对4种自由基的清除能力[J].食品科技,2017,42(3):238-243.