柿(Diospyros kaki Thunb)为柿科柿属植物,原产于中国,至今已有3千多年种植历史,种植面积和年产量均居世界首位[1]。柿果营养丰富且具有较高的经济价值和药用价值,柿子品种繁多,其口感、风味和营养物质的含量都不同,用途也就非常广泛[2-3]。柿果属于呼吸跃变型的果实,一旦脱离柿树其保质期就变短,目前仍以鲜果和柿饼为主销售,尚缺乏有效的深加工技术,每年秋冬都有大量柿果无人问津,难以实现资源有效配置[4-5]。本团队在柿果产品研发方面开展研究多年,采用冷冻脱涩解决产品后期返涩问题,已开发出柿粉、柿果酥点、柿果饮料、柿果果冻等产品[6-8]。实现果实的高质、高值、高效利用是我国果业十四五规划的重要任务和伟大历史使命,开展柿资源应用研究,是目前柿果业发展中亟待解决的问题。
酿造柿子酒是实现柿资源高值化利用的重要途径,可有效解决柿果季节性资源过剩的问题。酿酒过程的微生物对发酵过程有着很大的影响,其中酵母菌是最重要的微生物之一,酿酒酵母将糖类高效转化为乙醇的同时产生风味物质,其发酵性能及代谢产物的差异直接影响到出酒率和酒的风味品质[9]。目前尚缺乏柿子酒发酵专用酵母菌,除了采用复合酵母作为发酵剂改良发酵工艺[10-11],更多研究者关注于优良酵母菌种的筛选和选育以提升酿酒质量和发酵速度[12]。陈丽花等[13]从中国特色甜酒曲中分离6株优质酵母菌,通过不同菌种组合发酵以生产不同香气特征的米酒。胡江南等[14]从宁夏葡萄酒产区的土壤、葡萄中分离筛选得到2株优良酵母菌,其中酿酒酵母J-1具有比商业菌种更优的发酵性能和产香能力。
本研究从自然发酵柿子酒中分离筛选优良酵母菌,并对其进行分子生物学鉴定,筛选出发酵性能优良酵母菌应用于柿子酒酿造,并基于顶空固相微萃取结合气相色谱-质谱(headspace solid phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)技术分析柿子酒中挥发性香气组分,旨在提高柿子酒品质,为柿子果酒产业化生产奠定菌种基础。
1 材料与方法
1.1 材料与试剂
1.1.1 原料
富有柿:陕西学前师范学院校园。
1.1.2 材料与试剂
葡萄糖(分析纯)、琼脂粉、蛋白胨、酵母浸粉(均为生化试剂):北京奥博星生物技术有限责任公司;氯化钾、磷酸二氢钾、氯化钙、氯化铁(均为分析纯):广东省化学试剂工程技术研究开发中心;硫酸锰、硫酸镁(均为分析纯):天津市河东区红岩试剂厂;溴甲酚绿(分析纯):天津基准化学试剂有限公司;Lavlvin K1发酵剂:法国拉曼集团。
1.1.3 培养基
活化培养基:葡萄糖20 g/L,蛋白胨20 g/L,酵母浸粉10 g/L,115 ℃灭菌20 min。
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD)培养基:葡萄糖20 g/L,蛋白胨20 g/L,酵母浸粉10 g/L,琼脂粉18 g/L,115 ℃灭菌20 min。
Wallerstein Laboratory(WL)培养基:葡萄糖52 g/L,蛋白胨5 g/L,酵母浸粉5.2 g/L,氯化钾0.44 g/L,磷酸二氢钾0.56 g/L,氯化钙0.16 g/L,氯化铁0.004 g/L,硫酸锰0.006 g/L,硫酸镁0.14 g/L,溴甲酚绿0.02 g/L,琼脂粉18 g/L,调节pH 5.5,115 ℃灭菌25 min。
2,3,5-三苯基氯化四氮口坐(2,3,5-trimethylbenzotriazolium chloride,TTC)培养基:上层:葡萄糖5 g/L,2,3,5-三苯基氯化四氮口坐0.5 g/L,琼脂18 g/L;下层:YPD培养基。121 ℃灭菌20 min。
发酵培养基:葡萄糖40 g/L,蛋白胨20 g/L,酵母浸粉10 g/L,pH 5.0,115 ℃灭菌20 min。
1.2 仪器与设备
TM-767-IV型破碎机:广东省中山市海盘电器有限公司;SPX-250B-Z型恒温培养箱:上海博迅实业有限公司医疗设备厂;RHB-10ATC型折光仪:上海垒固仪器制造有限公司;YTUP-15S型超净纯水机:四川卓越水处理有限公司;CX21型显微镜:上海泽仕光电科技有限公司;ISQ7610型GC-MS联用仪(配有RSH型TriPlus自动进样装置)、TGWAXMS型气相色谱柱(30 m×0.25 mm×0.25 μm):美国Thermo Scientific公司。
1.3 实验方法
1.3.1 柿子酒加工工艺流程及操作要点
新鲜柿果→打浆→装罐→发酵→浆汁分离→陈酿→柿子酒成品
操作要点:
打浆:挑选没有病虫害的果实,经流水冲洗、削皮、切块、去籽后,破碎机打浆至均匀、细腻无块状。
装罐、发酵:将柿浆分装到提前杀菌的发酵罐中,一组加入0.02%Lavlvin K1发酵剂,另一组不添加发酵剂,均置于28 ℃恒温发酵,发酵过程中定期测定酒精度和残糖量,二者不再变化即终止发酵。
浆汁分离、陈酿:发酵结束后,利用虹吸原理吸取上层清液,再用纱布过滤,置于新的发酵罐中封口18 ℃陈酿50 d,即得柿子酒成品。
1.3.2 柿子酒感官评定
参照顾凡等[15]的方法,邀请10位食品专业人员从外观、滋味、香气、典型性四个方面对柿子酒进行感官评分,满分100分,柿子酒感官评分标准见表1。
表1 柿子酒感官评分标准
Table 1 Sensory evaluation standards of persimmon wine

项目 评分标准 评分/分外观(20分)滋味(40分)香气(30分)典型性(10分)澄清、透明、具有柿果特征颜色澄清、颜色较好浑浊、有杂物、色泽不好具有浓郁的柿果果香风味特征不苦不涩、酸甜适中、柔和口感适中、纯正无杂味略苦、涩、酸,酒味微淡苦、涩、酸明显,带有异味果酒香味浓郁,具有浓郁果香味具有柿子果香味,较悦人果香味不足不具有果香味有明显的柿子果香味,酒香具有香味、酒味果香、酒香味不明显不具备果香味、有异味16~20 11~15≤10 35~40 30~34 25~29 20~24≤19 25~30 20~24 16~19≤15 9~10 7~8 5~6≤4
1.3.3 柿子酒理化指标测定
总酸含量测定:参照国标GB/T 12456—2021《食品中总酸的测定》中的第一法;可溶性固形物(残糖量)测定:采用手持糖度仪;酒精度测定:参照国标GB 5009.225—2023《食品安全国家标准酒和食用酒精中乙醇浓度的测定》中的第二法。
1.3.4 优势酵母菌分离纯化
取自然发酵的柿子酒样品1 mL于发酵培养基中,在30 ℃、160 r/min条件下振荡培养2 d,平板涂布法梯度稀释,分别取10-6、10-7、10-8浓度菌悬液接种至YPD培养基27 ℃培养2 d进行初步纯化,再以平板划线法反复分离纯化直至得到纯菌落[16-17],再划线接种WL培养基28 ℃培养2 d,观察菌落形态,伊红美兰染色后镜检,参考《酵母菌特征和鉴定手册》和文献对菌种进行初步鉴定[18-19]。
1.3.5 优良酵母菌的复筛
TTC显色剂能够被活细胞中的脱氢酶还原,形成从无色到红色的呈色反应,显色越深表明产酒精能力越强[20]。具体步骤:挑取初筛酵母菌于活化培养基于28 ℃培养2 d,然后均匀涂布在YPD培养基上作为TTC培养基的底层,28 ℃培养2 d后倒入TTC培养基,30 ℃避光培养2~4 h,观察其颜色变化。
1.3.6 发酵性能的测定
酵母菌发酵性能的测定参考文献[21]并适当修改,将菌种按2%比例接种至发酵培养基中,以未接种的为对照组,依次编号、称质量,28 ℃、100 r/min摇床培养,每隔1 d取出称质量,直至发酵液质量不再减少,即为发酵结束,通过计算发酵前后CO2的质量损失,以CO2释放量表征酵母菌的发酵性能。
1.3.7 优良酵母菌种应用于柿子酒酿造
挑取分离纯化得到的优良酵母菌于活化培养基于28 ℃培养2 d后,即得种子液。种子液按照2%接种量加入柿果浆中,以未接种酵母菌为对照组,28 ℃恒温发酵10 d左右,监测发酵过程总酸、可溶性固形物(残糖量)、酒精度的变化,并进行感官评定。
1.3.8 菌种分子生物学鉴定
采用真菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒提取酵母菌的基因组DNA,以其为模板,采用26S rDNA D1/D2区序列扩增,使用通用引物NL1(5'-GCATATCAATAAGCGGAGGAAAAG-3')和NL4(5'-GGTCCGTGTTTCAAGACGG-3')。PCR扩增体系(25 μL):10×EasyTaqBuffer 2.5 μL,NL1和NL4(10 μmol/L)各0.5 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphos-phates,dNTPs)(2.5 mmol/L)2 μL,10×Easy Taq聚合酶0.25 μL,酵母菌DNA模板1 μL,双蒸水(ddH2O)18.25 μL。PCR扩增条件:95 ℃预变性5 min;94 ℃变性1 min,52 ℃退火1 min,72 ℃延伸80 s,36次循环;72 ℃再延伸8 min。PCR扩增产物送至北京清析技术研究院有限公司测序,将测序得到的序列提交至美国国家生物技术信息中心(national center of biotechnology information,NCBI)GenBank数据库进行基本局部比对搜索工具(basiclocalalignmentsearchtool,BLAST)同源性比对分析,并使用MEGA-X 64软件中邻接(neighbor joining,NJ)法构建系统进化树构建系统发育树。
1.3.9 柿子酒香气成分分析
柿子酒香气成分分析采用顶空固相微萃取-气相色谱-质谱(HS-SPME-GC-MS)法。取1 mL柿果酒样品,加29 mL蒸馏水稀释,充分混合均匀后,取6 mL置于20 mL顶空瓶中,60 ℃平衡15 min。选用85 μm CAR/PDMS萃取头,以60 ℃萃取30 min,在进样口(250 ℃)解吸3 min。进样前萃取头在老化炉中260 ℃老化10 min。
气相色谱条件:TG-WAXMS色谱柱(30 m×0.25 mm×0.25 μm),载气为高纯氦气(He)(纯度≥99.999%),流速1 mL/min,进样口温度250 ℃,不分流进样,溶剂延迟3.5 min。程序升温为起始温度50℃,保持3min,以4℃/min升至170℃,保持2 min,再以6 ℃/min的速率升温至230 ℃,保持5 min。
质谱条件:电子电离(electronic ionization,EI)源,离子源温度230 ℃,传输线温度230 ℃,电子能量70 eV,全扫描模式,扫描范围33~350 m/z。
定性定量方法:利用美国国家标准技术研究所(National Institute of Standards and Technology,NIST)质谱数据库进行化合物匹配,筛选出匹配度>800的物质进行鉴定,结合人工图谱解析和相关文献查证确认挥发性成分,峰面积归一化法进行定量分析。
1.3.10 数据处理与分析实验结果以“平均值±标准差”表示,采用SPSS 25.0软件对数据进行方差分析,P<0.05表示差异显著。
2 结果与分析
2.1 自然发酵柿子酒品质分析
2.1.1 柿子酒发酵过程中残糖和酒精度变化
采用自然发酵制备柿子酒,以添加Lavlvin K1发酵剂制备柿子酒为对照,发酵过程残糖和酒精度变化结果见图1。由图1可知,柿子酒发酵过程残糖量呈下降趋势,酒精度呈上升趋势,柿子酒均可以正常发酵。整个发酵期,自然发酵比添加发酵剂的发酵速率略低,这是由于发酵剂中含有提高发酵速度的优势菌,其利用糖发酵成乙醇的能力比较强,可直接利用柿浆中的糖进行发酵,其次在自然发酵的柿子酒中存在的不同菌种,可能存在相互抑制作用,致使柿子酒中的酵母菌占劣势,酒精度也相对较低。然而两种柿子酒发酵过程酒精度和残糖差异不显著(P>0.05),说明添加发酵剂对柿子酒发酵速率没有显著影响。因此可以结合其他指标考虑利用自然发酵或者自然发酵过程的优势菌种生产柿酒。
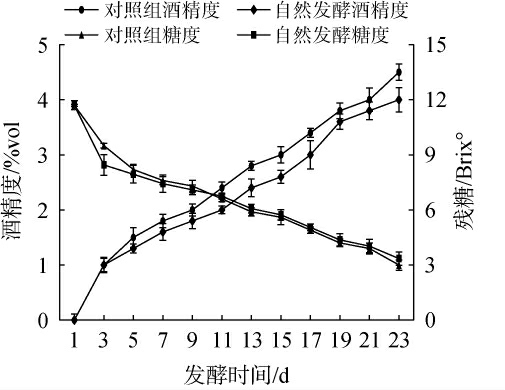
图1 柿子酒发酵过程中残糖含量和酒精度的变化
Fig.1 Change of residual sugar contents and alcohol content during fermentation process of persimmon wine
2.1.2 柿子酒发酵过程中总酸变化
酵母菌可以利用水果中的糖生成乙醇、酸类等物质,除了乙醇是代谢的主要产物,同时代谢产生的酸类物质也对果酒的口感产生重要影响[22]。以添加Lavlvin K1发酵剂制备柿子酒为对照,自然发酵柿子酒发酵过程总酸含量变化结果见图2。由图2可知,两种柿子酒发酵过程中总酸含量先上升后降低,这可能是由于前期发酵过程菌种生长代谢速度较快,产生的酸类物质上升,以及细胞在高糖的环境下,激发了细胞代谢产酸的应激效应[23]。发酵后期微生物在酸性条件下生长受到抑制,活性降低,从而导致总酸含量逐渐降低。赵驰等[24]研究表明,柿酒发酵第17天后柿酒的理化指标基本稳定,结合感官评定判定为发酵结束,之后陈酿过程中需要对陈酿环境以及储藏管理加大控制力度,避免总酸含量持续增高对柿酒口感和品质造成负面影响。经差异性分析,两种柿酒的总酸含量变化差异不显著(P>0.05)。因此,自然发酵对柿子酒的降酸效果无不利影响,可结合感官评定进一步评估自然发酵柿子酒的可行性。
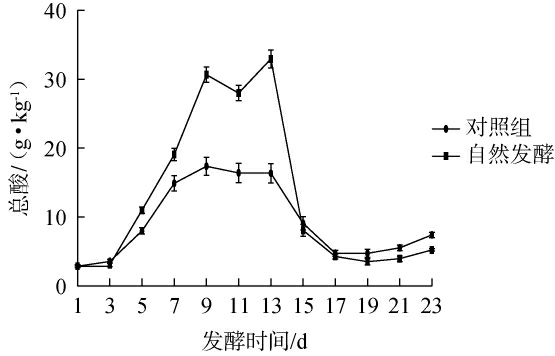
图2 柿子酒发酵过程总酸含量变化
Fig.2 Change of total acid contents during fermentation process of persimmon wine
2.1.3 柿子酒感官品质分析
以添加Lavlvin K1发酵剂制备柿子酒为对照,自然发酵制备柿子酒,两种柿子酒感官评定结果见表2。由表2可知,两组柿子酒均有浓郁的酒香味和柿子果味,无其他杂味,口感略涩,无明显苦味和酸味,颜色有所差异,自然发酵柿子酒呈亮黄色,添加Lavlvin K1发酵剂的对照组柿子酒颜色较暗。自然发酵柿子酒较发酵剂发酵的颜色更理想,Lavlvin K1发酵剂制备柿子酒及自然发酵制备柿子酒感官评分相近(总分分别为78分、80分),但略有苦涩味需要改善。自然发酵柿子酒中可能存在更利于柿子酒生产的优良菌种,有必要进行分离筛选以提高柿子酒感官品质。
表2 两种柿子酒感官品质对比分析
Table 2 Comparative analysis of sensory quality of two kinds of persimmon wines

项目外观滋味香气典型性对照组 得分/分 自然发酵柿子酒 得分/分澄清、透明、酒体为暗黄色具有浓郁的柿子果香味特征,略涩和苦,不酸,无异味具有柿子果香味且浓郁,气味宜人有明显的果香味和酒味,无其他异味17 27 26 8澄清透明、酒体为亮黄色果香味特征浓郁,略涩、苦,无其他异味具有柿子果香味浓郁醇厚,气味宜人有明显的果香味和酒味,无其他异味19 25 28 8
2.2 菌株的分离纯化
从自然发酵柿子酒样品中经多次分离纯化共筛出8株菌,编号分别为1-1、1-2、1-3、2-1、2-8、3-4、3-5、3-6,其菌落形态及细胞形态结果见表3。
表3 筛选酵母菌的菌落及细胞形态
Table 3 Colonies and cell morphology of screened yeast strains

菌株编号 菌落形态 细胞形态 假菌丝 孢子1-1 1-2 1-3圆、光滑、淡黄色、半透明、平坦圆、光滑、淡粉色、半透明、平坦椭圆、光滑、乳白色、不透明、平坦椭圆形圆形圆筒形有无无有有无
续表

菌株编号 菌落形态 细胞形态 假菌丝 孢子2-1 2-8 3-4 3-5 3-6圆、不光滑、乳白色、半透明、高凸圆、光滑、淡粉色、不透明、低凸椭圆、不光滑、乳白色、不透明、高凸圆、不光滑、乳白色、不透明、高凸圆、光滑、乳白色、不透明、高凸椭圆形椭圆形圆形圆形椭圆形无无无无无有无有有有
由表3可知,大多数筛选菌株菌落形态为圆形和椭圆形,表面光滑,乳白色,隆起的形状不一,无假菌丝,其中菌株1-1、1-2、1-3和2-8的菌落形态比其他菌株的菌落形态小且生长的速度比较慢,结合镜检结果初步鉴定菌株3-4可能为酿酒酵母,菌株2-1、3-5和3-6可能为中间型酒香酵母。
2.3 优良酵母菌筛选
2.3.1 筛选酵母菌TTC染色结果
TTC染色法能对酵母的代谢产物产生显色反应,常被应用于高产乙醇酵母的筛选,通过其颜色的深浅可以判断其胞内转化酶活力的大小,颜色越深表明其细胞活性越强,产乙醇能力也越强[25]。筛选的酵母菌在TTC培养基上的显色结果见表4。由表4可知,菌株3-4、3-5和3-6TTC染色呈现出深红色和红色,其余菌株TTC染色为粉色或者浅粉色,故将显色深的菌株3-4、3-5和3-6菌种重新编号为J1、J3和J2,进行后续发酵性能测定。
表4 筛选酵母菌菌株在TTC培养基上的显色结果
Table 4 Chromogenic results of screened yeast strains on TTC medium
注:“+++”表示深红;“++”表示红色;“+”表示浅红。
菌株编号 1-1 1-2 1-3 2-1 2-8 3-4 3-5 3-6结果 + + + + + +++ ++ ++
2.3.2 筛选酵母菌发酵力的测定
发酵力是判断酵母菌株发酵性能最重要的指标,酵母菌在无氧条件下通过呼吸作用,将糖类转化为乙醇,并释放CO2,因此发酵过程CO2的释放量可以表征发酵效率,继而判断菌种的发酵力强弱[14]。以未接种为对照,将菌株J1、J3和J2分别接种至发酵培养基中,以发酵时间为横坐标,CO2释放量为纵坐标绘制发酵性能曲线见图3。由图3可知,所有菌种在1 d内启动发酵,11 d后趋于平稳,四组CO2释放量由高到低依次为:菌株J1>菌株J3>菌株J2>对照组,其中菌株J1和J3的CO2释放量始终保持高水平,说明其产乙醇能力较优,发酵性能较强,筛选作为后续试验菌种。
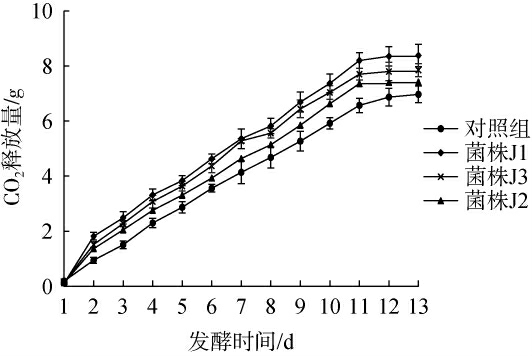
图3 筛选酵母菌菌株发酵过程中CO2释放量
Fig.3 CO2 emissions of screened yeast strains during fermentation process
2.3.3 优良酵母菌株应用于柿子酒酿造
将优良酵母菌株接种于柿子浆中发酵制备柿子酒,以自然发酵柿子酒为对照,其发酵过程中残糖和酒精度、总酸及感官品质变化情况见图4。由图4a可知,与对照组相比,优势菌种发酵过程的残糖下降幅度和酒精度上升幅度更大,J3的酒精度始终高于J1,说明J1和J3在同等条件下利用糖的能力强于对照组,且J3的发酵能力强于J1。总酸含量太高或太低对柿酒口感和品质影响较大。由图4b可知,对照组酒样和菌株J1发酵酒样发酵过程的总酸含量呈先上升再下降再上升的趋势,菌株J2发酵酒样的总酸含量一直呈上升趋势。由图4c可知,3组柿酒随发酵时间的增加感官评分越高,菌株J3发酵的柿子酒香气浓郁,无明显苦、涩味,感官评分在各项指标上高于对照组和菌株J1组,发酵品质更优。
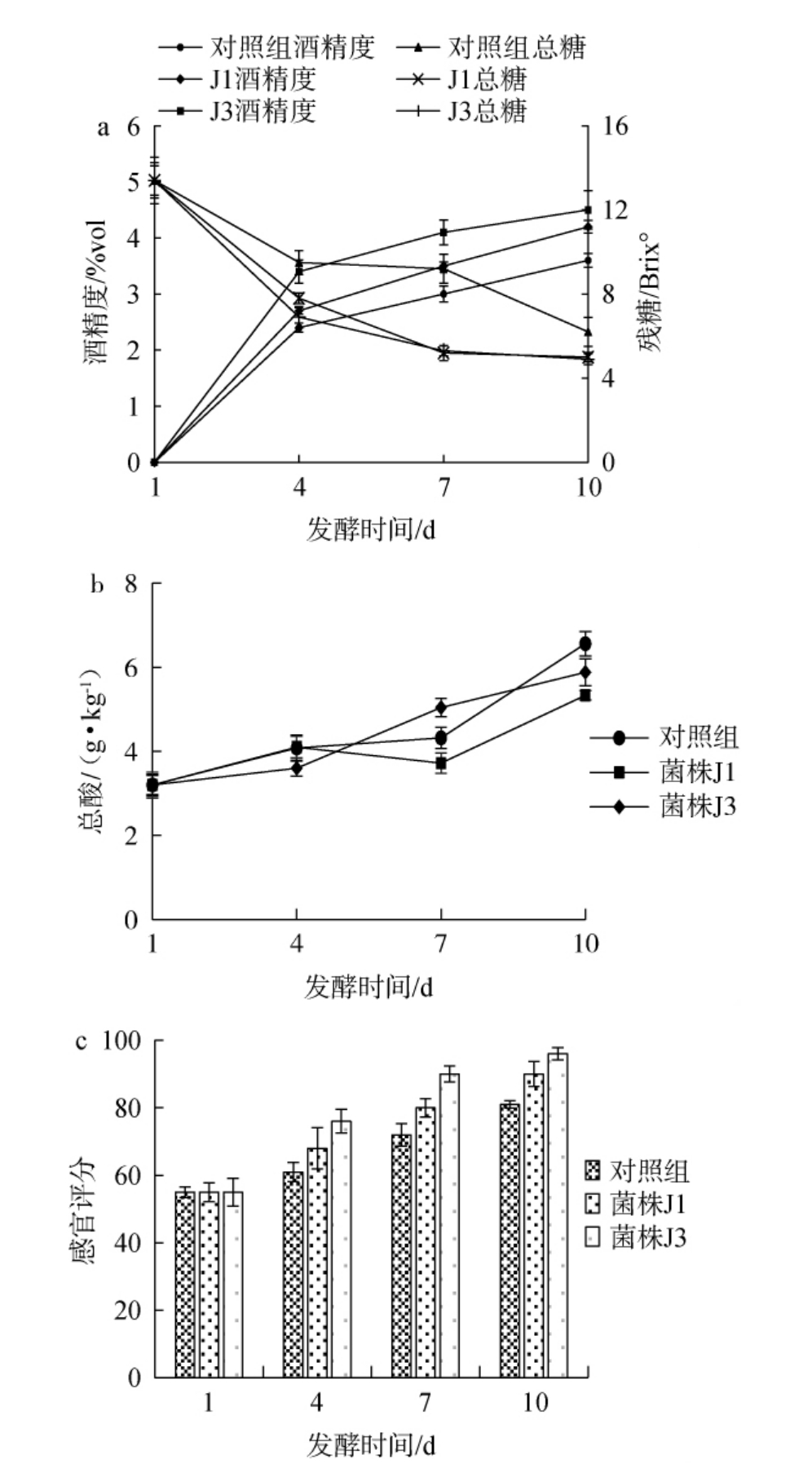
图4 优良酵母菌株J1、J3酿造柿子酒发酵过程中残糖含量和酒精度(a)、总酸含量(b)及感官评分(c)变化
Fig.4 Changes of residual sugar contents and alcohol content (a),total acid contents (b) and sensory score (c) during fermentation process of persimmon wine brewed by excellent yeast strains J1 and J3
2.4 优良菌株J3分子生物学鉴定结果
NCBI网站上将菌株J3的26S rDNA基因测序结果用BLAST软件进行同源性比对,用MEGA7.0软件构建系统发育树,结果见图5。由图5可知,菌株J3的26S rDNA基因片段与酿酒酵母(Saccharomyces cerevisiae)相似性为100%。因此,菌株J3被鉴定为酿酒酵母(Saccharomyces cerevisiae)。
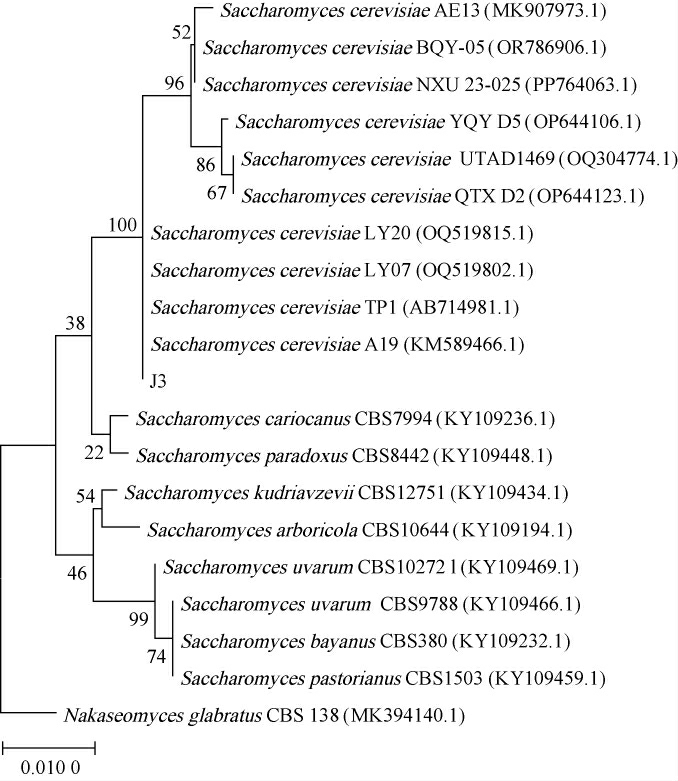
图5 基于26S rDNA基因序列菌株J3系统发育树
Fig.5 Phylogenetic tree of strain J3 based on 26S rDNA gene sequences
2.5 柿子酒香气成分分析结果
香气物质是构成果酒感官品质和典型性的重要物质基础,不同果酒因原料、菌种、发酵工艺的不同其香气物质的含量和种类也不尽相同[26-27]。以自然发酵柿子酒为对照,将菌株J3应用于柿子酒酿造,采用HS-SPME-GC-MS技术对两种柿子酒的香气成分进行检测,结果见表5。由表5可知,从优良酵母菌株J3酿造柿子酒共鉴定出34种香气成分,包括醇类11种、酯类13种、酸类5种、其他类5种。自然发酵柿子酒共鉴定出30种香气成分,包括醇类8种、酯类11种、酸类5种、其他类6种。两种柿子酒相比,优良菌株J3发酵柿子酒的香气成分种类更多,含量更高,尤其是醇类和酯类物质。
表5 两种柿子酒香气成分GC-MS分析结果及香气特征
Table 5 GC-MS analysis results of aroma components and aroma characteristics of two kinds of persimmon wines

种类 序号 化合物 CAS 香气特征[29,33-35]相对含量/%菌株J3发酵柿子酒 自然发酵柿子酒醇类1234567891 0酯类11 12 13 14 15 16乙醇3-甲基-1-丁醇仲辛醇苯乙醇3-甲基-2-己醇2-乙基己醇2,3-丁二醇(R,R)-(-)-2,3-丁二醇正辛醇D-香茅醇1-壬醇正十一醇甘油3-甲基-1-丁醇乙酸酯乳酸乙酯己酸乙酯64-17-5 123-51-3 5978-70-1 1960/12/8 2313-65-7 104-76-7 19132-06-0 24347-58-8 111-87-5 1117-61-9 143-08-8 112-42-5 56-81-5 123-92-2 687-47-8 123-66-0 29.73 34.20 3.62 16.62--0.49--0.19 0.09 0.09 0.12 0.09 0.14 4.71 0.95 1.24 21.06 22.02 2.85 7.86 0.14 0.23 1.47————0.12--23.78 5.98--酒精味苹果白兰地香气、辛辣味芳香气味清甜的玫瑰花香化学酒味或者果味甜味轻微的甜味和酒精味甜味、酒精气味油脂气味、柑橘气息玫瑰叶和油性花瓣香气玫瑰香味淡甜脂腊香、玫瑰花香,柑橘和菠萝样果香味甜味类似香蕉气味朗姆酒、水果和奶油的香气菠萝、香蕉水果香气
续表
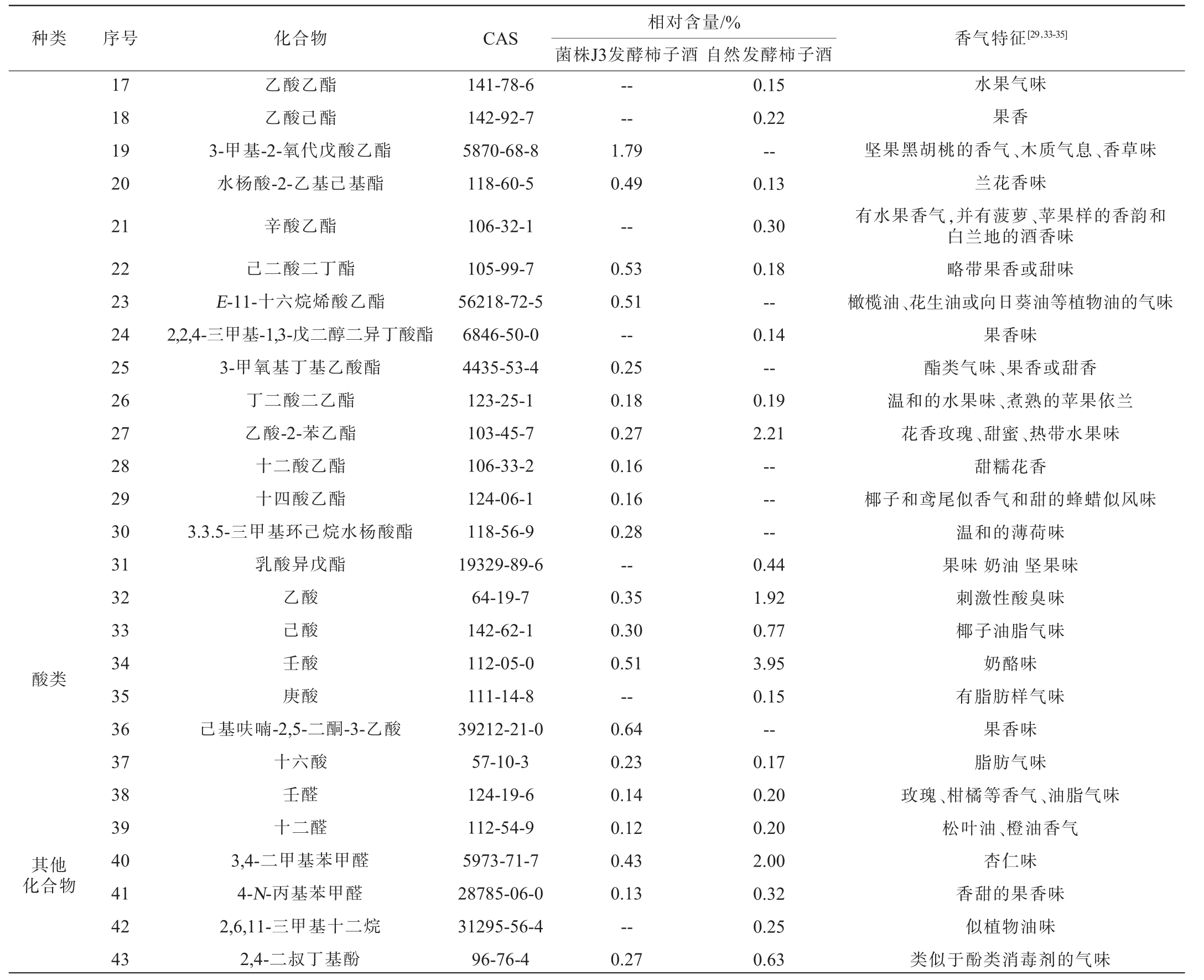
注:“--”表示未检出。
种类 序号 化合物 CAS 香气特征[29,33-35]相对含量/%菌株J3发酵柿子酒 自然发酵柿子酒酸类其他化合物17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43乙酸乙酯乙酸己酯3-甲基-2-氧代戊酸乙酯水杨酸-2-乙基己基酯辛酸乙酯己二酸二丁酯E-11-十六烷烯酸乙酯2,2,4-三甲基-1,3-戊二醇二异丁酸酯3-甲氧基丁基乙酸酯丁二酸二乙酯乙酸-2-苯乙酯十二酸乙酯十四酸乙酯3.3.5-三甲基环己烷水杨酸酯乳酸异戊酯乙酸己酸壬酸庚酸己基呋喃-2,5-二酮-3-乙酸十六酸壬醛十二醛3,4-二甲基苯甲醛4-N-丙基苯甲醛2,6,11-三甲基十二烷2,4-二叔丁基酚141-78-6 142-92-7 5870-68-8 118-60-5 106-32-1 105-99-7 56218-72-5 6846-50-0 4435-53-4 123-25-1 103-45-7 106-33-2 124-06-1 118-56-9 19329-89-6 64-19-7 142-62-1 112-05-0 111-14-8 39212-21-0 57-10-3 124-19-6 112-54-9 5973-71-7 28785-06-0 31295-56-4 96-76-4——1.79 0.49--0.53 0.51--0.25 0.18 0.27 0.16 0.16 0.28--0.35 0.30 0.51--0.64 0.23 0.14 0.12 0.43 0.13--0.27 0.15 0.22--0.13 0.30 0.18--0.14--0.19 2.21——--0.44 1.92 0.77 3.95 0.15--0.17 0.20 0.20 2.00 0.32 0.25 0.63水果气味果香坚果黑胡桃的香气、木质气息、香草味兰花香味有水果香气,并有菠萝、苹果样的香韵和白兰地的酒香味略带果香或甜味橄榄油、花生油或向日葵油等植物油的气味果香味酯类气味、果香或甜香温和的水果味、煮熟的苹果依兰花香玫瑰、甜蜜、热带水果味甜糯花香椰子和鸢尾似香气和甜的蜂蜡似风味温和的薄荷味果味奶油坚果味刺激性酸臭味椰子油脂气味奶酪味有脂肪样气味果香味脂肪气味玫瑰、柑橘等香气、油脂气味松叶油、橙油香气杏仁味香甜的果香味似植物油味类似于酚类消毒剂的气味
柿子果酒香气成分复杂多样,以醇类化合物占比最高,其次是酯类化合物,酸类和醛酮类化合物占比较少,与相关柿子果酒文献报道一致[28-30]。醇类化合物主要来源于发酵、氨基酸的转化及亚麻酸降解物的氧化,是柿子酒香气中最主要的成分。优势菌种发酵柿子酒中检测到醇类物质11种,占总香气成分85.38%,自然发酵柿酒中检测到醇类物质8种,占总香气成分55.75%。两种柿子酒中乙醇含量均为最高,除此之外相对含量最高的醇类化合物是3-甲基-1-丁醇,在优势菌种和自然发酵柿子酒总香气成分中分别占34.20%、22.02%,具有苹果白兰地的香气和辛辣味是柿子酒的主要香气特征,这与相关报道相吻合[31];其次是苯乙醇,是水果中重要的香气成分,具有清甜的玫瑰样花香,在两种柿子酒中含量分别占16.62%、7.86%,赋予柿子酒主要特征香气;仲辛醇含量也较高,分别占3.62%和2.85%,具有芳香气味,对增进柿子酒香气亦有贡献。
两种柿子酒的酯类物质种类最为丰富,分别在优势菌种和自然发酵柿子酒中检测到14种和11种,占总香气成分含量的11.52%和33.72%。两种柿子酒的酯类化合物均以3-甲基-1-丁醇乙酸酯主,其相对含量分别占4.71%、23.78%,3-甲基-1-丁醇乙酸酯使得柿子酒果香浓郁,具有类似香蕉的果香,对柿子酒总体香气产生较大的增进作用,相关文献已有报道[32-33]。
柿子酒的酸类化合物主要有乙酸、己酸、己基呋喃-2,5-二酮-3-乙酸、壬酸等,在优良菌种发酵柿子酒中检测到5种酸类化合物,相对含量2.03%,其中己基呋喃-2,5-二酮-3-乙酸的相对含量最高,占0.64%,具有果香味典型特征,对维持柿子酒浓郁的酯香等方面具有重要作用。在自然发酵柿子酒中也检测到5种酸类化合物,但种类不同,相对含量更高,为6.96%,其中相对含量最高的是乙酸,占1.92%,酸味较为刺激。优势菌种发酵柿子酒风味更为柔和醇厚。综上,柿子酒的发酵方式影响香气成分的种类和含量,呈现出不同的香气风味,优势菌种酿酒酵母(Saccharomyces cerevisiae)可以一定程度上提升柿子酒的果香和香气组分的复杂性。
3 结论
以柿果为原料分别进行自然发酵和发酵剂发酵,两种柿子酒的的感官品质相近,乙醇发酵速率相当,从自然发酵柿子酒中分离出8株优势菌种,经发酵力筛选得到1株优良酵母菌菌株J3,经分子生物学鉴定菌株J3为酿酒酵母(Saccharomyces cerevisiae),将其用于发酵制备柿酒,产品色泽清亮,无明显涩味,香气浓郁。优良菌株J3发酵柿子酒经HS-SPME-GC-MS分析共鉴定出34种香气成分,其中醇类11种、酯类13种、酸类5种和其他类5种,与自然发酵柿子酒相比,香气成分含量更高、种类更多,特别是醇类和酯类物质,对于增进柿子酒香气,改善柿子酒风味具有重要作用。研究结果可为柿子酒生产提供优良菌种基础。
[1]DONG Y,SUN W M,YUE Z H,et al.Phenotypic diversity and relationships of fruit traits in persimmon(Diospyros kaki Thunb.)germplasm resources[J].Agriculture,2023,13(9):1804.
[2]王艺儒,刁松锋,李华威,等.柿种质资源果实糖组分及含量多样性分析[J].西北农林科技大学学报(自然科学版),2023,51(11):76-85.
[3]杨恒,赵萍,刘裕慧,等.柿子资源开发利用现状[J].生物资源,2019,41(5):402-410.
[4]JIA Y Y, WANG Z, LIANG X H, et al.Unlocking the potential of persimmons: A comprehensive review on emerging technologies for postharvest challenges, processing innovations, and prospective applications[J].Food Chem,2024,459:140344.
[5]HOSSEININEJAD S,GONZÁLEZ C M,HERNANDO I,et al.Valorization of persimmon fruit through the development of new food products[J].Front Food Sci Technol,2022,2:914952.
[6]杨苗苗,吴丹,莫金凤,等.膳食纤维柿果果冻的研制[J].保鲜与加工,2023,23(10):50-55.
[7]杨苗苗,张颖,王力,等.柿果清汁饮料的开发研制[J].食品科技,2018,43(5):118-121.
[8]李白存.柿叶精油的提取工艺研究[J].应用化工,2012,41(11):1940-1942.
[9]SANT'ANA A S,JUNIOR W J F L.Microbial synergies and their impact on economic and quality innovation in sustainable winemaking:Yeast and lactic acid bacteria interconnections[J].Food Biosci,2024,62:105238.
[10]周悦.柿子酒及柿子醋的发酵工艺研究[D].西安:陕西科技大学,2014.
[11]李慧敏.红曲柿酒加工工艺及品质研究[D].南宁:广西大学,2020.
[12]GUEDES J P,CARDOSO T V,FERNANDES T,et al.Exploring wine yeast natural biodiversity to select strains with enological traits adapted to climate change[J].Heliyon,2024,10(18):e36975.
[13]陈丽花,任丽霞,李东娜,等.甜酒曲中优质酵母菌的分离鉴定及其产香特性分析[J].食品科学,2021,42(6):142-149.
[14]胡江南,高熳熳,马立娟,等.葡萄酒发酵优良酵母的筛选、鉴定及应用[J].中国酿造,2023,42(7):43-50.
[15]顾凡,晏恒,赵存朝,等.葡萄百香果酒的酿造工艺研究[J].中国酿造,2021,40(8):222-226.
[16]向丽萍,范斌强,黄娇,等.包包曲中可培养酵母菌的分离纯化与鉴定[J].酿酒科技,2021(6):29-33.
[17]尹欣,杨媛媛,闫卓洋,等.酸樱桃果酒专用酵母菌的筛选、鉴定及耐受性研究[J].中国酿造,2025,44(5):86-91.
[18]赖呈纯,赖恭梯,车建美,等.福建地区葡萄自然发酵过程中酵母菌的组成及差异分析[J].南方农业学报,2021,56(6):1655-1664.
[19]巴尼特.酵母菌的特征与鉴定手册[M].青岛:青岛海洋大学出版社,1991:53-55.
[20]赵苗苗,赵智慧,董建方,等.枸杞酒酿酒酵母的选育及其产香性能分析[J].食品与发酵工业,2022,48(18):155-161.
[21]赵海霞,王晓蕾,张琇.贺兰山东麓鲜食葡萄优良本土酿酒酵母的筛选和发酵特性研究[J].中国酿造,2025,44(1):73-79.
[22]韦璐,孙钦菊,黄杰,等.香蕉果酒发酵过程中主要成分变化规律的研究[J].食品研究与开发,2020,41(23):37-43.
[23]陈晓蝶,胡陆军,曹雨澜,等.混菌发酵对沃柑果酒品质改善作用[J].食品工业科技,2023,44(6):183-192.
[24]赵驰,朱永清,董玲,等.李子果酒主发酵过程中理化指标及挥发性成分变化分析[J].中国酿造,2019,38(9):65-68.
[25]黄庆,苏圆媛,左勇,等.耐受高浓度乙醇酿酒酵母的定向驯化及其在桑葚果酒中的应用初探[J].食品与发酵工业,2023,49(12):166-173.
[26]SUN W S,CHEN X W,FENG S N,et al.Effect of sequential fermentation with indigenous non-Saccharomyces cerevisiae combinations and Saccharomyces cerevisiae on the chemical composition and aroma compounds evolution of kiwifruit wine[J].Food Chem,2024,460:140758.
[27]CAIRNS P,HAMILTON L,RACINE K,et al.Effects of hydroxycinnamates and exogenous yeast assimilable nitrogen on cider aroma and fermentation performance[J].J Am Soc Brew Chem, 2022, 80(3): 236-247.
[28]李丹青,马恺阳,胡新中,等.柿子果酒发酵工艺优化及其香气成分的GC-MS分析[J].西北农业学报,2023,32(3):420-428.
[29]李慧敏,林凤,王玉梅,等.红曲柿酒工艺优化及挥发性风味物质分析[J].食品研究与开发,2021,42(7):126-133.
[30]凌育赵,刘经亮.柿子果酒香气成分的GC/MS分析[J].现代食品科技,2011,27(12):1530-1532.
[31]朱明明,彭泽宇,郭鑫哲,等.蓝莓添加对柿子果酒抗氧化及风味物质的影响[J].食品工业科技,2020,41(4):211-217,228.
[32]谭敏华,张巧苑,于立梅,等.柚子全果果酒发酵工艺优化及其抗氧化活性、挥发性成分分析[J].食品工业科技,2021,42(13):149-155.
[33]周得刚,徐彬艳,王青霞,等.戴尔有孢圆酵母与酿酒酵母细胞间接触对‘赤霞珠’葡萄酒风味品质的影响[J].中国农业科学,2024,57(16):3264-3282.
[34]高银祥,刘亚男,姚丽萍,等.不同品种茶籽油挥发性成分分析与比较[J].粮食与油脂,2024,37(3):40-45.
[35]巩文杰.柿子酒酿造工艺及风味特征的研究[D].天津:天津农学院,2020.