中国白酒酿造的工艺特点是制曲酿酒,制曲过程中最重要的操作是温度控制,根据制曲过程中顶温的区别可将大曲分为高温大曲、中温大曲和低温大曲,分别用于酱香、浓香和清香白酒的酿造。在高温大曲的生产过程中,在气温较低(冬天)或曲坯升温不太理想的情况下,会出现的部分高温大曲带有红心现象,但也有少数的曲块红心部位长在曲块表层的现象,即为红心曲。朱德文等[4]以酱香型红心曲为材料,筛选出1株酵母菌和3株产红色素优良的霉菌,鉴定为胶红酵母(Rhodotorula mucilaginosa)和红色红曲霉(Monascus ruber)。张柱等[5]从呈粉红色的高温大曲中分离筛选得到3株优良的功能红曲霉菌株,其中菌株H14可提高基酒产率(7.5%vol),菌株H30改善了高温大曲的酯化活性,菌株H26具有产特征风味化合物(吡嗪类物质)的潜力,其强化高温大曲中2,3,5,6-四甲基吡嗪的含量达0.27 mg/kg。王昊乾等[6]比较不同顶温对红心曲微生物群落结构及其理化性质的影响。结果表明,不同顶温红心曲中微生物多样性没有显著区别,而属水平微生物群落结构发生明显变化。顶温升高5 ℃,红心曲真菌中嗜热子囊菌(Thermoascus aurantiacus)相对丰度由原来的64.7%增至78.4%,扣囊腹膜酵母(Saccharomycopsis fibuligera)相对丰度则由33.3%降至15.2%,显著增加的还有产淀粉酶的曲霉和根霉;顶温升高后显著增加的细菌有醋酸菌、魏斯氏菌和葡萄球菌等,均有利于白酒风味的形成。理化性质方面,顶温升高5 ℃,红心曲糖化力由596.9 U降至516.1 U,液化力由1.26 U降至1.05 U,发酵力由0.74 U增至2.27 U,酒化力由7.1%vol增至8%vol。唐艺婧[7]对不同厂家及批次清香白酒酿造用红心曲的红心部分进行高通量测序,结果显示,嗜热子囊菌(Thermoascus aurantiacus)是红心曲红心部分的优势真菌,选定其中糖化力最高菌株QH-1进行生长特性研究,结果显示,菌株QH-1在马铃薯葡萄糖琼脂(potato dextrose agar,PDA)、麦芽汁琼脂(malt extract agar,MEA)和沙氏葡萄糖琼脂(Sabouraud dextrose agar,SDA)培养基中生长迅速且有红色色素产生,在合成培养基察氏及25%甘油硝酸盐琼脂基础(25%glycerol nitrate agar base,G25N)培养基上菌落生长速度较慢,几乎没有色素产生,说明菌株QH-1代谢产生红色素有生长条件限制。王婷[7]将嗜热子囊菌(Thermoascus aurantiacus)QH-1纯种曲添加到制曲原料中制备生物强化大曲,发现强化后大曲中的酯类物质含量普遍增加,如强化大曲中乙酸乙酯含量相比普通大曲提高1.115倍。制曲过程发现,嗜热子囊菌只在强化曲后期出现,与红心曲红心出现规律相似,说明嗜热子囊菌是红心曲的关键真菌。综上,清香型红心曲产红色素的优势微生物为嗜热子囊菌(Thermoascus aurantiacus),其代谢物质对白酒风味物质有一定的影响,但其产红色素的条件及其对风味的具体影响尚不明确。而在酱香型大曲制曲过程中出现的红心曲,其主要微生物为胶红酵母、红曲霉。目前对于高温大曲红心部分的理化性质、风味成分和形成原因尚不明确,对酿造的具体影响也无明确定论,探寻酱香型红心大曲的微生物成因,对于酿酒生产具有积极的意义。
本研究以酱香型红心曲为研究对象,采用常规方法对红心曲进行感官、理化及微生物指标分析,并通过用平板分离法、形态学观察及分子生物学技术对产红色素菌株进行筛选及鉴定。通过分析酱香型高温红心曲的品质及对产红色素菌株进行分离鉴定,以期揭示红心曲产生的成因,并从中选育出有潜在理论和应用价值的微生物资源,为后续制备生物强化大曲,改善酱香型白酒基酒风味提供科学依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料酱香红心曲、酒醅:茅台镇某酒厂;GF254薄层色谱硅胶:青岛海洋化工厂。
1.1.2 化学试剂
正己烷(色谱纯):德国Merck公司;聚合酶链式反应(polymerase chain reaction,PCR)扩增引物、真菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒、琼脂糖凝胶回收试剂盒、琼脂糖、DNAMarker:生工生物工程(上海)股份有限公司。
1.1.3 培养基
孟加拉红培养基:蛋白胨5 g/L,磷酸二氢钾1.0 g/L,硫酸镁0.5 g/L,葡萄糖10.0 g/L,氯霉素0.1 g/L,孟加拉红0.033 g/L,琼脂20.0 g/L。121 ℃灭菌15 min。
营养琼脂培养基:蛋白胨10.0 g/L,氯化钠5.0 g/L,牛肉膏粉3.0 g/L,琼脂15.0 g/L。121 ℃灭菌15 min。
马铃薯葡萄糖琼脂(PDA)培养基:马铃薯3.0 g/L,葡萄糖20.0 g/L,琼脂14.0 g/L。121 ℃灭菌15 min。
1.2 仪器与设备
SW-CJ-2FD型双人单面净化工作台:浙江孚夏医疗科技有限公司;LDZX-50KBS型立式压力蒸汽灭菌器:上海申安医疗器械厂;FA2204N型电子天平:上海菁海仪器有限公司;DM300型显微镜:徕卡微系统(瑞士)有限公司;XW-80A旋涡混合器:江苏海门市其林贝尔仪器制造有限公司;FQD-96A荧光定量PCR仪:杭州博日科技股份有限公司。
1.3 方法
1.3.1 大曲感官分析
邀请10名有经验的高温大曲制作/感官评价专业人员,依据QB/T 4257—2011《酿酒大曲通用分析方法》对大曲外观、断面、曲皮厚、曲香等进行感官评价。感官评价标准:①外观:在适宜光线(非直射阳光)下,从大曲六个面立体观察曲坯表面菌丝颜色、穿衣、裂缝及光洁度等外表特征,并进行记录。②断面:将曲块断开,观察界面上菌丝形态、颜色、菌斑、泡气等情况,并进行特征记录。③曲皮厚:对曲块表层未发酵的生淀粉及菌丝不密集部分的厚度(并非水圈以外部分)进行观测和记录。④曲香:嗅闻大曲断面散发出来的香气,分辨是否纯正、有无复合曲香,检查有无异杂味,并进行记录。
1.3.2 大曲样品采集与编码
将采集的2块高温大曲样和2块红心曲样进行分样,将一块高温大曲曲心分离出来(大曲其他部分用锤子敲掉,保留曲心部分),单独粉碎得到1号样品:高温大曲曲心样(PX1);另一块高温大曲整曲进行粉碎得到2号样品:高温大曲整曲样(PQ2);将一块红心曲样红色部分分离出来(其他部分用锤子敲掉),单独粉碎得到3号样品:红心曲曲心样(HX3);另取一块红心曲不做分离,直接粉碎得到4号样品:红心曲整曲样(HQ4)。
1.3.3 分析检测
大曲理化指标:采用QB/T 4257—2011《酿酒大曲通用分析方法》[1]测定大曲的水分含量、酸度、淀粉含量、糖化力、发酵力及酯化力。
大曲微生物指标:采用平板菌落计数法对红心曲和普通大曲的全曲和曲心样品中的酵母菌、细菌及霉菌数量进行检测。酵母菌和霉菌均采用孟加拉红培养基,细菌采用营养琼脂培养基。具体方法参照GB 4789.2—2022《食品微生物学检验菌落总数测定》。
1.3.4 实验室模拟发酵
实验室模拟堆积发酵:用粉碎后红心曲全曲样品(HQ4)、红心曲曲心样品(HX3)和普通大曲样品(PQ2)作为糖化发酵剂,取正常酿酒车间二轮次摊晾后拌曲前的酒醅进行实验室模拟堆积发酵。具体步骤如下:称取500 g酒醅(二轮次生产过程中摊晾结束,拌曲前酒醅)拌入约60 g的曲粉,将曲粉和酒醅充分混匀后取出部分酒醅(约20 g)作为检测样品,剩余部分进行常温堆积发酵。堆积发酵约4 d后,结束发酵。将堆积发酵前后样品进行感官及理化分析,比较堆积前后的差异。
实验室模拟窖池发酵:将模拟堆积发酵后的酒醅进行实验室模拟窖池发酵。具体步骤如下:将堆积结束后的酒醅装入发酵瓶中,使用玻璃棒混匀或摇晃振荡瓶身尽量减少酒醅在瓶中的空隙。用不透气的密封膜封口,确保发酵瓶密封性良好。将装好酒醅的发酵瓶置于36 ℃的恒温培养箱中进行模拟窖池发酵30 d后取出。将结束模拟窖池发酵的酒醅进行理化指标检测。酒醅理化指标检测方法参照DB 34/T 2264—2014《固态发酵酒醅分析方法》。
1.3.5 产红色素微生物的筛选
利用稀释涂布平板法进行菌种分离、纯化。称取酱香型红心曲样5 g于45 mL无菌生理盐水在混合器上混合均匀,记作10-1,以10倍稀释法稀释为10-2、10-3、10-4、10-5、10-6、10-7,取10-3~10-6,4种稀释液各0.2 mL接种到各无菌分离培养基平板上,每个梯度做3个平行。于30 ℃倒置培养3~5 d。待平板上长出单菌落,从平板中依次挑出特征性红色单菌落,利用平板划线对挑出的特征性菌落进行多次纯化培养得到纯种菌株,于4 ℃下斜面保存,备用。
1.3.6 产红色素菌株的鉴定
(1)霉菌及酵母菌形态学观察
显微镜观察霉菌菌丝的形态、有无横隔,分枝情况;分生孢子着生方式、形状;有无闭囊壳及其形状等。将待检酵母菌株,于PDA培养基30 ℃培养2 d,选取酵母单个菌落观察其颜色、形状、边缘整齐、光滑、湿润和透明度等菌落形态。无菌条件下,挑取少量菌体于无菌生理盐水中,混合均匀,盖上盖玻片,显微镜下观察酵母细胞形态。
(2)菌株的分子生物学鉴定
利用真菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒提取霉菌和酵母的基因组DNA。以基因组DNA为模板,用真菌内部转录间隔区(internal transcribed spacer,ITS)通用引物进行聚合酶链式反应(PCR)扩增。
霉菌引物序列:正向引物ITS1(5'-TCCGTAGGTGAACCTGCGG-3'),反向引物ITS4(5'-TCCTCCGCTTATTGATATGC-3');酵母引物序列:正向引物NL1(5'-GCATATCAATAAGCGGAGGAAAAG-3'),反向引物NL4(5'-GGTCCGTGTTTCAAGACGG-3')。
PCR扩增体系:基因组DNA 20~50 ng/μL 0.5 μL,10×Buffer(含Mg2+)2.5 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)(各2.5 mmol/L)1 μL,DNA聚合酶0.2 μL,正向引物(F)(10 μmol/L)0.5 μL,反向引物(R)(10 μmol/L)0.5 μL,加双蒸水(ddH2O)至25 μL。PCR扩增条件:94 ℃预变性4 min,94 ℃变性45 s,55 ℃退火45 s,72 ℃延伸1 min,30个循环,72 ℃修复延伸10 min,4 ℃保存。
按Takara![]() 18-T Vector连接试剂盒进行克隆测序,将测序所得序列利用CExpress软件7.0完成拼接,得到目的基因序列。将基因测序结果提交至美国国家生物技术信息中心(national center for biotechnology information,NCBI)GeneBank数据库进行基本局部比对搜索工具(basic local alignment search tool,BLAST)进行同源性序列比对,然后利用MEGA11.0软件中的邻接(neighbor joining,NJ)法构建系统发育树。
18-T Vector连接试剂盒进行克隆测序,将测序所得序列利用CExpress软件7.0完成拼接,得到目的基因序列。将基因测序结果提交至美国国家生物技术信息中心(national center for biotechnology information,NCBI)GeneBank数据库进行基本局部比对搜索工具(basic local alignment search tool,BLAST)进行同源性序列比对,然后利用MEGA11.0软件中的邻接(neighbor joining,NJ)法构建系统发育树。
2 结果与分析
2.1 红心曲的感官评价
高温大曲是酱香型白酒生产使用的糖化发酵剂,其制曲原料是小麦。小麦经润料、粉碎、踩曲等工艺环节,进入发酵仓经高温发酵后,出仓成为高温大曲成品曲。出仓后的高温大曲还需经3~6个月的贮存,再投入制酒生产。
高温大曲的出仓曲按照发酵程度、曲坯颜色及香味等可以分为黄曲、黑曲和白曲。由于曲坯在发酵仓中的位置不同,导致其发酵程度存在差异,故每一仓曲都有一定比例的黄曲、黑曲和白曲。发酵理想的发酵仓,黄曲比例在83%以上,黑曲不高于5%,白曲10%~15%。在制曲过程中,除了常规的黑、白、黄曲,有时候也会有一些曲心呈现红色的曲块,红心曲主要出现在曲坯升温不太理想的发酵仓内。以高温大曲为对照,红心曲外观见图1,感官评价结果见表1。
表1 高温大曲和红心曲感官评价结果
Table 1 Sensory evaluation results of high-temperature Daqu and Hongxinqu

高温大曲 红心曲外观断面曲皮厚曲香曲坯表面菌丝呈灰白色,穿衣良好,有裂缝,裂缝内菌丝呈灰白色、生长良好,曲坯色泽较均一,呈黄褐色,光洁度良好曲坯断面菌丝生长良好,颜色灰白色,无明显菌斑、泡气等。层次明显,色泽基本一致为黄褐色曲皮较薄,约0.5 cm有浓郁的曲香、酱香、酱味等复合曲香,香气纯正,具有典型的酱香大曲风格,无异杂味曲坯表面菌丝呈灰白色,穿衣良好,无裂缝,曲坯色泽较均一,呈浅黄色,光洁度好于高温大曲曲坯断面菌丝生长良好(差于高温大曲),颜色灰白色。曲心有明显红色菌斑,无泡气。层次明显,曲心呈现红色,外部呈现浅黄色曲皮较厚,约0.8 cm有复合曲香,酱香不明显,曲心部分有淡淡的霉味,略带酯香,略有异味,香气不太纯正

图1 高温大曲(a)与红心曲(b)外观比较
Fig.1 Comparison of the appearance of high-temperature Daqu (a)and Hongxinqu (b)
由表1可知,高温大曲曲坯表面菌丝呈灰白色,穿衣良好,有裂缝,裂缝内菌丝呈灰白色、生长良好,曲坯色泽较均一,呈黄褐色,光洁度良好。曲坯断面菌丝生长良好,颜色灰白色,无明显菌斑、泡气等。层次明显,色泽基本一致为黄褐色。曲皮较薄,约0.5 cm;有浓郁的曲香、酱香、酱味等复合曲香,香气纯正,具有典型的酱香高温大曲风格,无异杂味。而红心曲曲坯表面菌丝呈灰白色,穿衣良好,无裂缝,曲坯色泽较均一,呈浅黄色,光洁度好于高温大曲;曲坯断面菌丝生长良好(差于高温大曲),颜色灰白色。曲心有明显红色菌斑,无泡气。层次明显,曲心呈现红色,外部呈现浅黄色。曲皮较厚,约0.8 cm,具有复合曲香,酱香不明显,曲心部分有淡淡的霉味,略带酯香,略有异味,香气不太纯正。从感官指标来看,红心曲与普通高温大曲有显著差异,其感官差异的不同可能是不同优势微生物发酵及其代谢风味差异导致的。酱香型高温大曲在发酵过程中经常有红心曲出现,推测其对基酒的风味有一定的贡献作用。
2.2 红心曲的理化指标
以高温大曲为对照,红心曲理化指标分析结果见图2。水分含量是鉴别高温大曲出仓曲合格与否的重要指标之一,发酵良好的出仓曲水分含量一般在13%以下。由图2a可知,高温大曲曲心与整曲的水分含量差异不明显,而红心曲曲心水分含量(12.61%)明显高于整曲(11.64%),说明大曲产红色素位置发酵略差,存在轻微窝水现象。红心曲曲心酸度达到2.07 mmol/10 g,明显高于红心曲整曲,而红心曲整曲酸度明显高于普通大曲,说明红心曲的发酵存在产酸倾向。红心曲淀粉含量(曲心48.77%,整曲46.04%)明显低于普通大曲(曲心59.37%,整曲53.67%),说明红心曲在发酵过程中淀粉消耗较大,在一定程度上会降低制酒过程中淀粉的有效利用。
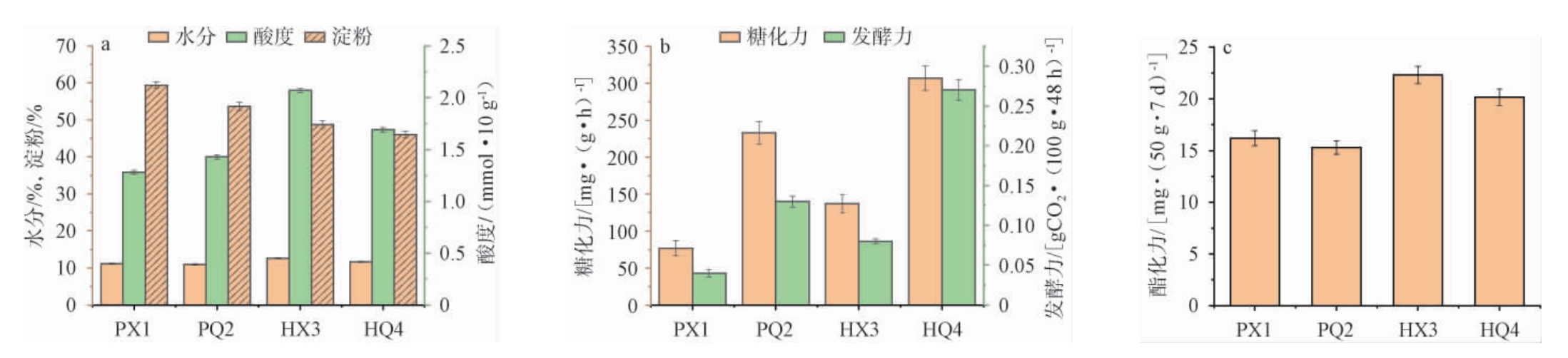
图2 高温大曲与红心曲水分、淀粉、酸度(a)及糖化力、发酵力(b)、酯化力(c)比较
Fig.2 Comparison of moisture, starch, acidity (a), saccharification power, fermentation power (b) and esterification power (c) of high-temperature Daqu and Hongxinqu
固体曲中的糖化酶(包括α-淀粉酶和β-淀粉酶)能将淀粉水解为葡萄糖,进而被微生物发酵,生成酒精。糖化酶活力高,淀粉利用率就高[2]。生曲中的糖化力较高,主要源于小麦本身富含较多的糖化酶,糖化酶活力在制曲过程中呈现波动性变化,一方面物料本身的糖化酶活力开始下降,同时由霉菌生长代谢所产生的糖化酶活力开始上升。最后出仓曲中的糖化酶活力在一定程度上反映了大曲的发酵情况。大曲的发酵程度越高,嗜热微生物含量越丰富,糖化力越低。由图2b可知,红心曲整曲的糖化酶活力高于高温大曲,推测红心曲的发酵略差于高温大曲[31]。红心曲曲心的糖化酶活力明显低于高温大曲,说明产红色素的微生物产糖化酶能力较弱。红心曲整曲及曲心的发酵力均明显高于普通高温大曲,说明红心曲具有良好的发酵糖产酒精能力。由图2c可知,红心曲的酯化力明显高于普通大曲,说明红心曲具有较好的催化生成酯类物质的能力。
从理化指标来看,红心曲产酸产酯能力要由于普通高温大曲,说明其具有潜在的可以提升基酒酸酯风味能力。
2.3 红心曲的微生物指标
高温大曲在发酵过程中,曲坯最高顶火温度可以达到65 ℃以上,属于典型的高温发酵,因而高温大曲中酵母菌含量较低。但在出仓曲中依然可以检测到少量的酵母菌,一方面是因为高温大曲发酵顶火温度最高虽然可以达到65 ℃以上,但并非整仓曲坯的温度都可以顶到这么高,处于门口、窗边及最上层的曲块温度相对要低一些。这也是高温大曲出仓曲分为黑曲、白曲、黄曲的主要原因。顶火温度不太高的曲块,发酵程度要弱一些,形成白曲。白曲作为出仓曲的组成之一,其糖化力较高,在制酒发酵淀粉糖化过程中起着重要作用。另一方面是因为制曲过程中存在耐热酵母菌,使其在高温条件下能够存活[3]。以高温大曲为对照,红心曲的微生物指标检测结果见图3。由图3可知,酵母菌在高温大曲及红心曲中的含量(红心曲曲心6.9×103 CFU/g,高温大曲曲心3.6×103 CFU/g)差异不明显。红心曲与高温大曲主要差异是霉菌含量高(红心曲曲心8.0×104 CFU/g,高温大曲曲心2.5×104 CFU/g),细菌含量低(红心曲曲心2.8×105 CFU/g,高温大曲曲心3.5×106 CFU/g)。从微生物指标来看,红心曲与高温大曲的微生物组成具有显著差异性。
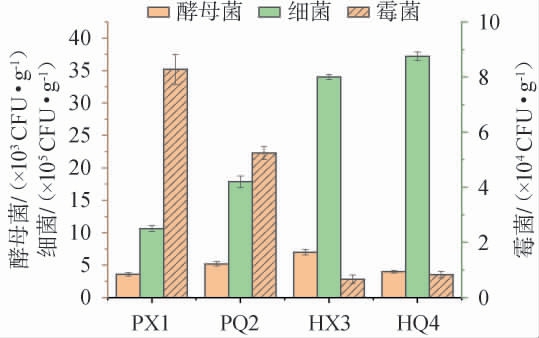
图3 高温大曲与红心曲微生物指标比较
Fig.3 Comparison of microbial indicators of high-temperature Daqu and Hongxinqu
2.4 红心曲模拟窖池发酵酒醅理化指标分析
大曲中的微生物经过拌曲的过程进入酒醅,参与酒醅的堆积发酵与窖内发酵。水分是微生物代谢产物之一,其含量的变化在一定程度上反映了微生物的代谢活性。以高温大曲为对照,红心曲模拟窖池发酵酒醅理化指标分析结果见图4。
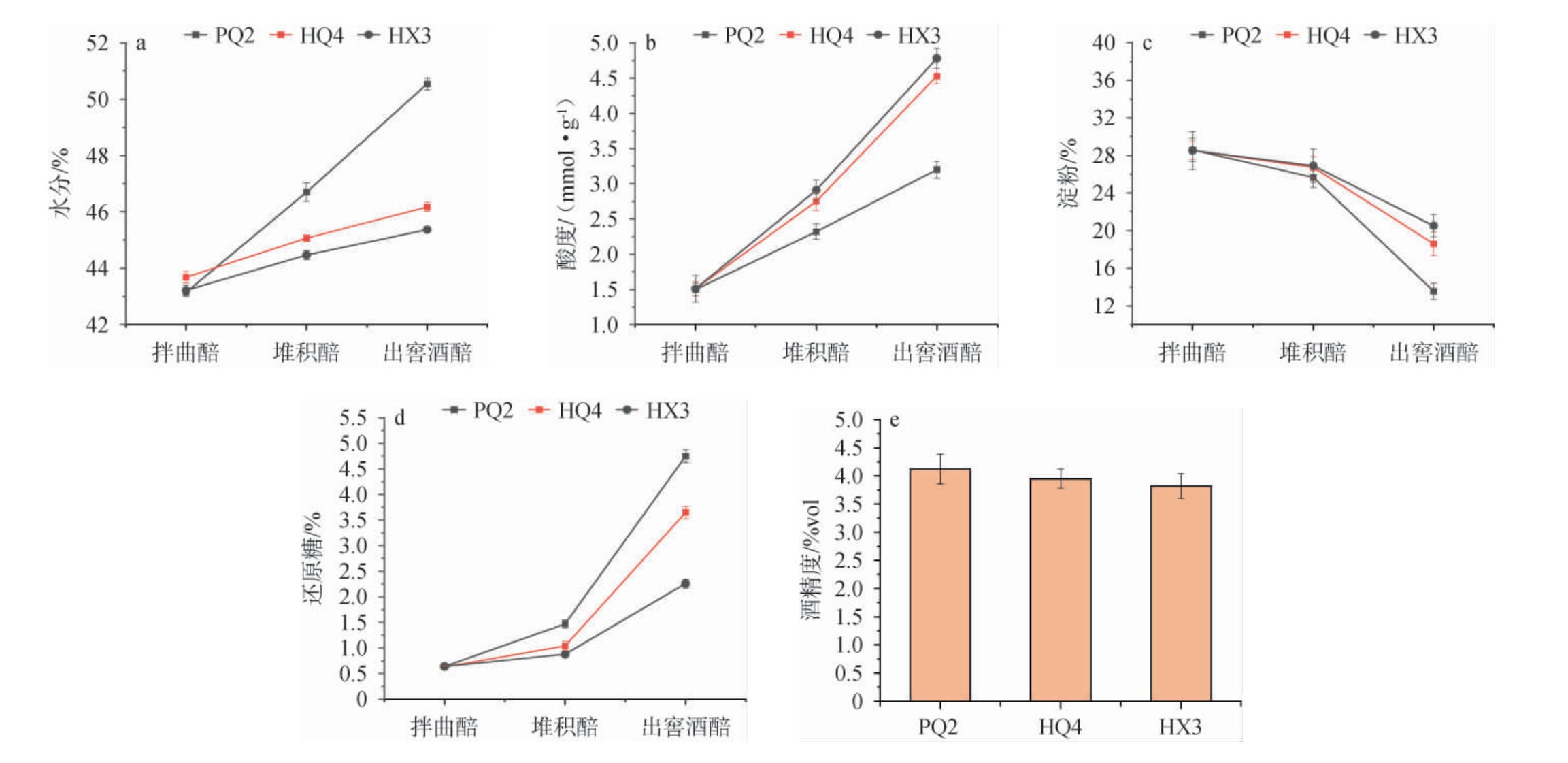
图4 红心曲模拟窖池发酵过程中酒醅水分(a)、酸度(b)、淀粉(c)、还原糖(d)及酒精度(e)测定结果
Fig.4 Determination results of moisture (a), acidity (b), starch (c), reducing sugar (d) and alcohol content (e) of fermented grains during simulated pit fermentation process of Hongxinqu
由图4a可知,拌高温大曲与红心曲后酒醅的水分含量差异不大,经堆积发酵后,拌普通大曲的酒醅水分含量有显著提高,由43.15%提升到46.70%,水分含量提升了3.55个百分点,经窖内发酵后,酒醅的水分含量提升到50.54%,水分含量提升了3.84%,整个发酵过程,水分含量提升了7.39%。拌红心曲全曲的酒醅,经堆积发酵后,酒醅水分含量由43.68%提升到45.07%,提升了1.49%,经窖内发酵后,酒醅的水分含量提升到46.17%,水分含量提升了1.10%,整个发酵过程,水分含量提升了2.59%,远低于拌高温大曲的酒醅。拌红心曲曲心的酒醅,经堆积发酵后,酒醅水分含量由43.22%提升到44.47%,提升了1.25个百分点,经窖内发酵后,酒醅的水分含量提升到45.37%,水分含量提升了0.90个百分点,整个发酵过程,水分含量提升了2.15%,远低于拌高温大曲的酒醅,略低于拌红心曲全曲的酒醅。
酒醅中的酸主要由乳酸、乙酸等组成,其主要是由大曲及酒醅中产酸微生物代谢的产物。酒醅中酸含量的高低与其微生物的构成及发酵环境有极大的关系。由图4b可知,拌不同曲后酒醅的酸度差异不大,经堆积发酵后,拌高温大曲的酒醅酸度有所提高,由1.50 mmol/10 g提升到2.32 mmol/10 g,酸度提升了0.82 mmol/10 g,经窖内发酵后,酒醅的酸度提升到3.20mmol/10g,酸度提升了0.88mmol/10g,整个发酵过程,酸度提升了1.70 mmol/10 g。拌红心曲全曲的酒醅,经堆积发酵后,酒醅酸度由1.50 mmol/10 g提升到2.75 mmol/10 g,提升了1.25 mmol/10 g,经窖内发酵后,酒醅的酸度提升到4.53 mmol/10 g,酸度提升了1.78 mmol/10 g,整个发酵过程,酸度提升了3.03 mmol/10 g。拌红心曲曲心的酒醅,经堆积发酵后,酒醅酸度由1.50 mmol/10 g提升到2.91 mmol/10 g,提升了1.41 mmol/10 g,经窖内发酵后,酒醅的酸度提升到4.78 mmol/10 g,酸度提升了1.87 mmol/10 g,整个发酵过程酸度提升了3.28 mmol/10 g,明显高于拌高温大曲的酒醅,略高于拌红心曲全曲的酒醅。
酒醅中的淀粉是酿酒微生物的营养来源,淀粉在大曲微生物代谢的液化酶、糖化酶等作用下被分解为还原糖,进一步被产酒、产酸及产风味微生物等代谢为醇类、酸类、吡嗪、醛酮类等酒体主要物质成分。由图4c可知,拌不同曲后酒醅的淀粉差异不大,经堆积发酵后,拌高温大曲的酒醅淀粉含量下降明显,由28.59%下降到25.67%,经窖内发酵后,降至13.56%,整个发酵过程,淀粉含量降低了15.03个百分点。拌红心曲全曲的酒醅,经堆积发酵后,淀粉含量由28.54%降至26.73%,经窖内发酵后,酒醅的淀粉含量降至18.61%,整个发酵过程,淀粉降低了9.93个百分点。拌红心曲曲心的酒醅,经堆积发酵后,淀粉含量由28.53%降至26.91%,经窖内发酵后,酒醅的淀粉含量降至20.52%,整个发酵过程,淀粉降低了8.01个百分点,明显低于拌高温大曲的酒醅,略低于拌红心曲全曲的酒醅。
酱香型白酒的堆积发酵及窖内发酵均是边糖化边发酵的过程,酒醅还原糖含量的多少一方面取决于大曲的糖化力,一方面取决于酒醅的发酵活性。由图4d可知,拌高温大曲的酒醅经堆积后及窖内发酵后还原糖含量显著提高,说明高温大曲可持续糖化力较好。拌红心曲全曲的酒醅经堆积后及窖内发酵后还原糖含量也有较大程度提高。由图4e可知,拌红心曲全曲的酒醅出窖酒醅酒精度达到3.95%vol,说明红心曲全曲的可持续糖化力良好。拌红心曲曲心的酒醅经堆积后及窖内发酵后还原糖含量也有所提高,但提升幅度较小,出窖酒醅酒精度达到3.82%vol,说明红心曲曲心的可持续糖化力虽然低于高温大曲及红心曲全曲,但也能满足发酵需求。
通过实验室模拟堆积及窖内发酵过程,明确红心曲虽然发酵活力、可持续糖化能力略差于普通大曲,但其产酒能力可以满足实际需求,产酸酯能力突出,若是能与普通大曲搭配使用可以有效提升基酒的酸酯含量,从而提升基酒风味。
2.5 产红色素微生物的筛选与鉴定
2.5.1 产红色素菌株菌落及细胞形态特征
为明确红心曲产红色素微生物的种属,利用稀释涂布平板法进行菌种分离、纯化,得到3株产红色素的菌株,分别命名为B1、B2、A1。菌株B1、B2、A1菌落及细胞形态特征见图5。
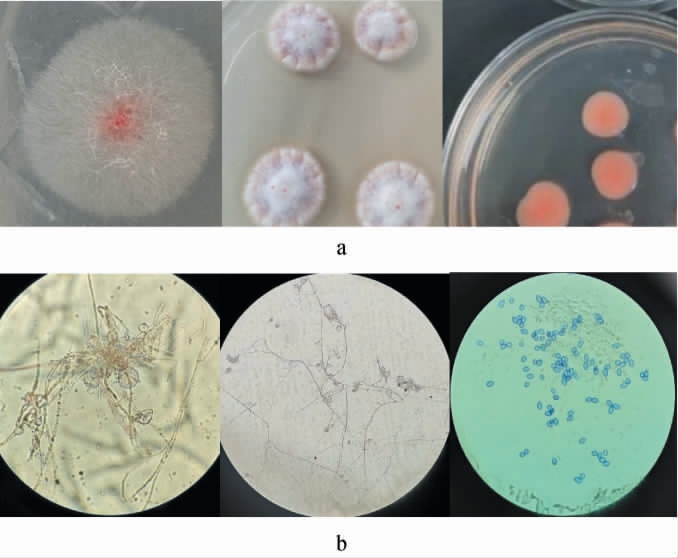
图5 菌株B1、B2及A1菌落(a)及细胞(b)形态
Fig.5 Colony (a) and cell (b) morphology of strains B1, B2 and A1
由图5a可知,菌株B1培养72 h,菌落较平坦(吸附力较强),菌丝呈绒毛状,整体呈白色带红色,菌落中心红色较明显,向外延申,红色逐渐变淡。菌株B2培养72 h,菌落有凸起褶皱(吸附力较强),菌丝短小密集,整体呈白色带橙红色。菌株A1培养72 h,菌落圆形,边缘整齐,整体呈粉红色,表面光滑、湿润,不透明。由图5b可知,菌株B1细胞形态有错综复杂的成串菌丝,有横隔,多核、闭囊壳成鸭梨形,菌丝体大量分枝,在分支的顶端产生无色透明的子囊孢子。菌株B2细胞形态有错综复杂的成串菌丝,即菌丝无色,具分枝和隔膜,产生闭囊壳,球形。子囊簇生,光滑,易消解,卵圆形。子囊孢子无规则排列,卵圆形至椭圆形。菌株A1细胞形态呈卵圆形,直径约5 μm,有出芽生殖现象。
2.5.2 分子生物学鉴定
以菌株B1、B2及A1的基因组DNA为模板,PCR扩增出菌株ITS区序列,电泳检测结果见图6。由图6可知,菌株B1、B2碱基大小约为556 bp,菌株A1碱基大小约为643 bp。
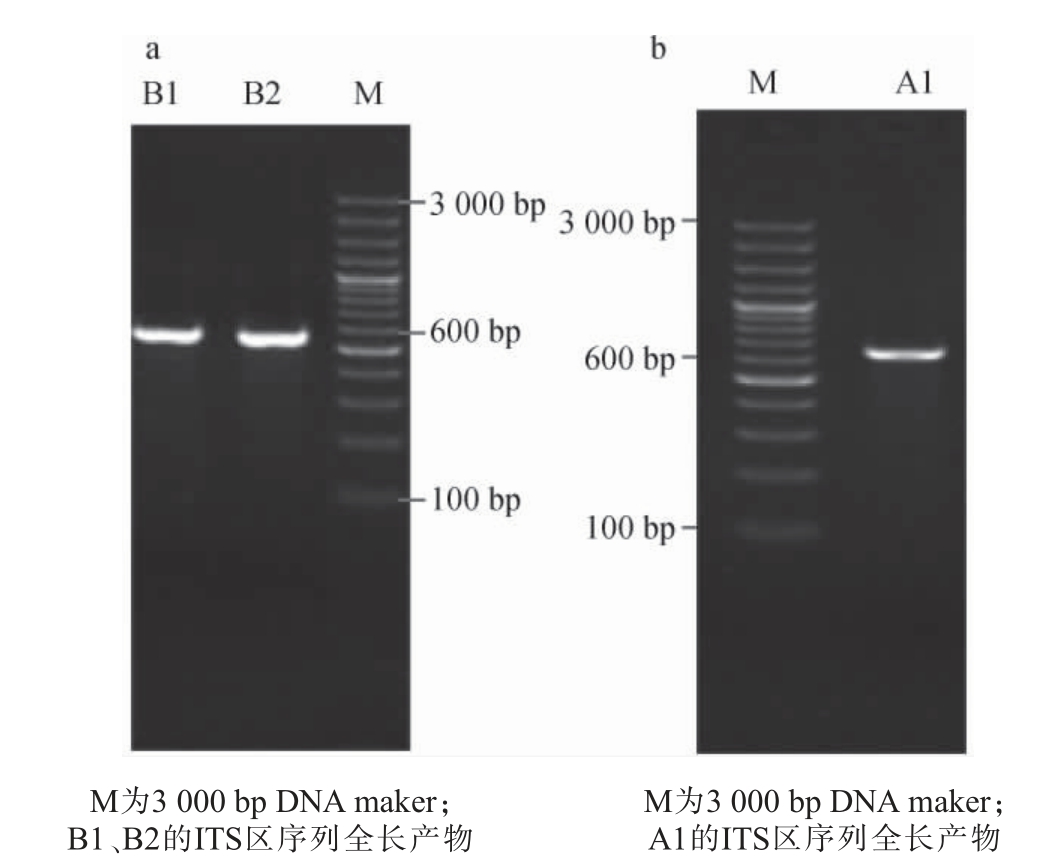
图6 菌株B1、B2(a)及A1(b)ITS rDNA基因序列电泳检测结果Fig.6 Results of electrophoresis detection of ITS rDNA gene
sequences of strains B1, B2 (a) and A1 (b)
将测序所得到的18S rDNA、ITS、26S rDNA序列提交至NCBI进行BLAST序列比对,结果见图7。由图7可知,菌株B1、B2与紫红曲霉(Monascus purpureus)、火红色红曲霉(Monascus rutilus)及 橙 色 红 曲 霉(Monascus aurantiacus)的匹配率均为99.82%,结合样本形态学观察结果,菌株B1被鉴定为火红色红曲霉(Monascus rutilus),菌株B2被鉴定为橙色红曲霉(Monascus aurantiacus)。菌株A1与生泡囊担孢酵母属(Cystobasidium)的相似度为99.53%,结合样本形态学观察结果,菌株A1被鉴定为生泡囊担孢酵母属(Cystobasidium)。

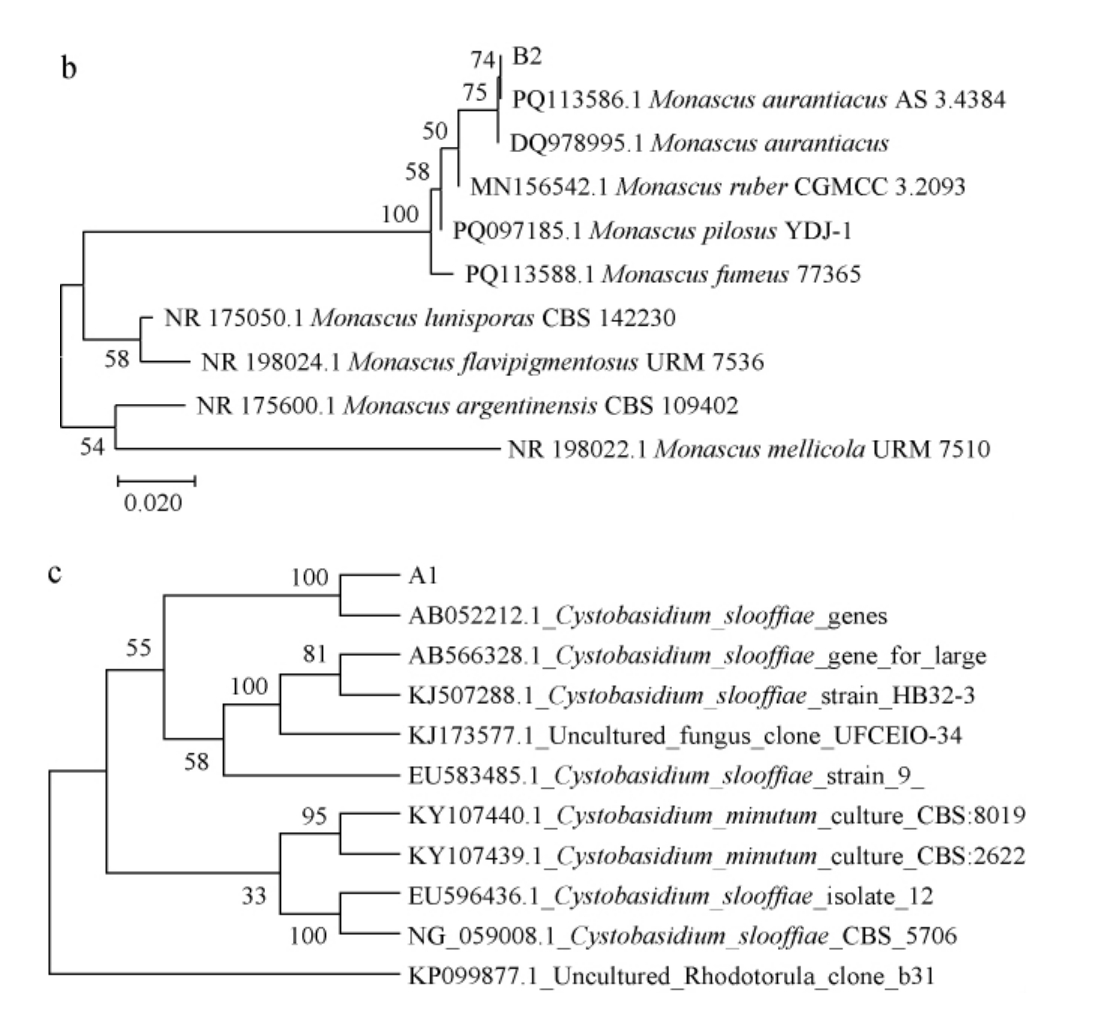
图7 基于ITS rDNA基因序列菌株B1(a)、B2(b)及A1(c)系统发育树
Fig.7 Phylogenetic tree of strains B1(a), B2(b) and A1(c) based on ITS rDNA gene sequence
3 结论
本研究以酱香型红心曲为研究对象,采用常规方法对红心曲进行感官、理化及微生物指标分析,并通过稀释涂布平板法、形态学观察及分子生物学技术对产红色素菌株进行筛选及鉴定。结果表明,红心曲曲坯表面菌丝呈灰白色,穿衣良好,无裂缝,曲坯色泽较均一,呈浅黄色,光洁度优于高温大曲;曲坯断面菌丝生长良好,曲心有明显红色菌斑;曲皮较厚,约0.8 cm,有复合曲香,酱香不明显,曲心部分有淡淡的霉味,略带酯香。红心曲水分12.61%、酸度2.07 mmol/L,均高于普通高温大曲;淀粉含量48.77%,低于高温大曲。红心曲、高温大曲曲心霉菌数、细菌数分别为8.0×104 CFU/g、2.5×104 CFU/g;2.8×105 CFU/g、3.5×106 CFU/g。从红心曲中筛选出3株产红色素菌株(编号分别为B1、B2、A1),菌株B1、B2、A1分别被鉴定为火红色红曲霉(Monascus rutilus),橙色红曲霉(Monascus aurantiacus)以及生泡囊担孢酵母属(Cystobasidium)。
通过实验室模拟堆积及窖内发酵,明确红心曲虽然发酵活力、可持续糖化能力略差于普通大曲,但其产酒能力可以满足实际需求,产酸酯能力突出,若是能与普通大曲搭配使用可以有效提升基酒的酸酯含量,提升基酒风味。
[1]李喆,冯海燕,吴德光,等.高温大曲发酵过程中理化指标及风味变化规律的研究[J].酿酒科技,2022(10):40-45.
[2]沈怡方.白酒生产技术全书[M].北京:中国轻工业出版社,2020:618-619.
[3]王珍,张永利,孟勤燕,等.耐高温高产酒精酵母的筛选及其大曲生产应用研究[J].酿酒科技,2020(1):107-114.
[4]朱德文,蒋英丽,高鸿,等.酱香型红心曲中产红色素功能菌株的分离筛选[J].酿酒科技,2014(10):27-31.
[5]张柱,黄钧,周荣清,等.高温大曲中功能红曲霉菌株的筛选与功能浅析[J].中国酿造,2024,43(4):53-61.
[6]王昊乾,刘昌录,顾铁刚,等.顶温对红心曲微生物群落结构及理化性质的影响[J].中国食品学报,2024,24(3):75-85.
[7]唐艺婧.红心曲红心部分优势真菌的分离纯化及生物学功能分析[D].太原:山西师范大学,2023.
[8]王婷.黄嗜热子囊菌QH-1的生物强化对红心曲的影响[D].太原:山西师范大学,2024.
[9]TAN J,CHU J,WANG Y,et al.High-throughput system for screening of Monascus purpureus high-yield strain in pigment production[J].Bioresource Bioproc,2014,1(1):1-7.
[10]SHI W, CHAI L J, ZHAO H, et al.Deciphering the effects of different types of high-temperature Daqu on the fermentation process and flavor profiles of sauce-flavor Baijiu[J].Food Biosci,2024,61:104917.
[11]LIU Y B,WU J Y,LI H D,et al.Combined microbiome and metabolomics analysis of Taorong-type Baijiu high-temperature Daqu and mediumtemperature Daqu[J].Peer J,2024,12:e16621.
[12]DU Y L, SHIM S M, WANG L, et al.Impact of Monascus purpureus combined with Lactobacillus plantarum and Saccharomyces cerevisiae fermentation on nutritional and flavor characteristics of Pyropia yezoensis[J].Food Chem,2025,472:142973.
[13]XU Y Q,WANG X C,LIU X,et al.Discovery and development of a novel short-chain fatty acid ester synthetic biocatalyst under aqueous phase from Monascus purpureus isolated from Baijiu[J].Food Chem, 2021,338:128025.
[14]REN X Y,HE Z G,LIN X Z,et al.Screening and evaluation of Monascus purpureus FJMR24 for enhancing the raw material utilization rate in rice wine brewing[J].J Sci Food Agr,2020,101(1):185-193.
[15]翟威涛,吴双全,柴丽娟,等.酱酒酒醅中普通高温放线菌的筛选及其挥发性物质代谢分析[J].食品科学,2025,46(12):118-126.
[16]邓阿玲,唐杰,朱楚天,等.黑色高温大曲在固态发酵过程中的微生物群落及风味化合物演替驱动机制[J].食品科学,2024,45(23):102-112.
[17]梁二宏,李金洋,李微微,等.3种高温大曲功能特征与微生物群落结构差异性分析[J].食品科学,2024,45(21):166-175.
[18]史洪丽,余梦婷,王世昕,等.高温大曲中高产四甲基吡嗪芽孢杆菌的筛选及其在酒醅堆积中的应用[J].中国酿造,2025,44(3):59-65.
[19]张柱,黄钧,周荣清,等.红曲霉对高温大曲的扰动及制曲工艺探究[J].食品与发酵工业,2025,51(2):275-284.
[20]杜琳琳,赵祥颖,刘丽萍,等.红曲霉菌的筛选及其在液态食醋酿造中的应用[J].中国调味品,2024,49(1):33-39.
[21]郑平,覃先武,张彦,等.高产开环型monacolin K红曲霉菌株的筛选及其在红曲酒酿造中的应用[J].中国酿造,2023,42(3):129-134.
[22]赵江林,陈林,刘钰浩,等.一株产类胡萝卜素酵母的鉴定及其对猕猴桃酒风味的影响[J].食品与发酵工业,2020,46(16):49-55.
[23]王晓丹,庞博,陆安谋,等.酱香型白酒堆积过程中酵母变化趋势研究[J].食品工业,2014,35(12):42-44.
[24]CAO L B,SUN H M,XU Z Y,et al.Metagenomic and physicochemical profiling reveal microbial functions in pit mud for Jiang-Nong Jianxiang Baijiu fermentation[J].BMC Microbiol,2025,1(25):190.
[25]YANG H L,HU X J,TIAN J P,et al.Exploring the influence of pottery jar formula variables on flavor substances through feature ranking and machine learning:Case study of Maotai-flavored Baijiu[J].Foods,2025,6(14):1063.
[26]NIU J,YAN Y H,ZHANG G H,et al.Temporal and workshop heterogeneity of microbial communities with physicochemical properties and flavor substances during stacked fermentation of sauce-flavor Baijiu[J].Foods,2025,6(14):929-929.
[27]CAO Y, ZHANG H X, DU H, et al.Microorganisms and metabolic characteristics of temperature-dependent fermentation during sauce-flavor Baijiu production[J].Food Biosci,2025,63:105787.
[28]魏雯丽,刘宜睿,程伟,等.酱香型白酒封窖泥微生物多样性及理化特性解析[J].食品科技,2025,50(2):1-10.
[29]谢丹,吴成,赵雯宇,等.酱香型白酒一轮次堆积过程微生物多样性及风味分析[J].食品研究与开发,2025,46(1):194-201.
[30]龙亚飞,郭淳钦,朱孜,等.酱香型白酒前三轮次堆积发酵过程中四甲基吡嗪变化规律研究[J].酿酒科技,2024,12:47-51,60.
[31]唐佳代,石雨菲,赵益梅,等.不同感官特性酱香型大曲理化指标与霉菌群落关联分析[J].食品工业科技,2024,45(3):153-161.
[32]丁润月,李姝,魏阳,等.不同颜色高温大曲形成机理及特性差异研究进展[J].食品与发酵工业,2025,51(11):376-384.