我国是世界上最早发明蒸馏酒的国家,我国白酒与威士忌、伏特加、白兰地、朗姆酒和金酒并称为世界六大蒸馏酒[1-2]。其中,保健酒在白酒的基础上发展起来,因具有保健功能在白酒市场中扮演者愈发重要的角色。保健酒是指以蒸馏酒、发酵酒或食用酒精为基酒,加入可食用、药食两用的辅料,进行调配、加工制成的具有保健功能的饮料酒,是属于露酒范畴[3]。复方保健酒是以清香型白酒为基酒,以多味药材为原料,按照科学的用量配比经过数字化提取精制而成[4]。本文研究的复方保健酒主要以西红花、蛹虫草为主要原料。西红花和蛹虫草均是名贵的药食同源食品,其中西红花具有活血化瘀、凉血解毒、解郁安神的功效[5],在治疗抑郁症、护肝、抗炎、神经保护以及抗糖尿病[6-10]等方面有一定作用。蛹虫草富含虫草素、虫草酸、腺苷、多糖等生物活性物质,具有抗氧化[11]、免疫调节[12]、抗癌[13]、抗菌[14]、抗炎[15]、抗病毒[16]等功效。
随着保健酒市场的快速发展,保健酒的功能成分的检测逐渐成为研究的热点。高效液相色谱(high performance liquid chromatography,HPLC)因其灵敏性高、分析速度快、分离效能好等优点被广泛用于功能成分的检测[17-19]。彭志强等[20]利用高效液相色谱可准确快速检测梅州客家娘酒中的5-羟甲基糠醛含量,陈彦和等[21]通过高效液相色谱建立了益肾保健酒中9种有效成分的检测方法,可对保健酒中5-羟甲基糠醛、阿魏酸、肉桂醛等成分进行准确定量。此外,李先芝等[22]利用高效液相色谱建立了追风八珍酒中的7种有效成分的检测方法,可准确定量追风八珍酒中原儿茶酸、绿原酸、巴利森苷B等成分。张龙等[23]建立了高效液相色谱同时测定天龙泉-陶藏酒中10种酚类物质和2种三萜类物质的方法。目前,针对复方保健酒中有效成分的检测方法还未见报道。
本研究采用高效液相色谱(HPLC)同时测定复方保健酒中8种有效成分(5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II)的含量,并考察了酒样中8种有效成分在温度、光照等不同贮存条件下的稳定性,以期建立高效检测复方保健酒产品中有效成分的方法,为复方保健酒的贮藏提供参考依据。
1 材料与方法
1.1 材料与试剂
复方保健酒:劲牌有限公司;5-羟甲基糠醛(批号:111626-201711,含量97.3%)、腺苷(批号:110879-201703,含量99.7%)、虫草素(批号:110879-201703,含量99.4%)、苦番红花素(批号:112056-202102,含量99.9%)、芦丁(批号:100080-201610,含量91.1%)、西红花苷I(批号:111588-201704,含量88.4%)、西红花苷II(批号:111589-201705,含量92.2%):中国食品药品检定研究院;N6-(2-羟乙基)腺苷(批号:C10092454,含量98%):上海麦克林生化科技股份有限公司;乙腈、乙酸(均为色谱级):美国赛默飞公司;甲醇(分析纯):国药集团化学试剂有限公司。
1.2 仪器与设备
UltiMate 3000高效液相色谱仪:美国赛默飞公司;SK1200H数控超声波清洗仪:上海科导超声仪器有限公司;SQP电子分析天平:德国赛多利斯公司;PURELAB-超纯水仪:英国埃尔格电子科技有限公司;HX-T-500D2低温恒温箱:东莞市昊昕仪器设备有限公司;DH209D电热恒温培养箱:天津市泰斯特仪器有限公司;MKF720高低温交变气候箱:德国BINDER公司。
1.3 方法
1.3.1 标准溶液配制
精密称取5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II标准品适量,加入50%甲醇溶解,制成5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II质量浓度分别为27 μg/mL、35 μg/mL、51 μg/mL、51 μg/mL、53 μg/mL、11 μg/mL、11 μg/mL、4 μg/mL的混合标准品溶液。
1.3.2 供试品溶液配制
精密量取样品5 mL至10 mL容量瓶中,加水定容至刻度线,摇匀,用0.22 μm针头过滤器过滤,即得供试品溶液。
1.3.3 色谱条件
Agilent SB-Aq C18色谱柱(4.6 mm×250 mm,5 μm);柱温:30 ℃;0~68 min检测波长260 nm,68~80 min检测波长440 nm;进样量10 μL;流动相A:乙腈;流动相B:0.1%乙酸溶液,梯度洗脱程序:0~10 min,2%A~2%A,10~15 min,2%~4%A;15~25 min,4%~7%A;25~35 min,7%~10%A;35~40 min,10%~10%A;40~60 min,10%~18%;60~80 min,18%~35%A;流速1.0 mL/min。
1.3.4 定性定量方法
根据5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II标准品在色谱图上的保留时间对复方保健酒样品中的8种成分进行定性分析,并采用外标法对各物质进行定量分析。计算公式如下:
式中:cx为样品质量浓度,mg/L;cr为对照品质量浓度,mg/L;Ax为样品峰面积;Ar为对照品峰面积。
1.3.5 方法学考察
(1)标准曲线回归方程、线性范围、检出限和定量限
将上述混合标准品溶液稀释成5个不同浓度,采用1.3.3色谱条件进行测定,以物质的质量浓度(X)为横坐标,色谱峰面积(Y)为纵坐标绘制标准曲线,建立标准曲线回归方程,得出线性关系及范围。将8种成分对照品溶液进行适当稀释后制得一系列不同浓度的溶液混合溶液,以3倍信噪比(S/N)对应的质量浓度作为检出限(limit of detection,LOD),10倍信噪比对应的质量浓度作为定量限(limit of quantitation,LOQ)。
(2)精密度试验
取同一批次复方保健酒样品,按照1.3.2的方法制备供试品溶液,在1.3.3色谱条件下连续进样6次,记录对应的物质含量,并计算精密度试验结果的相对标准偏差(relative standard deviation,RSD)。
(3)稳定性试验
取同一供试品溶液,采用1.3.3色谱条件进行测定,分别于0 h、3 h、8 h、17 h、26 h、41 h进样,记录物质含量,并计算稳定性试验结果的RSD。
(4)重复性试验
取同一批次复方保健酒样品,按照1.3.2的方法制备供试品溶液6份,在1.3.3色谱条件下进样,记录物质含量,并计算测定重复性试验结果的RSD。
(5)加标回收率试验
精密量取已知含量的同一复方保健酒样品2.5 mL至10 mL容量瓶中,分别按酒样品中各成分含量的低、中、高三个水平加入标准品适量,加水定容。采用1.3.3色谱条件进行测定,计算各成分加标回收率。
1.3.6 复方保健酒稳定性试验
将复方保健酒样品分成6份,分别于不同条件(-5 ℃、室温、恒温37 ℃、高温50 ℃、光照、避光)贮存90 d,其中光照条件为设置总照度为1.2×106 Lux·hr,分别于0、30 d、60 d、90 d取样分析,考察其稳定性。
1.3.7 数据分析
利用软件Chromeleon 7查看色谱图,采用Origin2022软件绘图,采用Excel 2016软件处理数据。
2 结果与分析
2.1 8种有效成分定性分析结果
混合标准品及酒样的高效液相色谱图见图1。由图1A可知,该方法基线平稳,8种有效成分可以很好地分离,峰形对称完整,可在80 min内完成检测。由图1B可知,酒样中8种有效成分在标准品相同的保留时间下均有色谱峰出现,表明复方保健酒中含有5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II这8种有效成分。
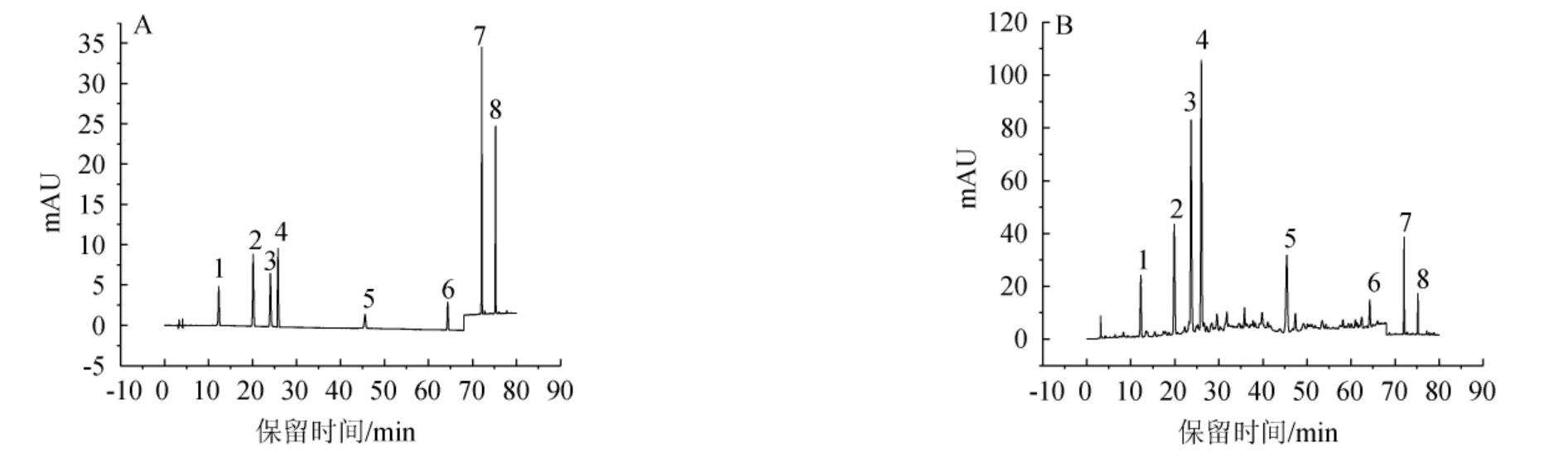
图1 混合标准品(A)及酒样(B)的高效液相色谱图
Fig.1 High performance liquid chromatogram of mixed standard (A) and wine sample (B)
1:5-羟甲基糠醛;2:腺苷;3:虫草素;4:N6-(2-羟乙基)腺苷;5:苦番红花素;6:芦丁;7:西红花苷I;8:西红花苷II。
2.2 方法学考察
2.2.1 线性范围、回归方程、检测限和定量限
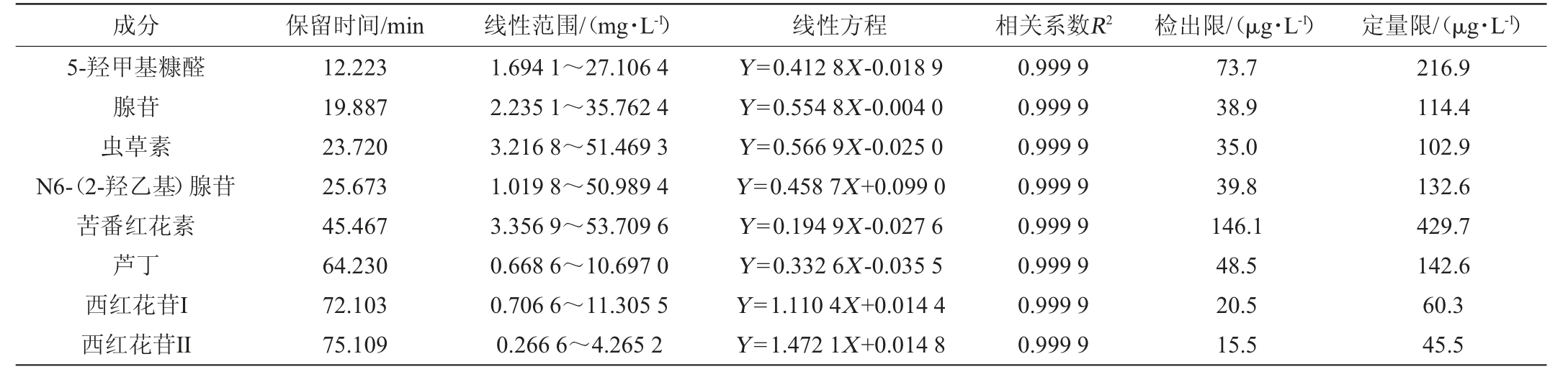
8种有效成分标准曲线回归方程、线性范围、相关系数、检出限及定量限见表1。由表1可知,8种目标化合物在质量浓度0.266 6~51.469 3 mg/L线性范围内与峰面积成良好的线性关系,相关系数R2均>0.999,检出限(LOD)为15.5~146.1 μg/L,定量限(LOQ)为45.5~429.7 μg/L,满足常规检测要求。
表1 8种有效成分的标准曲线回归方程、线性范围、相关系数、检出限及定量限
Table 1 Standard curve regression equation, linear range, correlation coefficient, limits of detection, and limits of quantitation of 8 effective components
成分 保留时间/min 线性范围/(mg·L-1)线性方程 相关系数R2 检出限/(μg·L-1)定量限/(μg·L-1)5-羟甲基糠醛腺苷虫草素N6-(2-羟乙基)腺苷苦番红花素芦丁西红花苷I西红花苷II 12.223 19.887 23.720 25.673 45.467 64.230 72.103 75.109 1.694 1~27.106 4 2.235 1~35.762 4 3.216 8~51.469 3 1.019 8~50.989 4 3.356 9~53.709 6 0.668 6~10.697 0 0.706 6~11.305 5 0.266 6~4.265 2 Y=0.412 8X-0.018 9 Y=0.554 8X-0.004 0 Y=0.566 9X-0.025 0 Y=0.458 7X+0.099 0 Y=0.194 9X-0.027 6 Y=0.332 6X-0.035 5 Y=1.110 4X+0.014 4 Y=1.472 1X+0.014 8 0.999 9 0.999 9 0.999 9 0.999 9 0.999 9 0.999 9 0.999 9 0.999 9 73.7 38.9 35.0 39.8 146.1 48.5 20.5 15.5 216.9 114.4 102.9 132.6 429.7 142.6 60.3 45.5
2.2.2 精密度试验
8种有效成分的精密度试验结果见表2。由表2可知,测得8种有效成分的精密度试验结果相对标准偏差(relative standard deviation,RSD)分别为0.59%、0.24%、0.38%、0.11%、0.36%、0.63%、0.57%、0.74%,RSD均<2%,表明该方法精密度良好,满足常规检测要求。
表2 8种有效成分的精密度试验结果
Table 2 Results of precision tests of 8 effective components

含量/(mg·L-1)成分 RSD/%5-羟甲基糠醛 11.277 8 11.353 4 11.354 4 11.224 6 11.217 6 11.212 6 0.59 1 2 3 4 5 6
续表
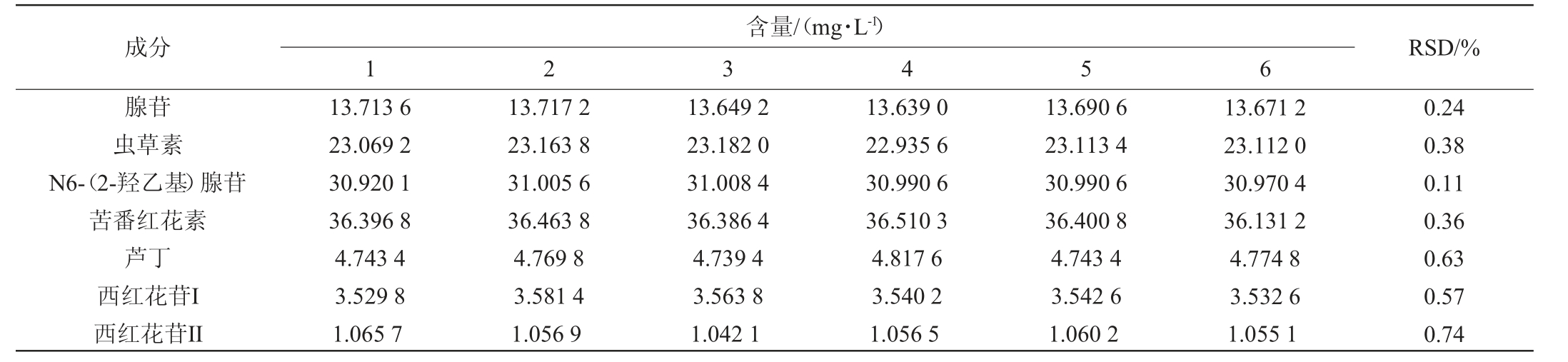
含量/(mg·L-1)成分 RSD/%腺苷虫草素N6-(2-羟乙基)腺苷苦番红花素芦丁西红花苷I西红花苷II 1 2 3 4 5 6 13.713 6 23.069 2 30.920 1 36.396 8 4.743 4 3.529 8 1.065 7 13.717 2 23.163 8 31.005 6 36.463 8 4.769 8 3.581 4 1.056 9 13.649 2 23.182 0 31.008 4 36.386 4 4.739 4 3.563 8 1.042 1 13.639 0 22.935 6 30.990 6 36.510 3 4.817 6 3.540 2 1.056 5 13.690 6 23.113 4 30.990 6 36.400 8 4.743 4 3.542 6 1.060 2 13.671 2 23.112 0 30.970 4 36.131 2 4.774 8 3.532 6 1.055 1 0.24 0.38 0.11 0.36 0.63 0.57 0.74
2.2.3 稳定性试验
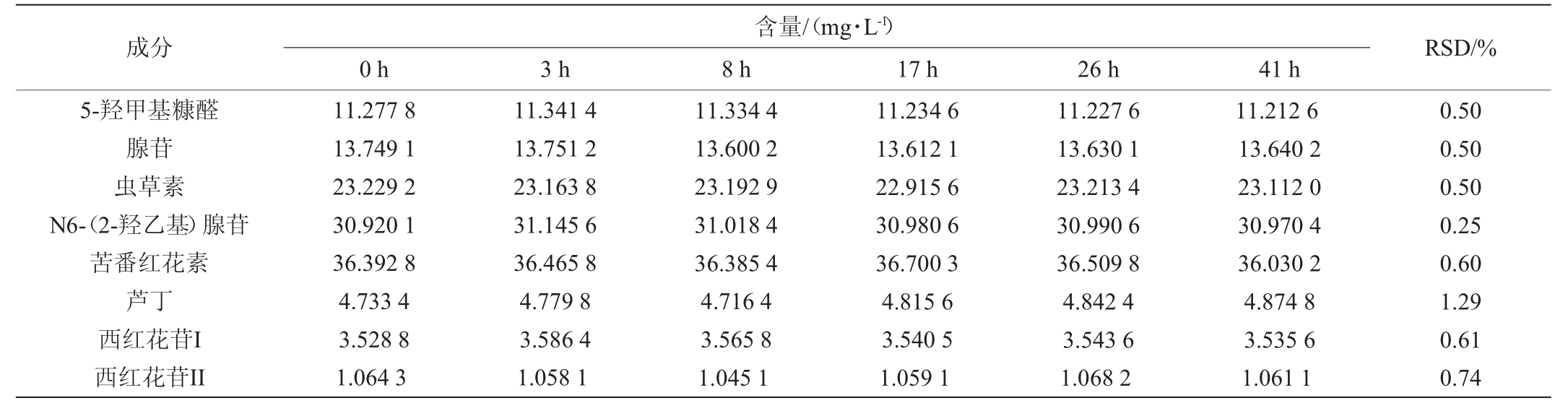
8种有效成分的稳定性试验结果见表3。由表3可知,测得8种有效成分5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II含量的RSD值分别为0.50%、0.50%、0.50%、0.25%、0.60%、1.29%、0.61%、0.74%,RSD均<2%,表明供试品溶液中各成分在室温条件下放置41 h内稳定性良好。
表3 8种有效成分的稳定性试验结果
Table 3 Results of stability tests of 8 effective components
成分 RSD/%含量/(mg·L-1)0 h 3 h 8 h 17 h 26 h 41 h 5-羟甲基糠醛腺苷虫草素N6-(2-羟乙基)腺苷苦番红花素芦丁西红花苷I西红花苷II 11.277 8 13.749 1 23.229 2 30.920 1 36.392 8 4.733 4 3.528 8 1.064 3 11.341 4 13.751 2 23.163 8 31.145 6 36.465 8 4.779 8 3.586 4 1.058 1 11.334 4 13.600 2 23.192 9 31.018 4 36.385 4 4.716 4 3.565 8 1.045 1 11.234 6 13.612 1 22.915 6 30.980 6 36.700 3 4.815 6 3.540 5 1.059 1 11.227 6 13.630 1 23.213 4 30.990 6 36.509 8 4.842 4 3.543 6 1.068 2 11.212 6 13.640 2 23.112 0 30.970 4 36.030 2 4.874 8 3.535 6 1.061 1 0.50 0.50 0.50 0.25 0.60 1.29 0.61 0.74
2.2.4 重复性试验
8种有效成分的重复性试验结果见表4。由表4可知,5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II含量分别为11.276 7 mg/L、13.658 1 mg/L、23.129 3 mg/L、30.979 3 mg/L、36.143 1 mg/L、4.791 6 mg/L、3.485 4 mg/L、1.052 0 mg/L,RSD值分别为1.72%、1.47%、0.92%、0.12%、0.89%、1.80%、1.77%、1.84%,RSD均<2%,表明该方法重复性良好,满足8种有效成分的分析要求。
表4 8种有效成分的重复性试验结果
Table 4 Results of repeatability tests of 8 effective components
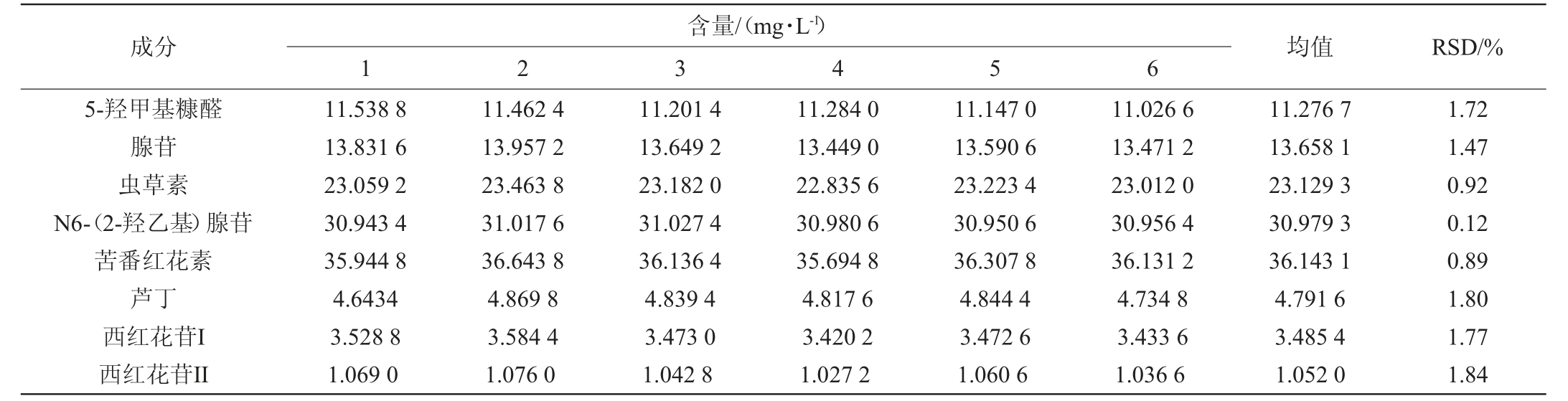
成分5-羟甲基糠醛腺苷虫草素N6-(2-羟乙基)腺苷苦番红花素芦丁西红花苷I西红花苷II含量/(mg·L-1)1 2 3 4 5 6均值 RSD/%11.538 8 13.831 6 23.059 2 30.943 4 35.944 8 4.6434 3.528 8 1.069 0 11.462 4 13.957 2 23.463 8 31.017 6 36.643 8 4.869 8 3.584 4 1.076 0 11.201 4 13.649 2 23.182 0 31.027 4 36.136 4 4.839 4 3.473 0 1.042 8 11.284 0 13.449 0 22.835 6 30.980 6 35.694 8 4.817 6 3.420 2 1.027 2 11.147 0 13.590 6 23.223 4 30.950 6 36.307 8 4.844 4 3.472 6 1.060 6 11.026 6 13.471 2 23.012 0 30.956 4 36.131 2 4.734 8 3.433 6 1.036 6 11.276 7 13.658 1 23.129 3 30.979 3 36.143 1 4.791 6 3.485 4 1.052 0 1.72 1.47 0.92 0.12 0.89 1.80 1.77 1.84
2.2.5 加标回收试验
8种成分的加标回收试验结果见表5。由表5可知,8种有效成分5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II平均加标回收率分别为99.23%、99.03%、98.11%、98.68%、99.00%、98.76%、98.03%、96.15%;加标回收率的RSD值分别为2.04%、2.28%、3.42%、0.83%、1.15%、1.89%、0.44%、4.00%,RSD均<5%,表明该方法准确度高,满足8种有效成分的分析要求。
表5 8种有效成分加标回收率试验结果
Table 5 Results of spiked recovery rates tests of 8 effective components
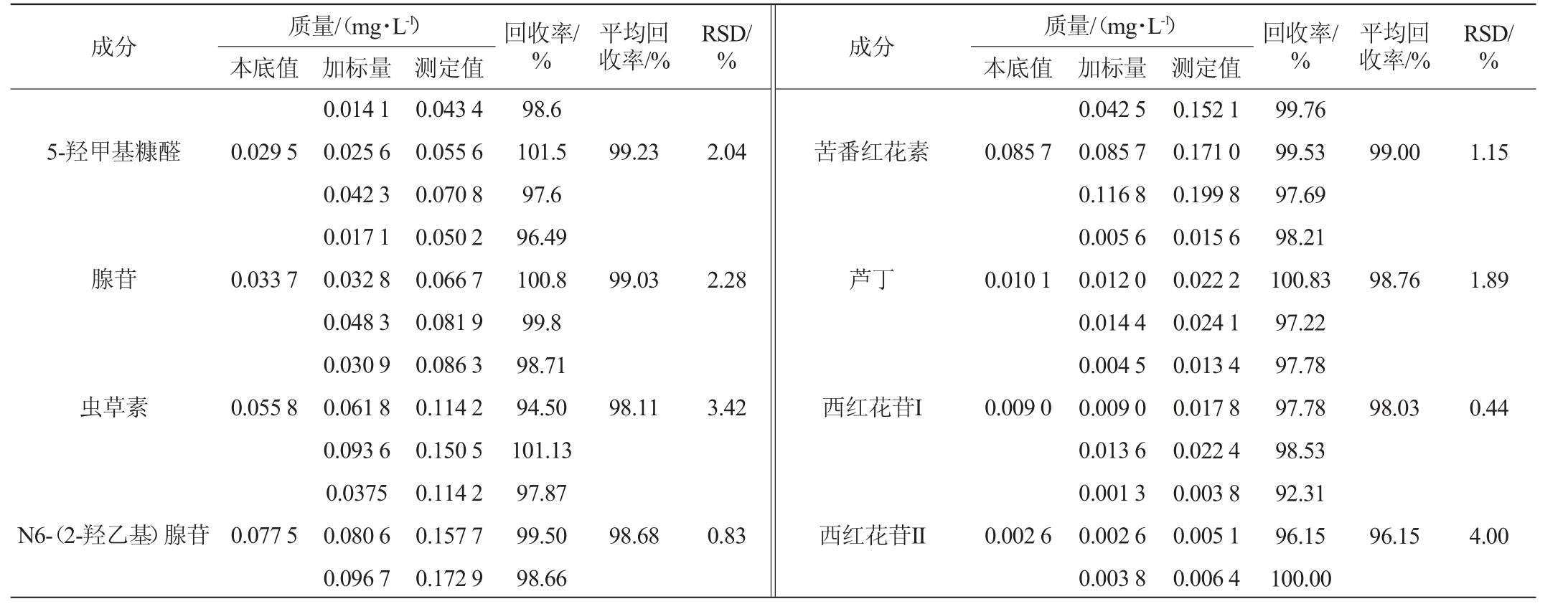
成分 回收率/%质量/(mg·L-1)本底值 加标量 测定值平均回收率/%RSD/%成分 回收率/%质量/(mg·L-1)本底值 加标量 测定值平均回收率/%RSD/%5-羟甲基糠醛0.029 5 0.014 1 0.025 6 0.042 3 0.017 1 0.032 8 0.048 3 0.030 9 0.061 8 0.093 6 0.0375 0.080 6 0.096 7 0.043 4 0.055 6 0.070 8 0.050 2 0.066 7 0.081 9 0.086 3 0.114 2 0.150 5 0.114 2 0.157 7 0.172 9 98.6 101.5 97.6 96.49 100.8 99.8 98.71 94.50 101.13 97.87 99.50 98.66 99.23 2.04苦番红花素腺苷0.033 7 99.03 2.28 0.085 7 0.042 5 0.085 7 0.116 8 0.005 6 0.012 0 0.014 4 0.004 5 0.009 0 0.013 6 0.001 3 0.002 6 0.003 8 0.152 1 0.171 0 0.199 8 0.015 6 0.022 2 0.024 1 0.013 4 0.017 8 0.022 4 0.003 8 0.005 1 0.006 4 99.76 99.53 97.69 98.21 100.83 97.22 97.78 97.78 98.53 92.31 96.15 100.00 99.00 1.15芦丁虫草素0.055 8 98.11 3.42 0.010 1 98.76 1.89西红花苷I N6-(2-羟乙基)腺苷0.077 5 98.68 0.83 0.009 0 98.03 0.44西红花苷II 0.002 6 96.15 4.00
2.3 样品的稳定性分析
样品稳定性试验结果见表6。由表6可知,腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素成分在不同环境条件下贮存时,平均含量分别为18.655 3 mg/L、15.299 8 mg/L、18.473 3 mg/L、32.106 7 mg/L,含量并无明显差异,说明这4种有效成分具有较好的稳定性。在37 ℃、50 ℃条件下,随着贮存时间的延长,5-羟甲基糠醛含量逐渐增加,尤其是在高温50 ℃条件下,上升趋势明显,由13.727 6 mg/L上升至42.350 6 mg/L,含量增加2倍,但在光照条件下无明显变化,说明5-羟甲基糠醛对温度较敏感[24]。芦丁在上述条件中均存在下降趋势,而在-5 ℃、室温及避光环境下,下降较为缓慢,然而在37 ℃、50 ℃及光照环境下贮存90 d后含量降低了近50%,说明芦丁对光和热都较敏感。西红花苷I、西红花苷II呈现出相同的变化趋势,在室温条件下存放时,随着贮存时间的延长含量逐渐降低,当贮存60 d后含量趋于稳定,但在-5 ℃条件下贮存90 d时含量变化均不明显;在避光条件下贮存90 d后含量均下降35%;然而在37 ℃及50 ℃环境下,随着贮存时间的延长,含量变化极为显著,特别是50 ℃条件下,两者含量均降低90%以上,且在光照环境下随着光照能力的增加,西红花苷I、西红花苷II含量均降低了58%以上,说明西红花苷对热和光及其敏感,这一结论与蔡仕宁等[25]研究结果一致。
表6 复方保健酒样品稳定性试验结果
Table 6 Results of stability tests of compound health wine samples mg/L

贮存条件 贮存时间/d 5-羟甲基糠醛 腺苷 虫草素 N6-(2-羟乙基)腺苷 苦番红花素 芦丁 西红花苷I 西红花苷II 0室温避光-5 ℃37 ℃30 60 90 0 30 60 90 0 30 60 90 0 30 60 90 13.727 6 13.568 0 13.597 4 13.474 6 13.727 6 13.920 2 13.905 6 14.056 2 13.727 6 13.620 8 13.569 8 13.562 2 13.727 6 15.713 4 17.015 2 18.366 0 18.291 0 18.844 2 19.098 6 18.777 4 18.291 0 19.090 2 19.146 4 18.696 2 18.291 0 18.571 4 18.276 0 19.404 4 18.291 0 18.558 8 18.506 0 18.108 6 15.156 0 14.674 6 15.676 4 15.567 8 15.156 0 14.994 2 15.563 6 15.067 8 15.156 0 15.059 4 15.515 4 15.277 8 15.156 0 14.965 6 15.609 8 15.080 6 18.864 6 18.737 2 18.162 0 18.261 2 18.864 6 18.785 8 18.120 4 18.502 2 18.864 6 18.786 0 18.256 0 18.682 4 18.864 6 18.451 4 17.885 2 18.436 0 32.748 0 32.456 6 32.190 0 32.076 6 32.748 0 32.839 6 32.268 4 32.211 4 32.748 0 32.773 4 32.511 2 32.753 4 32.748 0 31.886 0 31.635 4 31.275 6 6.071 2 4.952 8 4.473 2 4.526 4 6.071 2 5.406 6 4.882 2 4.476 2 6.071 2 5.634 6 5.834 4 5.430 8 6.071 2 4.432 8 3.851 6 3.774 4 18.945 7 13.762 8 11.485 8 11.846 0 18.945 7 16.579 6 14.292 4 12.277 6 18.945 7 18.676 5 17.720 8 17.466 0 18.945 7 11.431 6 9.165 8 6.266 4 8.120 9 5.818 6 4.941 4 5.031 2 8.120 9 7.048 8 6.129 8 5.222 0 8.120 9 8.030 5 7.703 4 7.592 0 8.120 9 4.875 7 3.816 8 2.561 0
续表
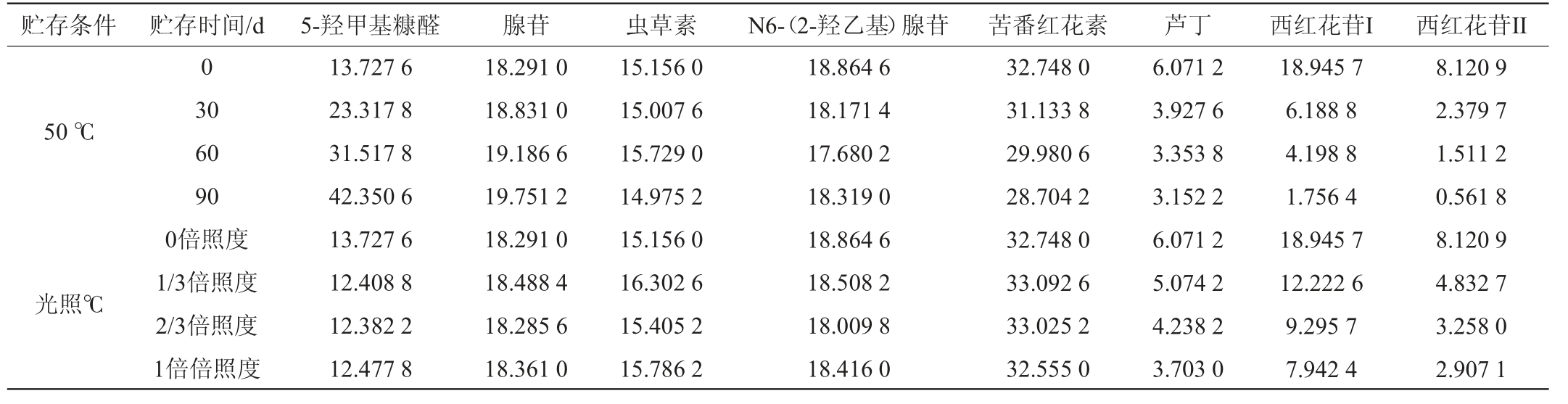
贮存条件 贮存时间/d 5-羟甲基糠醛 腺苷 虫草素 N6-(2-羟乙基)腺苷 苦番红花素 芦丁 西红花苷I 西红花苷II 0 50 ℃光照℃30 60 90 0倍照度1/3倍照度2/3倍照度1倍倍照度13.727 6 23.317 8 31.517 8 42.350 6 13.727 6 12.408 8 12.382 2 12.477 8 18.291 0 18.831 0 19.186 6 19.751 2 18.291 0 18.488 4 18.285 6 18.361 0 15.156 0 15.007 6 15.729 0 14.975 2 15.156 0 16.302 6 15.405 2 15.786 2 18.864 6 18.171 4 17.680 2 18.319 0 18.864 6 18.508 2 18.009 8 18.416 0 32.748 0 31.133 8 29.980 6 28.704 2 32.748 0 33.092 6 33.025 2 32.555 0 6.071 2 3.927 6 3.353 8 3.152 2 6.071 2 5.074 2 4.238 2 3.703 0 18.945 7 6.188 8 4.198 8 1.756 4 18.945 7 12.222 6 9.295 7 7.942 4 8.120 9 2.379 7 1.511 2 0.561 8 8.120 9 4.832 7 3.258 0 2.907 1
3 结论
本研究采用高效液相色谱建立了测定复方保健酒中5-羟甲基糠醛、腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素、芦丁、西红花苷I、西红花苷II的含量方法,最佳色谱条件为:采用Agilent SB-Aq C18色谱柱(4.6 mm×250 mm,5 μm),以乙腈-0.1%乙酸水溶液为流动相,流速1.0 mL/min,检测波长260 nm/440 nm,柱温30 ℃,进样量10 μL。该方法操作简便,精密度及重复性良好,准确度高,可为后期复方保健酒生产过程中的质量监控及评价提供参考依据。稳定性试验结果表明,在不同的贮存条件下贮存90 d,腺苷、虫草素、N6-(2-羟乙基)腺苷、苦番红花素含量稳定性较好;5-羟甲基糠醛对温度较敏感;芦丁、西红花苷I、西红花苷II对光和热均极其敏感。因此,复方保健酒在后期贮存过程中要避免光照、高温环境,可采取避光的材料存放酒体。
[1]刘万明.中国酒文化结构失调及优化[J].四川理工学院学报(社会科学版),2017,32(1):26-36.
[2]郑福平,马雅杰,侯敏,等.世界6大蒸馏酒香气成分研究概况与前景展望[J].食品科学技术学报,2017,35(2):1-12.
[3]秦月,严沁,张玲,等.中国保健酒的历史发展及研究进展[J].中国酿造,2021,40(9):7-11.
[4]国家药典委员会.中国药典一部[S].北京:中药医药科技出版社,2020:139.
[5]胡杨,李先芝,毛琼丽,等.高效液相色谱法测定人参保健酒中11种人参皂苷含量[J].中国酿造,2024,43(3):229-233.
[6]李萌,章从恩,章前,等.基于谱-效相关分析的西红花抗抑郁药效成分的研究[J].中国医院用药评价与分析,2022,22(9):1098-1101.
[7]钟晴柔,尤雅,朱琳,等.西红花及其活性成分对肝脏疾病作用及其机制的研究进展[J].中草药,2021,52(14):4386-4397.
[8]卢杏,杨军政,张学平,等.西红花提取物对病毒性心肌炎小鼠的保护作用[J].中华医院感染学杂志,2021,31(10):1441-1445.
[9]ABDEL-RAHMAN R F,EL AWDAN S A,HEGAZY R R,et al.Neuroprotective effect of Crocus sativus against cerebral ischemia in rats[J].Metab Brain Dis,2020,35:427-439.
[10]GHORBANZADEH V,MOHAMMADI M,DARIUSHNEJAD H,et al.Effects of crocin and voluntary exercise, alone or combined, on heart VEGF-A and HOMA-IR of HFD/STZ induced type 2diabetic rats[J].J Endocrinol Invest,2016,39:1179-1186.
[11]秦令祥,丁昱婵,赵俊芳,等.蛹虫草多糖提取工艺优化及其抗菌、抗氧化活性[J].食品研究与开发,2023,44(11):159-165.
[12]苗月,任桂红,甄东,等.蛹虫草多糖调节小鼠巨噬细胞RAW264.7免疫活性的分子机制[J].食品科学,2019,40(9):188-194.
[13]张虎成,邓丽娜,杨国伟,等.从蛹虫草小麦培养基残渣分离虫草素及提取物对肝癌细胞的抑制效果[J].菌物学报,2022,41(10):1680-1693.
[14]REIS F S,BARROS L,CALHELHA R C,et al.The methan-olic extract of Cordyceps militaris(L.)link fruiting body shows antioxidant,antibacterial,antifungal and antihuman tumor cell lines properties[J].Food Chem Toxicol,2013,62:91-98.
[15]KWON H K,SONG M J,LEE H J,et al. Pediococcus pentosaceus-fermented Cordyceps militaris inhibits inflammatory reactions and alleviates contact dermatitis[J].Int J Mol Sci,2018,19(11):3504.
[16]CHOI S J,RYU E,LEE S,et al.Adenosine induces EBV lytic reactivation through ADORA1 in EBV-associated gastric carcinoma[J].Int J Mol Sci,2019,20(6):1286.
[17]谭梅娥,何承辉,帕依曼·亥米提,等.高效液相色谱法同时测定维药香青兰有效部位中10个化学成分的含量[J].医药导报,2024,43(4):567-571.
[18]王米香,姬诚,朱景平,等.基于高效液相色谱法的参术儿康糖浆多成分定量研究[J].中药材,2024(3):681-684.
[19]尚朝利,白泽方,樊轻亚.HPLC法同时测定复方双花片中10个成分的含量[J].药物分析杂志,2024,44(2):242-248.
[20]彭志强,房丹,杨瑞环,等.高效液相色谱法检测梅州客家娘酒中5-羟甲基糠醛[J].中国酿造,2023,42(6):245-250.
[21]陈彦和,胡杨,李先芝,等.高效液相色谱法同时测定益肾保健酒中9种有效成分[J].化学分析计量,2023,32(8):80-84.
[22]李先芝,胡杨,杨峰,等.HPLC法同时测定追风八珍酒中7种有效成分[J].中国酿造,2022,41(9):229-233.
[23]张龙,郝俊光,杨金海,等.高效液相色谱法同时测定天龙泉-陶藏酒中12种活性成分[J].中国酿造,2023,42(2):221-227.
[24]ZHANG J H,LI Y Z,LV M X,et al.Determination of 5-hydroxymethylfurfural (5-HMF) in milk products by surface enhanced Raman spectroscopy and its simulation analysis[J].Spectrochim Acta A,2022,279:121393.
[25]蔡仕宁,陈阳.不同结构西红花苷稳定性的研究[J].食品科技,2012,37(8):212-215.