中国白酒是世界六大蒸馏酒之一[1],共有十二大香型,其中浓香型白酒具有很高的产量和消费市场占有率[2]。大曲作为约70%中国白酒酿造所应用的糖化发酵剂和生香剂,含有丰富的微生物、酶类和呈香呈味物质,对白酒香型起决定作用[3]。同时,大曲作为白酒酿造原料的一部分,其品质特性直接影响原酒的产量和质量,故有“曲为酒之骨”之说[4]。大曲多以小麦为主料,经过粗粉碎、加水搅拌、压块成型、入房发酵、出房储藏成熟等工艺生产而成[5]。根据最高发酵温度,大曲分为三种,即高温大曲(60~70 ℃)、中温大曲(50~60 ℃)和低温大曲(40~50 ℃)[6],分别用于不同香型白酒的生产。其中,中温大曲根据最高发酵温度又分为中高温大曲(55~62 ℃)和中温大曲(50~55 ℃)两种,常用于浓香型白酒的生产[7]。
真菌是中温大曲微生物的重要类群,主要包括霉菌和酵母菌,约占白酒酿造微生物总数的61%~80%,其种群组成与原酒的产量和香气密切相关[8]。霉菌和酵母菌多数为嗜温菌,生长温度为20~45 ℃[3]。然而,大曲生产工艺及发酵温度不同,导致不同类型大曲的真菌菌群组成也不同。相比高温大曲和低温大曲,中温大曲有中等数量的真菌和适温嗜热相结合的优势菌群[9]。有研究者对中国不同地域的32个三种类型的大曲真菌菌群进行分析,共分离鉴定出420株真菌,发现所有大曲样本中最普遍存在的真菌是酵母菌,优势真菌种为酿酒酵母菌(Saccharomyces cerevisiae)、异常威克汉姆酵母(Wickerhamomyces anomalus)和扣囊复膜酵母(Saccharomycopsis fibuligera)。目前,中温大曲普遍存在的优势真菌种主要有Saccharomyces cerevisiae、Wickerhamomyces anomalus、Saccharomycopsis fibuligera、库德毕赤酵母(Pichia kudriavzevii)、异常毕赤酵母(Pichia anomala)、总状毛霉(Mucor racemosus)[8,10];主要优势真菌属有毕赤氏酵母菌(Pichia)、假丝酵母菌(Candida)、酵母属(Saccharomyces)、复膜孢酵母属(Saccharomycopsis)、伊萨酵母属(Issatchenkia)、嗜热真菌属(Thermomyces)、散囊菌(Eurotium)、耐热囊菌属(Thermoascus)、曲霉(Aspergillus)、根霉(Rhizopus)、根毛霉(Rhizomucor)、链格孢属(Alternaria)[2,11-14],且多数优势霉菌和酵母为大曲功能菌或核心功能菌。有研究发现,真菌是中温大曲微生物菌群中最丰富和活跃的功能菌,且糖酵解途径中所有上调基因主要来自酵母目(Saccharomycetales)和毛霉菌目(Mucorales)[15]。大曲中的酵母菌是一种多功能菌,具有产酒、糖化、提高酯化度、贡献风味物或香气前体及高效利用原料等功能[10,15-17]。霉菌多属于丝状真菌,其功能主要表现为代谢液化酶、糖化酶、蛋白酶、酯化酶、纤维素酶等多种酶类[18-19],这些酶类均有助于大曲原料降解、风味物质及其前体物形成[20-22]。此外,霉菌与大曲细菌互作,可以促进大曲香气物质的产生[23]。然而,由于中温大曲的生产是开放式网络自然界环境微生物的一种自发固态发酵过程,其微生物群落组成受到多种因素的影响,原料便是其中之一[24]。
小麦作为中温大曲生产的主要原料,不仅是微生物生长的载体,同时也为微生物的生长代谢提供丰富的营养物质。然而,不同品种和种植区的小麦组成和品质特征存在差异,这些差异会影响微生物富集和代谢,进而影响大曲的理化性质。黄瑜等[25]模拟高温大曲固态发酵工艺,研究了来自南方和北方21个小麦样品的微生物组成及其模拟大曲的微生物组成和风味代谢物,发现南方和北方小麦模拟大曲的微生物组成不同,而相同或相邻地域小麦制备的大曲微生物组成却相似,且小麦微生物组成相似度越高,大曲风味组成越相似。该研究表明,不同小麦原料会影响大曲微生物的组成及其代谢。因此,适宜的小麦品种和特性不仅可以提高微生物生长的营养成分,还可以促进大曲风味物质的代谢和合成[26]。然而,目前大曲的生产主要依赖当地种植品种的混合小麦,很少应用特殊的单品种小麦。尽管前人对制曲小麦与大曲的理化指标也做了相关的研究,但该研究也主要集中在南方限制的几个制曲小麦品种或研究水平停留在实验室规模上,而酿酒小麦品种对生产试验大曲微生物组成及其代谢的影响至今仍然尚不明晰。因此,本研究以酒厂当地种植的多品种混合小麦(又称混合花麦)为对照,选择河南4个酿酒小麦品种进行生产制曲试验,采用高通量测序技术分析比较5种小麦中温大曲的真菌群落组成,并分析比较其感官品质和理化特性,探索小麦主要品质指标与大曲优势真菌的相关性,以期为制曲小麦对大曲优势菌群的影响提供新的见解,并为适宜的制曲小麦品种的选择及改善或稳定大曲品质提供可靠的理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
圣麦15、郑麦369、郑麦113、尚农8号(编号分别为B、C、D、E):由河南小麦育种专家根据小麦特性为酒厂制曲推荐,且均由河南商丘农科所提供;混合花麦(编号为A)、5种小麦中温大曲:河南张弓老酒酒业有限公司。
1.1.2 试剂
无水葡萄糖:北京索莱宝科技有限公司;磷酸二氢钠、磷酸氢二钠、冰乙酸、己酸:天津市科密欧化学试剂有限公司;可溶性淀粉、氢氧化钠、酒石酸钾钠、无水乙酸钠:国药集团化学试剂有限公司;引物ITS1F和ITS2R、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphates,dNTPs)混合液:上海美吉生物医药科技有限公司;琼脂糖:西班牙biowest公司;FastPfu脱氧核糖核酸(deoxyribonucleic acid,DNA)聚合酶、15Kmarker:北京全式金生物技术公司;E.Z.N.A.R土壤DNA提取试剂盒:美国Omega Bio-tek公司;AxyPrep DNA胶回收纯化试剂盒、建库试剂盒:美国Axygen Biosciences公司。本研究所用试剂均为分析纯或生化试剂。
1.2 仪器与设备
Kjeltec8400全自动凯氏定氮仪、NIRS DA 1650近红外谷物分析仪:丹麦FOSS公司;SW-CJ-2F型超净工作台:苏州净化设备有限公司;LDZX-50FBS型高压蒸汽灭菌锅:上海申安医疗器械厂;MJX-250B-Z型恒温培养箱:上海博迅实业医疗设备厂;MQD-B3R型恒温振荡培养箱:上海旻泉仪器有限公司;101-2AS型电热鼓风干燥箱:上海科润仪器设备有限公司;GeneAmp 9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司;5430R小型离心机:德国Eppendorf公司;NanoDrop2000超微量分光光度计:美国赛默飞世尔科技公司;Illumina Miseq PE300测序平台:美国Illumina公司。
1.3 试验方法
1.3.1 样本处理
采用麦堆五点取样法于2021年9月开始制曲时采集小麦样本,样本置于-20 ℃保存,用于测定主要品质指标。
2022年1月采集成熟3个月的5种小麦(A、B、C、D、E)中温大曲,分别从中温大曲曲堆的上、中、下各层任意抽取3块大曲,磨碎后充分混合为一个样本,编号分别为AMD、BMD、CMD、DMD、EMD,每个样本取2份,装入无菌袋密封,其中一份置于-20 ℃保存,用于大曲理化指标测定;另一份置于-80 ℃保存,用于高通量测序。每个样本进行3次重复。
1.3.2 小麦主要品质特性指标的测定
粉质率:采用目测法测定[24];粗淀粉含量:采用近红外光谱法测定[27];粗蛋白含量:按照GB/T 6432—2018《饲料中粗蛋白的测定凯氏定氮法》进行测定;湿面筋含量:按照GB/T 5506.2—2008《小麦和小麦粉面筋含量第2部分:仪器法测定湿面筋》测定。
1.3.3 大曲感官质量评定
感官质量评定组由生产经验丰富的制曲工人和白酒资深感官评定专家共7人组成。中温大曲感官评定要求参照国家轻工行业标准QB/T 4259—2011《浓香大曲》和地方标准DB37/T 1231—2009《大曲通用技术条件》进行制定,具体评分标准见表1。
表1 小麦中温大曲感官评定标准
Table 1 Sensory evaluation standards for medium-temperature Daqu made with wheat

评分标准二级大曲 三级大曲外观(20分)项目 一级大曲灰白色或微黄色,穿衣基本整齐,允许有裂口和少量的杂菌斑。(≤10分)灰白色或有红、黄菌丝,断面基本整齐,允许有少许生心、窝水、杂菌斑、水圈现象。(≤25分)曲香较淡,允许有轻微异味。(≤20分)皮张(10分)综合得分/分断面(40分)香气(30分)灰白色,穿衣均匀整齐,无裂口,无杂菌斑。(20~15分)灰白色或有红、黄菌丝,断面整齐,菌丝生长健壮、泡气,无生心、窝水现象。(40~35分)曲香浓郁,纯正、无异味。(30~25分)灰白色,穿衣较整齐,无裂口,无杂菌斑。(15~10分)灰白色或有红、黄菌丝,断面较整齐,菌丝生长健壮、泡气,无生心、窝水现象,允许有轻微水圈。(35~25分)曲香较浓郁,较纯正、无异味。(25~20分)≤1.5 mm(10~8分)85~100≤2.0 mm(8~5分)70~84≤2.5 mm(≤5分)60~69
1.3.4 大曲理化特性分析
水分、酸度、液化酶活力、糖化酶活力、酯化酶活力、发酵力:按照QB/T 4257—2011《酿酒大曲通用分析法》及地方标准DB37/T 1231—2009《大曲通用技术条件》进行测定。
1.3.5 高通量测序分析
(1)真菌菌群总基因组DNA提取、PCR扩增及测序
真菌菌群总基因组DNA的提取按照E.Z.N.A.R土壤DNA试剂盒的说明步骤进行,提取DNA的质量采用1%的琼脂糖凝胶电泳检测,其浓度和纯度用NanoDrop2000测定。以提取的总基因组DNA为模板,采用通用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')/ITS2R(5'-GCTGCGTTCTTCATCGATGC-3')对真菌的ITS1区基因序列进行PCR扩增。PCR扩增体系:5×TransStart FastPfu缓冲液4 μL,2.5 mmol/L dNTPs 2 μL,上游引物ITS1F(5 μmol/L)和下游引物ITS2R(5 μmol/L)各0.8 μL,TransStart FastPfu DNA聚合酶0.4 μL,模板DNA 10 ng,双蒸水(ddH2O)补足至20 μL。PCR扩增条件:95 ℃预变性3 min;95 ℃变性30 s,55 ℃退火45 s,72 ℃延伸45 s,共35个循环;最后72 ℃延伸10 min。PCR扩增产物的回收和纯化分别使用2%琼脂糖凝胶和AxyPrep DNA胶提取试剂盒,使用QuantusTM荧光分析仪对回收产物进行检测定量,并使用NEXTflexTM Rapid DNASeq Kit进行文库构建,最终有效的文库序列委托上海美吉生物医药科技有限公司利用Illumina公司的Miseq PE300平台进行测序。
(2)序列数据处理与生信分析
下机后的原始序列数据由QIIME(v1.9.1,http://qiime.org/install/index.html)处理。通过FLASH(v1.2.11,https://ccb.jhu.edu/software/FLASH)对原始reads进行过滤,去除接头、低质量和模糊的碱基,进行拼接得到高质量的序列。使用UPARSE(v7.0.1090,http://drive5.com/uparse/)在相似性≥97%水平进行操作分类单元(operational taxonomic unit,OTU)归类。使用RDP分类器(v2.13,https://sourceforge.net/projects/r)对照Unite数据库(v8.0,http://unite.ut.ee/index.php)对真菌进行注释,最小置信阈值为0.7。使用USEARCH(v11,http://www.drive5.com/usearch)将所有高质量序列与OTU进行比较,生成每个样品的OTU丰度统计表。基于OTU水平,通过Mothur(v1.30.2,https://mothur.org/wiki/calculators/)和QIIME(v1.9.1)评估Alpha多样性和Beta多样性。
1.3.6 统计分析
采用Excel 2016软件对小麦主要品质指标和大曲理化性质进行统计分析,结果用“平均值±标准差”表示。基于OTU水平,采用非度量多维尺度法(non-metric multidimensional scaling,NMDS)分析不同小麦品种中温大曲样品的差异性。采用R语言(v3.3.1)vegan包基于皮尔逊(Pearson's rank)相关指数的冗余分析(redundancy analysis,RDA)对大曲优势真菌属与理化性质间的相关性进行分析。采用R语言(v3.3.1)heatmap包基于斯皮尔曼相关系数(Spearman's rank)对小麦品质指标与主要真菌属的相关性进行分析。
2 结果与分析
2.1 小麦的品质特性
不同品种小麦的主要品质特性指标见表2。由表2可知,5种小麦的主要品质特性存在一定差异。所有小麦的淀粉含量接近,为68.07%~70.10%。C小麦的粉质率(95%)、粗蛋白(14.20%)和湿面筋含量(29.07%)最高;D小麦的粗蛋白(14.07%)和湿面筋含量(29.03%)接近于C小麦,但其粉质率(28%)相对较低;E小麦有最低的粗蛋白含量(12.31%)和湿面筋含量(25.40%);而A小麦和B小麦的粗蛋白和湿面筋含量均处于上述两类小麦的同等指标之间。对照国家标准GB/T 17320—2013《小麦品种品质分类》可知,C和D小麦均属于强筋小麦(粗蛋白含量≥14.0%),且属于河南省强筋小麦品种范畴[28],E小麦属于弱筋小麦(粗蛋白含量<12.5%,湿面筋含量<26.0%),A、B小麦品种的粗蛋白、湿面筋等指标分别符合中强筋小麦(粗蛋白含量≥14.0%,湿面筋含量≥28.0%)和中筋小麦(粗蛋白≥12.5%,湿面筋含量≥26.0%)的品质标准,因此A、B小麦分别属于中强筋小麦和中筋小麦。
表2 不同品种小麦的主要品质特性
Table 2 Predominant quality properties of different wheat varieties
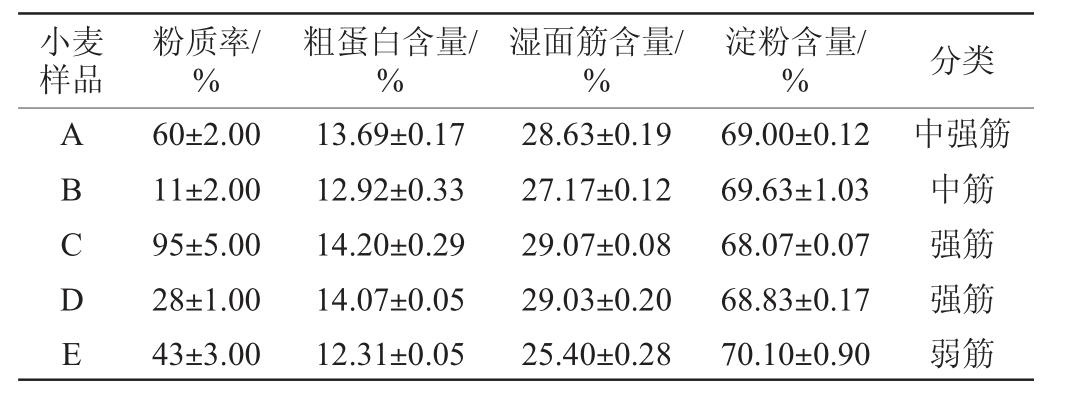
小麦样品粉质率/%粗蛋白含量/%湿面筋含量/%淀粉含量/% 分类ABCDE 60±2.00 11±2.00 95±5.00 28±1.00 43±3.00 13.69±0.17 12.92±0.33 14.20±0.29 14.07±0.05 12.31±0.05 28.63±0.19 27.17±0.12 29.07±0.08 29.03±0.20 25.40±0.28 69.00±0.12 69.63±1.03 68.07±0.07 68.83±0.17 70.10±0.90中强筋中筋强筋强筋弱筋
2.2 中温大曲品质分析
2.2.1 感官质量评定
5种中温大曲的感官评定结果见图1。由图1可知,中温大曲BMD的综合感官评价得分最高,次之为中温大曲DMD和AMD,而中温大曲CMD和EMD综合得分最低。从外观及综合评分来看,中温大曲BMD、AMD和DMD均有较高的得分,而大曲EMD得分最低;从断面评分来看,除中温大曲DMD外,其他4种大曲均有较高的得分;从香气评分来看,中温大曲BMD、CMD和DMD均有较高的得分,其原因可能与大曲样本产香菌群的组成及其代谢活动有关。总体来看,大曲BMD具有浓香型白酒中温大曲的感官特性优势,即中筋小麦制成的成品大曲具有优良的感官品质特性,中温大曲DMD和AMD次之。然而,弱筋小麦中温大曲EMD综合得分较低,这可能与其品质特性及化学组成影响曲块成型、大曲微生物生长等情况有关。
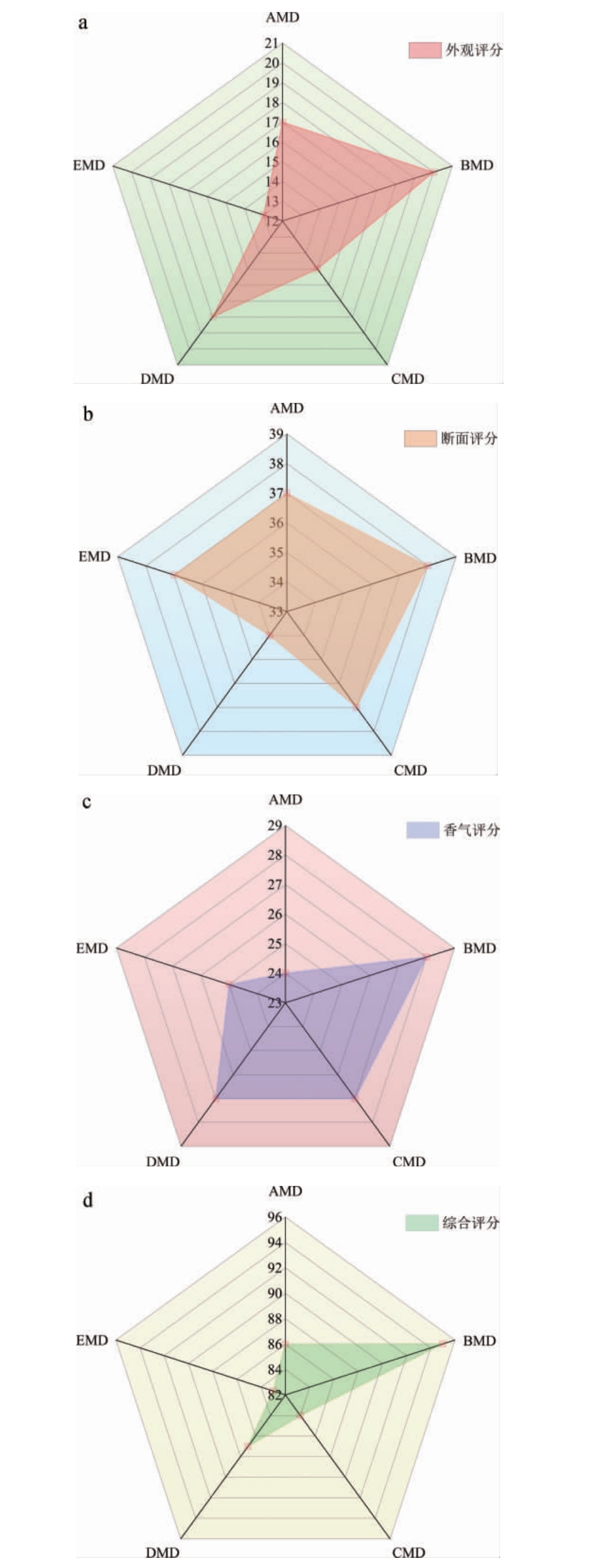
图1 不同品种小麦中温大曲成曲的感官评定结果
Fig.1 Sensory evaluation results of medium-temperature Daqu from different wheat varieties
2.2.2 理化特性
5种中温大曲的理化特性见表3。
表3 不同品种小麦中温大曲样品的理化特性指标
Table 3 Physiochemical properties indexes of medium-temperature Daqu samples from different wheat varieties
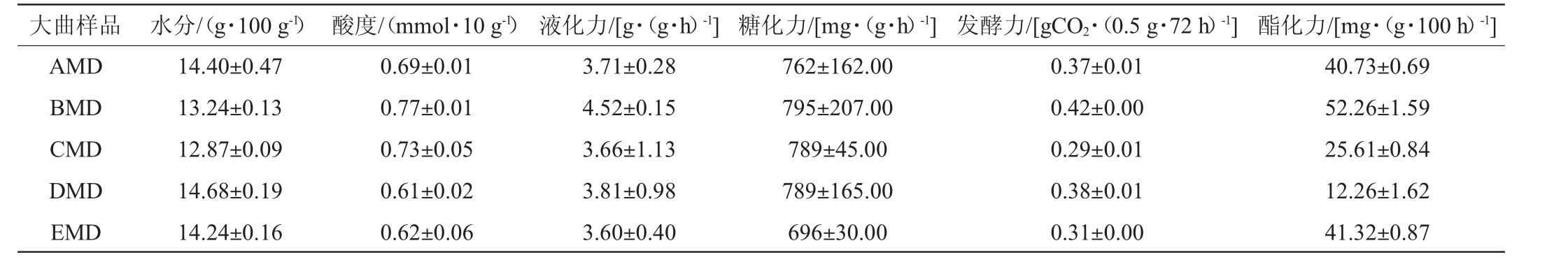
大曲样品 水分/(g·100 g-1) 酸度/(mmol·10 g-1) 液化力/[g·(g·h)-1] 糖化力/[mg·(g·h)-1] 发酵力/[gCO2·(0.5 g·72 h)-1] 酯化力/[mg·(g·100 h)-1]AMD BMD CMD DMD EMD 14.40±0.47 13.24±0.13 12.87±0.09 14.68±0.19 14.24±0.16 0.69±0.01 0.77±0.01 0.73±0.05 0.61±0.02 0.62±0.06 3.71±0.28 4.52±0.15 3.66±1.13 3.81±0.98 3.60±0.40 762±162.00 795±207.00 789±45.00 789±165.00 696±30.00 0.37±0.01 0.42±0.00 0.29±0.01 0.38±0.01 0.31±0.00 40.73±0.69 52.26±1.59 25.61±0.84 12.26±1.62 41.32±0.87
水分和酸度是微生物生长的必要条件,同时也是大曲贮存和品质特性评价的必要项目(QB/T 4259—2011《浓香大曲》)。尽管较高的水分含量较有利于细菌和部分真菌如酵母菌的快速生长,然而,水分过高不利于大曲贮藏,过低易使曲块干硬,不利于微生物存活与大曲品质保证[24]。由表3可知,5种中温大曲的水分含量和酸度均满足QB/T 4259—2011《浓香大曲》中成熟大曲的要求,其中,中温大曲AMD、DMD和EMD均有较高的水分含量(≥14.0 g/100 g),而中温大曲CMD水分含量较低(12.87%)。大曲水分含量与原料小麦中氮含量形成的大曲微孔结构有关,太高含量的蛋白质会导致大曲成型时结构疏松,疏松的微孔结构加速了培曲过程中水分的蒸发和传递[29]。因此,强筋小麦制曲会产生较低的水分含量,这与前期研究报道相一致[24]。相反,小麦过低的蛋白质会使曲块结构致密,培曲时水分不易蒸发,从而影响微生物的生长代谢,这与弱筋小麦中温大曲EMD具有较低的感官得分相一致。
酸类物质是白酒主要呈香呈味物质,同时也是白酒色谱骨架酯类香气物的前体物[30]。总酸度是酸类物质的综合体现,不仅是评价大曲成熟度的重要判断依据,也是衡量酒醅发酵质量的主要指标[31]。酸度过高,易于掩盖香气,酸度过低则不利于呈香,因此,大曲酸度会影响其酒醅的发酵,进而影响原酒质量[31]。大曲酸度的形成与来源于制曲环境产酸菌的生长和代谢密切相关[32]。5种大曲的酸度均在0.60~0.80 mmol/10 g之间,差异不大,说明5个小麦品种对产酸菌富集及代谢影响较小。液化力和糖化力是原料中淀粉转化为糊精与糖的能力[33]。浓香型大曲的糖化力一般为100~1 000 U(QB/T 4259—2011《浓香大曲》),5种不同中温大曲的糖化力均符合要求。然而,中温大曲EMD具有相对较低的液化力和糖化力,其他4种中温大曲差异不大,这表明弱筋小麦影响大曲微生物代谢产生液化酶和糖化酶的能力,而中筋或中强筋小麦利于提高大曲淀粉酶的活力,这可能与不同品种小麦富集产淀粉酶微生物的种群组成有关。大曲的酯化力和发酵力影响酒醅酯类物质的合成与乙醇的形成,是大曲提升酒醅发酵品质的主要特性指标[34]。5种中温大曲的发酵力和酯化力差异较大,中温大曲BMD具有最高的发酵力和酯化力,分别为0.42 g CO2/(0.5 g·72 h)和52.26 mg/(g·100 h),而中温大曲CMD和DMD分别有最低的发酵力和酯化力,这可能与不同小麦大曲产酯酶菌群和发酵菌群的组成有关,同时也说明中筋小麦有利于发酵菌和产酯酶菌群的富集与代谢。
2.3 中温大曲真菌群落多样性的高通量测序分析
2.3.1 Alpha多样性分析
通过高通量测序,从5种中温大曲共15个样本中获得74 474条真菌有效序列。采用Sobs指数、Chao1指数、Shannon指数可对大曲真菌群落的Alpha多样性进行分析。其中Sobs指数、Chao1指数分别表示可观测物种丰富度和估算物种的丰富度,该指数越大,表示真菌群落丰富度越高;Shannon指数表示物种多样性,Shannon指数越大,表示真菌物种多样性越高。5种中温大曲样品真菌菌群的Alpha多样性分析结果见表4。由表4可知,5种中温大曲样本的真菌序列覆盖度均>99%,说明测序结果能正确反映样本真菌群落的真实信息。5种中温大曲真菌菌群丰度及多样性存在一定差异,其中,中温大曲EMD的Sobs指数、Chao1和Shannon指数均较小,说明该小麦中温大曲的真菌菌群丰富度及多样性均较低。相反的,中温大曲AMD的3个指数值均较大,说明该小麦中温大曲真菌菌群多样性较高,而中温大曲BMD的Chao1指数最高,表明该小麦中温大曲真菌菌群的丰富度较高。
表4 中温大曲样品真菌群落的Alpha多样性指数
Table 4 Alpha diversity indexes of fungal communities in mediumtemperature Daqu samples
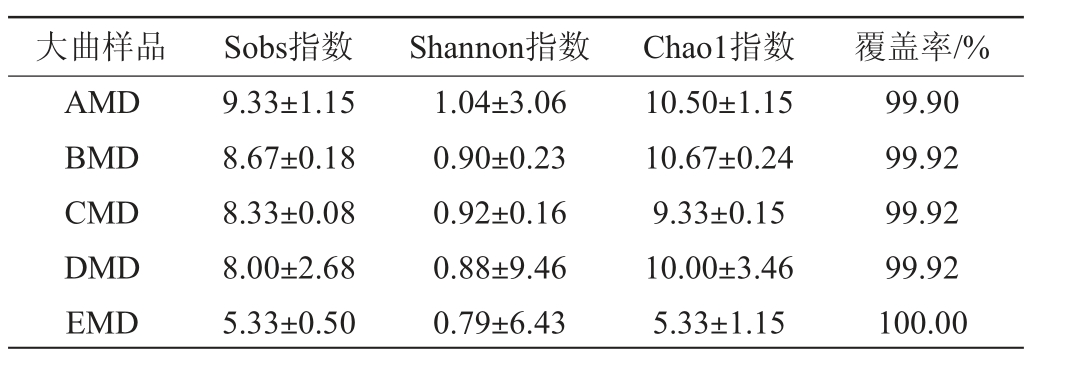
大曲样品 Sobs指数 Shannon指数 Chao1指数 覆盖率/%AMD BMD CMD DMD EMD 9.33±1.15 8.67±0.18 8.33±0.08 8.00±2.68 5.33±0.50 1.04±3.06 0.90±0.23 0.92±0.16 0.88±9.46 0.79±6.43 10.50±1.15 10.67±0.24 9.33±0.15 10.00±3.46 5.33±1.15 99.90 99.92 99.92 99.92 100.00
2.3.2 基于OTU水平中温大曲真菌菌群Venn图与聚类分析
为直观表现5种中温大曲样品中真菌菌群的共有物种和特有物种数目,基于真菌OTU水平绘制5种中温大曲样品的Venn图,结果见图2。由图2可知,中温大曲AMD、BMD、CMD、DMD和EMD特有的OTU数分别为16、36、41、19、22个,共有的OTU数为35个。中温大曲CMD和BMD具有较高的OTU总数和独有的OTU数,说明部分强筋小麦和中筋小麦均可富集更多的真菌群落,但其种群存在一定的差异。
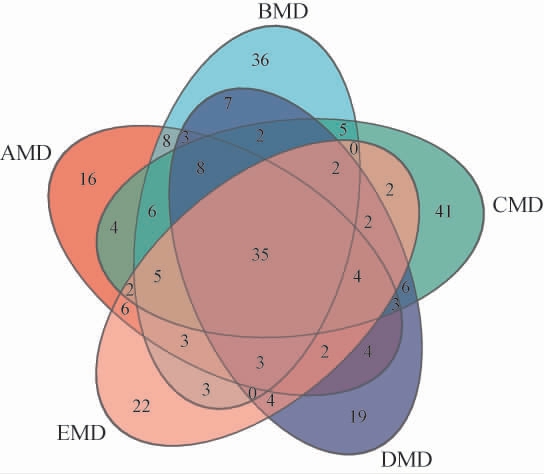
图2 基于操作分类单元水平中温大曲样品真菌菌群的Venn图
Fig.2 Venn diagram of fungal communities in medium-temperature Daqu samples based on operational taxonomic unit level
为考察5种中温大曲样品之间的真菌菌群分布差异,基于OTU水平对5种中温大曲样品的真菌菌群进行NMDS分析,结果见图3。由图3可知,stress<0.2,说明该模型具有一定的解释意义。在OTU水平,中温大曲CMD和BMD样品位于第一和第四象限,而其他的3个中温大曲样本基本集中在第二和第三象限,说明中温大曲CMD和BMD有独特的真菌组成,而中温大曲AMD、DMD和EMD具有相似的真菌组成。值得注意的是,中温大曲DMD为强筋小麦大曲,但其样本分布接近大曲AMD和EMD,这可能与D小麦较低的粉质率或其他品质特性有关。
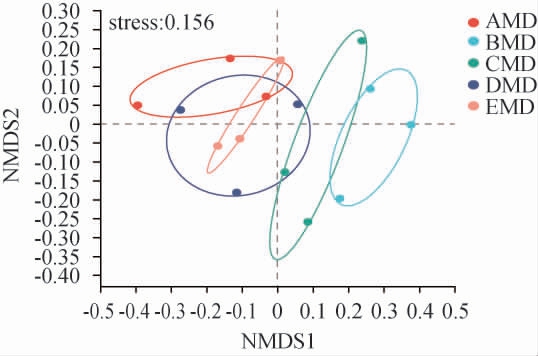
图3 基于操作分类单元水平中温大曲样品真菌菌群的非度量多维尺度法分析结果
Fig.3 Non-metric multidimensional scaling analysis results of fungal communities in medium-temperature Daqu samples based on operational taxonomic unit level
2.3.3 真菌菌群组成分析
基于门、属和种水平5种中温大曲样品真菌菌群的组成见图4。
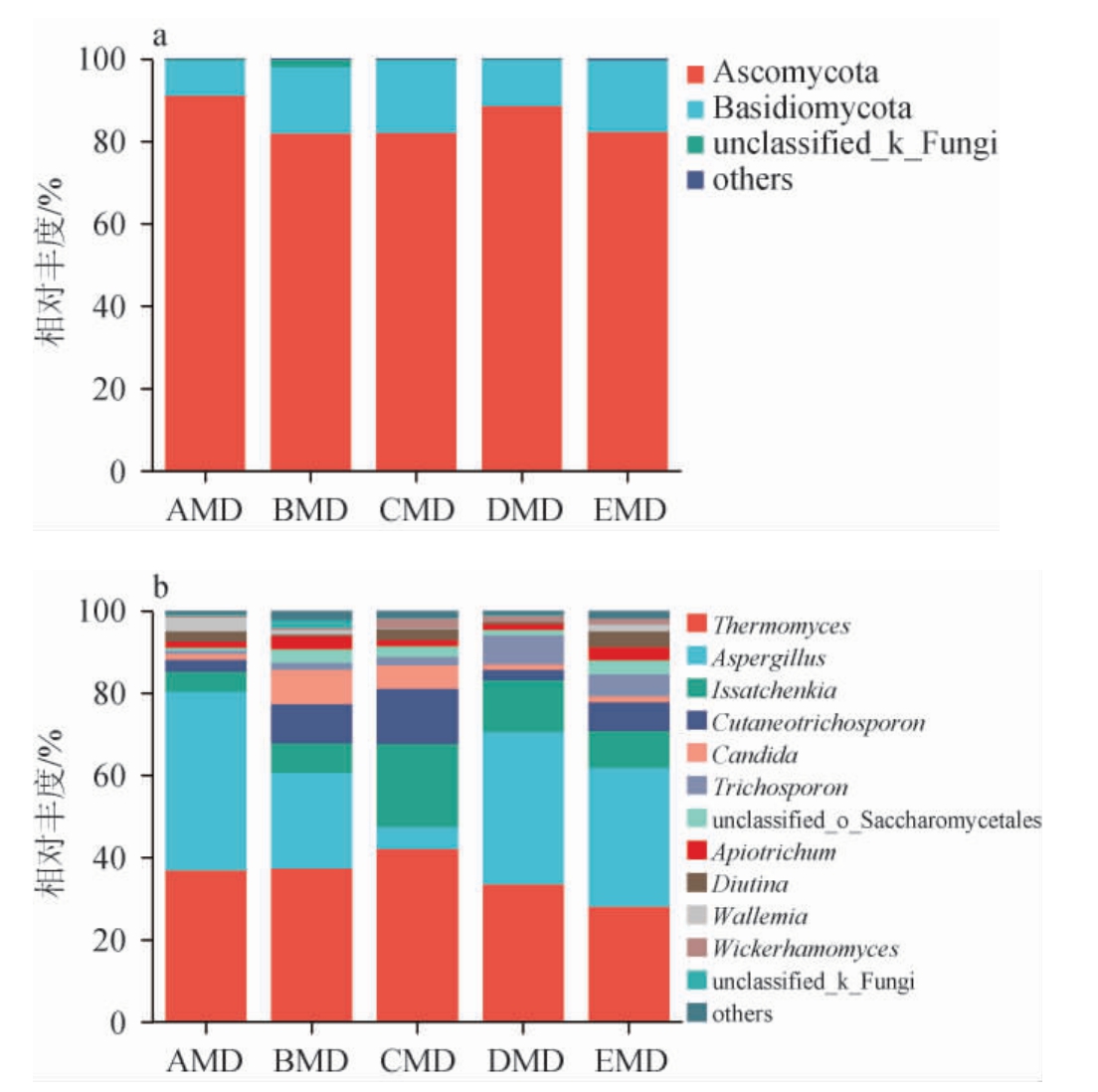
图4 基于门(a)和属(b)水平中温大曲样品真菌群落组成
Fig.4 Composition of the fungal communities in mediumtemperature Daqu samples based on phylum (a) and genus (b) level
others:相对丰度≤1%的其他菌门、属。
由图4a可知,从5种中温大曲样品中共注释到3个优势真菌门(相对丰度>1%),分别为子囊菌门(Ascomycota)、担子菌门(Basidiomycota)和未分类的真菌(unclassified_k_Fungi),且子囊菌门(Ascomycota)的相对丰度为81.99%~91.02%,成为5种中温大曲共有的绝对优势真菌门。5种中温大曲中2个优势真菌门相对丰度均较为接近,此外,中温大曲BMD中检测到相对丰度为1.88%的未分类的真菌门(unclassified_k_Fungi)。
由图4b可知,从5种中温大曲样品中共注释到12个优势真菌属(相对丰度>1%),分别为嗜热真菌属(Thermomyces)(27.87%~42.02%)、曲霉属(Aspergillus)(5.35%~43.52%)、伊萨酵母属(Issatchenkia)(7.11%~20.16%)、Cutaneotrichosporon(2.58%~13.53%)、假丝酵母属(Candida)(1.28%~8.29%)、毛孢子菌属(Trichosporon)(0.66%~7.05%)、未分类的酵母目(unclassified_o_Saccharomycetales)(0.76%~3.40%)、Apiotrichum(1.53%~3.31%)、Diutina(0.37%~3.71%)、节担菌属(Wallemia)(0.24%~3.36%)、威克汉姆酵母属(Wickerhamomyces)(0.40%~2.30%)、未分类的真菌(unclassified_k_Fungi)(0.15%~1.88%)。12个优势真菌属均为5种中温大曲样品的共有真菌属,但主要优势真菌属有5个,分别为Thermomyces、Aspergillus、Issatchenkia、Cutaneotrichosporon和Candida。中温大曲CMD含有最高相对丰度的Thermomyces(42.02%)和最低相对丰度的Aspergillus(5.35%),而两者在中温大曲AMD、DMD和EMD中的相对丰度接近。Issatchenkia、Cutaneotrichosporon和Candida的总相对丰度在中温大曲CMD中最高(39.39%),在中温大曲BMD中次之(25.04%),在中温大曲AMD中最低(9.25%),说明部分强筋小麦利于富集酵母菌,而不利曲霉菌的生长,这与前期研究报道相一致[24]。相对其他4种小麦中温大曲,除Thermomyces之外,中温大曲BMD有相对丰度较为均衡的主要优势真菌属,说明中筋小麦更利于富集种类丰富的大曲功能真菌。主要优势真菌属在5种中温大曲中的分布情况与NMDS分析结果基本相符。
2.4 真菌群落与大曲理化特性及小麦主要品质的相关性分析
2.4.1 真菌群落与大曲理化特性的相关性分析
选取中温大曲样品中平均相对丰度位居前20的主要真菌属与大曲理化特性之间的相关性进行分析,发现有8个真菌属与其存在相关性,结果见图5。由图5可知,Aspergillus和Trichosporon与水分和糖化力呈正相关。曲霉属作为大曲优势真菌属,在浓香大曲中具有富集淀粉酶的能力,对大曲糖化力具有一定的贡献[35]。假丝酵母属和未分类的酵母目(unclassified_O_Saccharomycetales)与酸度、液化力、酯化力和发酵力均呈正相关,Issatchenkia、Cutaneotrichosporon和Apiotrichum与酯化力和发酵力呈负相关,Thermomyces与酸度和液化力呈正相关,而与糖化力和水分呈负相关。根据代谢功能,酒曲酵母一般分为两类即产酒酵母和产香酵母。Candida和酵母菌属(Saccharomyces)多为产香酵母,对白酒香气物质有着特殊的贡献[36]。此外,白酒香气物质多以酯类物质为主,而其合成离不开酯化酶的作用,因此,促进酯类物质合成的酵母应该具有代谢酯化酶的能力。有研究报道,扁平云假丝酵母(Candida humilis)与酿酒酵母(Saccharomyces cerevisiae)混合发酵葡萄酒能产生较高含量的酯类物质[37]。来自白酒发酵的一些酵母属如假丝酵母、毕赤酵母等的某些种用于大曲强化,均有利于促进提升白酒品质[38]。上述研究表明,假丝酵母属和酵母菌属与酯化酶具有一定的正相关性。Issatchenkia是浓香白酒酿造生态系统常见的酵母菌,彭远凤等[39]将一株东方伊萨酵母(Issatchenkia orientalis)接种到酒醅和黄水构建的浓香型白酒酿造微生物体系中进行发酵,结果发现,Issatchenkia orientalis会改变酒醅微生物组成结构,促进醇类挥发性化合物的形成,显著增加高级醇的含量。本研究中,Issatchenkia作为中温大曲CMD的优势真菌,与大曲的酯化力呈负相关,说明伊萨酵母属与大曲微生物共发酵,不利于酯类物质的增加,这与CAO J等[40]的研究结果相一致。理论上讲,Issatchenkia相对丰度越高,越有利于提高大曲发酵力,但试验结果表明Issatchenkia与大曲发酵力呈负相关,这说明单一微生物不能决定大曲的理化特性,而是通过多种微生物的相互作用共同决定[40]。Thermomyces与大曲酸度和液化力呈正相关,这可能与Thermomyces具有代谢产酸和产生淀粉酶功能有关[41-42]。
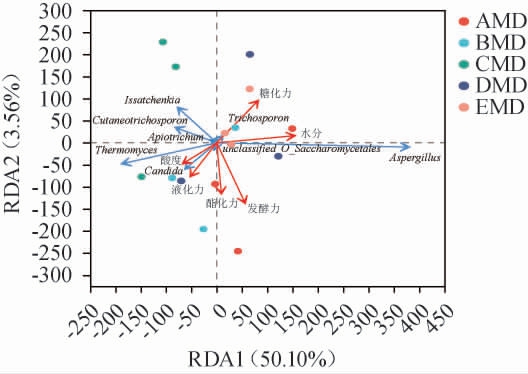
图5 中温大曲样品真菌属与理化特性的冗余分析结果
Fig.5 Redundancy analysis results between fungal genera and physiochemical properties of medium-temperature Daqu samples
2.4.2 真菌群落与小麦品质的相关性性分析
基于斯皮尔曼相关系数对制曲小麦的主要品质指标(粉质率、粗蛋白、湿面筋、淀粉)与大曲主要真菌属(平均相对丰度位居前20)的相关性进行分析,结果见表5。
表5 小麦的主要品质指标与中温大曲样品主要真菌属的相关性分析结果
Table 5 Analysis results of the correlation between main quality indexes of wheat and dominant fungal genara in medium-temperature Daqu samples

注:“*”表示显著相关(P<0.05);“**”表示极显著相关(P<0.01)。
真菌属 粉质率 粗蛋白 湿面筋 淀粉Thermomyces Aspergillus Issatchenkia Cutaneotrichosporon Candida Trichosporon unclassified_o_Saccharomycetales Apiotrichum Diutina Wallemia Wickerhamomyces unclassified_k__Fungi Monascus Cladosporium unclassified_f_Microascaceae unclassified_f_Saccharomycetales Thermoascus unclassified_p_Ascomycota Lichtheimia Mortierella 0.075-0.182 0.154 0.114 0.186-0.193 0-0.136 0.621*0.086 0.156-0.223-0.150-0.036-0.010-0.174-0.170-0.671**0.048-0.103 0.086-0.161 0.175 0.004 0.186-0.057-0.068-0.321*0.007-0.411*-0.143-0.005 0.184 0.399*-0.699**0.198-0.116-0.593*-0.059 0.045 0.086-0.161 0.175 0.004 0.186-0.057-0.068-0.321*0.007-0.411*-0.143-0.005 0.184 0.399*-0.699**0.198-0.116-0.593*-0.059 0.045 0.020 0.130-0.138-0.193-0.071 0.214-0.089 0.147 0.005 0.388*0.120 0.005-0.029-0.384*0.595*-0.107 0.126 0.544*0.315-0.050
平均相对丰度位居前5的真菌属即Thermomyces、As pergillus、Issatchenkia、Cutaneotrichosporon 和Candida 中,Aspergillus与原料小麦的粉质率、粗蛋白和湿面筋呈负相关,而与淀粉呈正相关,而Issatchenkia、Cutaneotrichosporon和Candida则恰好相反,说明高淀粉低蛋白的原料小麦可能更利于富集曲霉菌,而高蛋白的原料小麦可能更有利于富集酵母菌。曲霉属和酵母菌属是酿酒大曲主要的两大类真菌属,对大曲淀粉酶、酒化酶及酯化酶均起重要贡献作用,选育适宜两大类优势菌属生长代谢的小麦品种是酿酒小麦育种领域值得研究的课题。粗蛋白和湿面筋含量显著正相关于枝孢属(Cladosporium)(P<0.05),而显著负相关于Apiotrichum、节担菌属(Wallemia)、未分类的小囊菌科(unclassified_f_Microascaceae)和未分类的子囊菌门(un classified_p_Ascomycota)(P<0.05或P<0.01)。淀粉含量与主要真菌属的相关性则与上述情况恰好相反,即淀粉含量显著正相关于Wallemia、unclassified_f_Microascaceae和unclassified_p_Ascomycota(P<0.05),而显著负相关于Cladosporium(P<0.05),这充分说明,制曲小麦蛋白或湿面筋对大曲真菌的影响与淀粉的影响则是一对相反的关系,这与前期的研究结果相一致[24]。粉质率与Diutina呈显著正相关(P<0.05),而与unclassified_p_Ascomycota呈极显著的负相关(P<0.01)。Diutina的某些种如皱褶念珠菌(Diutina rugosa)常被认为是环境污染的有害真菌[43],而其在酿酒微生态系统中的作用及其来源并不清楚。此外,粉质率与真菌的相关性接近粗蛋白或湿面筋与真菌的关系。尽管本研究初步明确了小麦主要品质指标即粗蛋白(或湿面筋)、淀粉及粉质率与主要真菌的相关性,但具体的影响机制并不清楚,需要进一步的研究探索。
3 结论
本研究对河南4个品种酿酒小麦及酒厂制曲应用的混合花麦(对照组小麦)的主要品质指标进行了分析比较。根据小麦粗蛋白和湿面筋含量,5种制曲小麦可分为强筋、中强筋、中筋和弱筋四类即小麦A为中强筋小麦、B为中筋小麦、C和D小麦均为强筋小麦、E为弱筋小麦。比较分析了5种小麦生产的中温大曲的真菌群落、感官品质及理化特性。结合大曲理化特性和感官综合评定,中筋小麦中温大曲BMD具有最优良的品质特性,DMD次之,其大部分理化特性指标、外观及感官综合评分均接近混合花麦中温大曲AMD。高通量测序结果表明,5种中温大曲共注释到3个优势真菌门、12个优势真菌属,且共同的主要优势真菌属为Thermomyces、Aspergillus、Issatchenkia、Cutaneotrichosporon和Candida,但优势真菌属的平均相对丰度并不一致。强筋小麦中温大曲CMD含有最高丰度的Thermomyces和最低丰度的Aspergillus,而中温大曲AMD、DMD和EMD均有相似相对丰度的Thermomyces和Aspergillus,大曲BMD含有相对丰度较为均衡的4种优势真菌属(Aspergillus、Is satchenkia、Cutaneotrichosporon和Candida)。8个优势真菌属与大曲理化特性存在一定相关性。小麦粗蛋白和湿面筋显著正相关于Cladosporium,而显著负相关于Apiotrichum、Wallemia、unclassified_f_Microascaceae 及unclassified_p_Ascomycota(P<0.05),淀粉含量与优势真菌属的相关性则与上述相反,粉质率也影响部分真菌属。研究结果初步明确了不同品种酿酒小麦中温大曲真菌类群组成及品质特性差异,初步了解了酿酒小麦主要品质指标对优势真菌的影响,为适宜制曲小麦品种选育和稳定大曲品质提供了理论依据。
[1]LIU H L, SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].J Agr Food Chem,2018,66(22):5425-5432.
[2]MA S Y, SHANG Z C, CHEN J, et al.Differences in structure, volatile metabolites, and functions of microbial communities in Nongxiangxing Daqu from different production areas[J].LWT-Food Sci Technol,2022,166:113784.
[3]WANG D Q,CHEN L Q,YANG F,et al.Yeasts and their importance to the flavour of traditional Chinese liquor:a review[J].J I Brewing,2019,125(2):214-221.
[4]LIU Y B,LI H D,DONG S M,et al.Dynamic changes and correlations of microbial communities,physicochemical properties,and volatile metabolites during Daqu fermentation of Taorong-type Baijiu[J].LWT-Food Sci Technol,2023,173:114290.
[5]ZENG Y,WANG Y,CHEN Q,et al.Dynamics of microbial community structure and enzyme activities during the solid-state fermentation of Forgood Daqu:a starter of Chinese strong flavour Baijiu[J].Arch Microbiol,2022,204:577.
[6]KANG J M,JIA L L,ZHANG Z X,et al.Comparison of physicochemical characteristics and microbiome profiles of low-temperature Daqu with and without adding tartary buckwheat[J].Food Biosci,2022,49:101931.
[7]LIU J J,CHEN J Y,FAN Y,et al.Biochemical characterisation and dominance of different hydrolases in different types of Daqu-a Chinese industrial fermentation starter[J].J Sci Food Agr,2018,98(1):113-121.
[8]DU H,SUN J,ZHOU T C,et al.A High-throughput absolute abundance quantification method for the characterisation of Daqu core fungal communities[J].Fermentation,2022,8:345.
[9]KANG J M,CHEN X X,HAN B Z,et al.Insights into the bacterial,fungal,and phage communities and volatile profiles in different types of Daqu[J].Food Res Int,2022,158:111488.
[10]YAN S B, TONG Q Q, GUANG J Q.Yeast dynamics and changes in volatile compounds during the fermentation of the traditional Chinese strong-flavor Daqu[J].LWT-Food Sci Technol,2019,106:57-63.
[11]DENGYK,HUANGD,HANBL,et al.Correlation:between autochthonous microbial diversity and volatile metabolites during the fermentation of Nongxiang Daqu[J].Front Microbiol,2021,12:688981.
[12]陈蒙恩,侯建光,张振科,等.陶融型大曲微生物多样性与挥发性风味成分的相关性研究[J].中国酿造,2020,39(10):54-60.
[13]范光森,许岱,富志磊,等.古井贡酒曲中酵母的分离及其产香挥发性风味物质分析[J].中国食品学报,2018,18(7):220-229.
[14]HE M W, JIN Y, ZHOU R Q, et al.Dynamic succession of microbial community in Nongxiangxing Daqu and microbial roles involved in favor formation[J].Food Res Int,2022,159:111559.
[15]HUANG Y H, YI Z L, JIN Y L, et al.Metatranscriptomics reveals the functions and enzyme profiles of the microbial community in Chinese nong-flavor liquor starter[J].Front Microbiol,2017,8:1747.
[16]MA R F,SUI L,ZHANG J S,et al.Polyphasic characterization of yeasts and Lactic acid bacteria metabolic contribution in semi-solid fermentation of Chinese Baijiu (Traditional fermented alcoholic drink): towards the design of a Tailored starter culture[J].Microorganisms,2019,7(5):147.
[17]CAO X Z,YOU J M,REN L S,et al.Isolation and identification of yeasts from Luzhou flavor Daqu[J].Adv Appl Microbiol,2015,5(5):56305.
[18]ABEDINIFAR S, KARIMI K, KHANAHMADI M, et al.Ethanol production by Mucor indicus and Rhizopus oryzae from rice straw by separate hydrolysis and fermentation[J].Biomass Bioenerg,2009,33:828-833.
[19]ZHU Q,CHEN L Q,PENG Z,et al.Analysis of environmental driving factors on core functional community during Daqu fermentation[J].Food Res Int,2022,157:111286.
[20]李兵,张超,王玉霞,等.白酒大曲功能微生物与酶系研究进展[J].中国酿造,2019,38(6):7-12.
[21]朱丽萍,杨强,江威,等.清香型小曲白酒霉菌菌群解析与酶活特性研究[J].食品与发酵工业,2022,48(7):70-77.
[22]MA S Y,LUO H B,ZHAO D,et al.Environmental factors and interactions among microorganisms drive microbial community succession during fermentation of Nongxiangxing Daqu[J].Bioresour Technol,2022,345:126549.
[23]WANG P, WU Q, JIANG X J, et al. Bacillus licheniformis affects the microbial community and metabolic profile in the spontaneous fermentation of Daqu starter for Chinese liquor making[J].Int J Food Microbiol,2017,250:59-67.
[24]HOU X,HUI M,SUN Z K,et al.Associations between wheat varieties and the functional microbial community of Nongxiangxing Daqu from northern China[J].LWT-Food Sci Technol,2023,185:115119.
[25]黄瑜,杨帆,李江华,等.小麦原料微生物组成对高温大曲风味的影响[J].食品与发酵工业,2021,47(20):22-29.
[26]LIU C C,FENG S B,WU Q,et al.Raw material regulates flavor formation via driving microbiota in Chinese liquor fermentation[J].Front Microbiol,2019,10:1520.
[27]HELL J, PRÜCKLER M, DANNER L, et al.A comparison between near-infrared (NIR) and mid-infrared (ATR-FTIR) spectroscopy for the multivariate determination of compositional properties in wheat bran samples[J].Food Control,2016,60:365-369.
[28]信息荟萃.河南省强筋中强筋及弱筋小麦品种清单[J].粮食加工,2020,45(4):61.
[29]刘淼,丁丽,赵梦梦,等.基于主成分分析的不同小麦品种大曲发酵动态品质评价[J].食品与发酵工业,2020,46(6):19-24.
[30]WU Y S,HOU Y X,CHEN H,et al."Key Factor"for Baijiu quality:research progress on acid substances in Baijiu[J].Foods, 2022, 11(19):2-26.
[31]ZHAO X Y,LI J H,DU G C,et al.The influence of seasons on the composition of microbial communities and the content of lactic acid during the fermentation of Fen-flavor Baijiu[J].Fermentation,2022,8:740.
[32]ZHU M,ZHENG J,XIE J,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Res Int,2022,153:110955.
[33]LI Z M, CHEN L, BAI Z H, et al.Cultivable bacterial diversity and amylase production in two typical light-flavor Daqus of Chinese spirits[J].Front Life Sci,2015,8(3):264-270.
[34]TANG J,CHEN J,CHEN D M,et al.Structural characteristics and formation mechanism of microbiota related to fermentation ability and alcohol production ability in Nongxiang Daqu[J].Foods,2022,11:2602.
[35]XIA Y, ZHOU W, DU Y K, et al.Difference of microbial community and gene composition with saccharification function between Chinese nongxiangxing daqu and jiangxiangxing daqu[J].J Sci Food Agr,2023,103(2):637-647.
[36]FAN G S,TENG C,XU D,et al.Improving ethyl acetate production in Baijiu manufacture by Wickerhamomyces anomalus and Saccharomyces cerevisiae mixed culture fermentations[J].BioMed Res Int,2019,2019:1470543.
[37]尤雅,段长青,燕国梁.扁平云假丝酵母与酿酒酵母混合发酵对葡萄酒乙醇含量及香气的影响[J].食品科学,2018,39(20):146-154.
[38]LIU S P,HU J,XU Y Z,et al.Combined use of single molecule real-time DNA sequencing technology and culture-dependent methods to analyze the functional microorganisms in inoculated raw wheat Qu[J].Food Res Int,2020,132:109062.
[39]彭远凤,杨阳,赵东,等.东方伊萨酵母对浓香型白酒酒醅微生物群落结构及挥发性风味物质合成的影响[J/OL].食品科学,1-12[2024-04-27].http://kns.cnki.net/kcms/detail/11.2206.ts.20231020.1731.056.html.
[40]CAO J,ZHENG Y,ZHAO T,et al.Changes in the microbial community structure during the digitally managed fermentation of medium-temperature Daqu[J].Food Sci Technol,2022,42:e87122.
[41]CHEN L C,YI Z L,FANG Y,et al.Biochemical and synergistic properties of a novel alpha-amylase from Chinese Nong-flavor Daqu[J].Microb Cell Fact,2021,20(1):80.
[42]ZHENG X W,HAN B Z. Baijiu,Chinese liquor: History,classification and manufacture[J].J Ethnic Foods,2016,3(1):19-25.
[43]SANCHIS M, SUTTON D A, WIEDERHOLD N P, et al.Efficacy of echinocandins against murine infections by Diutina(Candida)rugosa[J].Diagn Microbiol Infect Dis,2016,86(1):61-65.