中国白酒是世界上最古老的蒸馏酒之一,通常由高粱、小麦和玉米等高淀粉粮食酿造而成,有清香、浓香、酱香、米香四大基础香型[1-2]。白酒的主要成分是乙醇和水,占总含量的98%~99%。同时白酒也富含多种呈香呈味风味物质,其中酯类、醇类、有机酸类、醛酮类、酚类等风味物质占白酒总含量1%~2%[3],含量虽低,但其种类、组成及比例直接影响白酒的口感、风味及香气,从而影响白酒品质的好坏[4-6]。现目前,据报道已有3 000多种挥发性风味成分在白酒中被检出[2],其中包括有酯、酸、醇等主体风味化合物,还有吡嗪类、酚类、萜烯类等功能化合物和醛类、芳香族化合物等。
吡嗪类化合物是酱香型白酒中种类最多、含量最高的一类健康功能化合物,曾被确认为是酱香型白酒的特征成分[7]。吡嗪类化合物通常由美拉德反应形成[8]和枯草芽孢杆菌(Bacillus subtilis)可以在大豆的固态发酵过程中产生[9-10],具有护肝、改善血液循环、扩张血管等功能[11]。其中2,3,5,6-四甲基吡嗪(2,3,5,6-tetramethylpyrazine,2356TTM)是吡嗪类化合物的典型代表[12],呈现烘焙烤香气味,因其对心脑血管疾病有治疗和药理作用[13],在酱香型白酒中一度被学者认为是极其重要的健康因子,属于健康功能化合物[14-16]。
现目前对于酱香型白酒中吡嗪类化合物的检测方法已有较多研究,主要集中在气相和气质联用法[17-18]。王国明等[19]通过液液萃取结合气相色谱-质谱联用技术对浓香型山庄老酒中8种吡嗪类化合物进行定性和定量分析,发现并确定了6种化合物。黄杰等[20]用气相色谱-三重四级杆质谱联用仪内标法测定古井贡酒中的四甲基吡嗪,首次采用三重四级杆气质联用仪测定白酒中吡嗪化合物的含量,为下一步继续定量其他吡嗪类物质奠定了基础。以上方法前处理过程较为复杂,需要经过多次样品转移,由此带来目标化合物的损失,从而影响定量的准确性,具有一定的局限性。然而液质联用方法不受样品挥发度和热稳定性的限制,特别是通过多反应监测模式可提高检测的灵敏度和选择性,定性定量更为准确。
吡嗪类化合物作为酱香型白酒中特征风味成分,相关文献表明不同轮次酱香型白酒中吡嗪类化合物含量存在差异,刘家欢等[21]研究发现,不同轮次酒中吡嗪类化合物含量呈规律性变化,在一、二轮次酒中较低,三轮次开始升高,在中间轮次(三、四、五、六轮次酒)中均维持较高含量,但目前对于不同年份白酒中吡嗪类化合物的研究鲜见报道。研究不同年份酱酒中吡嗪类化合物的含量及其变化,对调控酱香型白酒的生产工艺,进而提高酱香型白酒的风味特征与健康功能具有重要的指导意义。
本研究采用超高效液相色谱-串联质谱(ultra-high performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)联用技术建立了同时测定不同年份酱香型白酒中12种吡嗪类化合物的检测方法,首先对液相色谱条件和前处理条件都进行优化,同时对该方法进行方法学考察和验证,最后对不同年份白酒样品中化合物含量进行测定,结合多元统计学方法对酱香型白酒样品进行分析,进一步发掘不同年份酱香型白酒样品中吡嗪类物质的差异性,对建立健全酱香型白酒检测体系,促进酱香型白酒生产数字化发展,加强酱香型白酒深层次研究有着重要意义。
1 材料与方法
1.1 材料与试剂
1.1.1 酱香型白酒样品
样品由某酱香型白酒生产企业提供。不同年份酱香型白酒样品信息见表1。
表1 不同年份酱香型白酒样品信息
Table 1 Sample information of sauce-flavor Baijiu of different aging years

序号 样品编号 贮存年份 样品名称123456 NFJ-5-1 NFJ-5-2 NFJ-10-1 NFJ-10-2 NFJ-15-1 NFJ-15-2 5年10年15年5年L3-0023(成品酒)5年L3-0030(成品酒)10年A04-236(成品酒)10年13坛号(成品酒)15年B04-76坛(成品酒)15年B04138(成品酒)
1.1.2 化学试剂
甲酸(色谱纯):上海安谱科技公司;甲醇、乙腈(均为色谱纯):德国默克公司;2-甲基吡嗪(2-methylpyrazine,2M)、2,5-二甲基吡嗪(2,5-dimethylpyrazine,25DM)、2,6-二甲基吡嗪(2,6-dimethylpyrazine,26DM)、2,3-二甲基吡嗪(2,3-dimethylpyrazine,23DM)、2-乙基-6-甲基吡嗪(2-ethyl-6-methylpyrazine,2E6M)、2,3,5-三甲基吡嗪(2,3,5-trimethylpyrazine,235TM)、2,3,5,6-四甲基吡嗪(2,3,5,6-tetramethylpyrazine,2356TTM)、2,3-二乙基-5-甲基吡嗪(2,3-dimethylpyrazine-5-ethyl,23DE5M)、2-乙基-3,5,6-三甲基吡嗪(2-ethyl-3,5,6-trimethylpyrazine,2E356TM)、2-乙基吡嗪(2-ethylpyrazine,2E)、3-乙基-2,5-二甲基吡嗪(3-ethyl-2,5-dimethylpyrazine,3E25DM)、2,3-二乙基-5-甲基吡嗪(2,3-dimethylpyrazine-5-ethyl,23DE5M)标准物质(均为色谱纯):北京振翔科技有限公司。
1.2 仪器与设备
Xevo TQ-XS UPLC-MS/MS仪:美国沃特世公司;3-30KS型高速离心机:美国Sigma公司;AB265-S型电子天平:瑞士METTLER TOLEDO公司;Milli-Q超纯水仪:美国密理博公司;N-EVAP 112型氮吹仪:美国Organomation公司;LGND130氮气发生器:上海安谱科技公司。
1.3 方法
1.3.1 样品前处理
取10.0 mL酒样于50 mL的刻度试管中,室温下用氮气缓慢吹至约2.0 mL,用超纯水定容至5.0 mL,振荡混匀后经0.45 μm滤膜过滤,4 ℃保存待测。
1.3.2 仪器条件
超高效液相色谱条件:ACQUITYUPLCBEHC18(2.1mm×100 mm,1.7 μm)色谱柱,柱温:40 ℃,流动相A:0.9%甲酸水溶液,流动相B:0.9%甲酸乙腈,梯度洗脱,0~1 min,93%A,1~12 min,87%A,12~12.5 min,93%A,12.5~17.0 min,93%A;流速:0.45 mL/min;进样体积:2 μL;柱温:40 ℃。
质谱条件:电喷雾离子(electrospray ionization,ESI+)源;多反应监测(multi-reaction monitoring,MRM)模式;毛细管电压0.5 kV,离子源温度150 ℃,脱溶剂气氮气(N2)温度450℃,脱溶剂气流速和锥孔气氮气(N2)流速分别为1000L/h、 150 L/h,MRM优化质谱参数见表2。
表2 多反应监测模式的优化参数
Table 2 Optimized parameters of multi-reaction monitoring
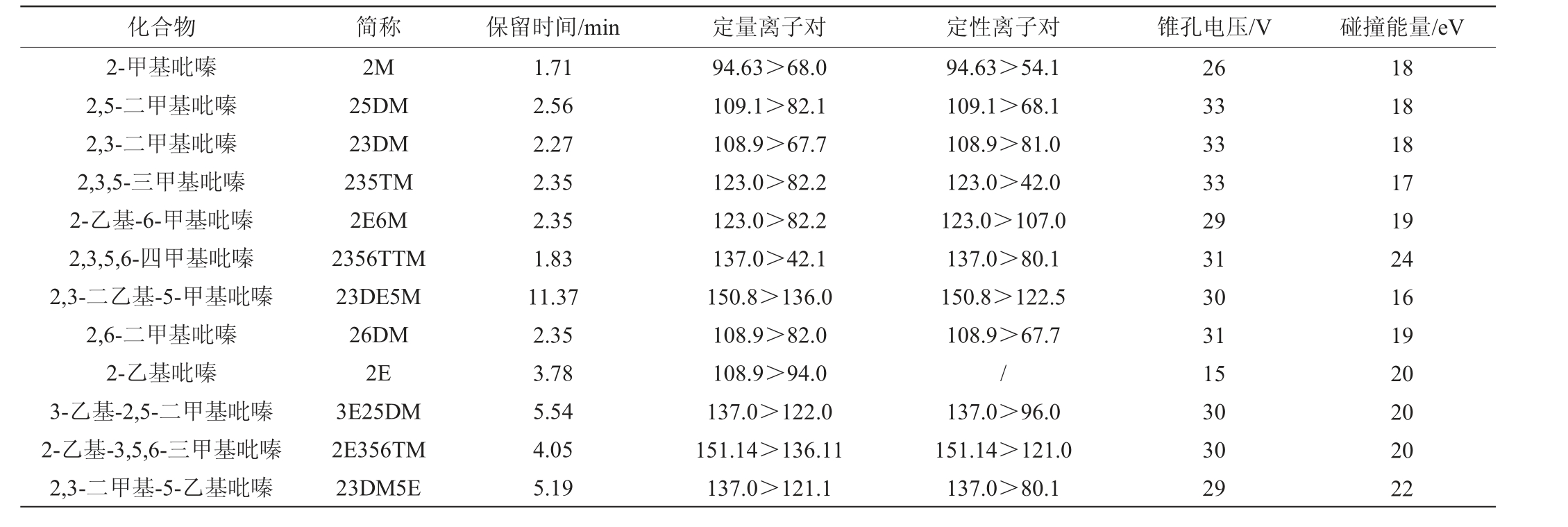
化合物 简称 保留时间/min 定量离子对 定性离子对 锥孔电压/V 碰撞能量/eV 2-甲基吡嗪2,5-二甲基吡嗪2,3-二甲基吡嗪2,3,5-三甲基吡嗪2-乙基-6-甲基吡嗪2,3,5,6-四甲基吡嗪2,3-二乙基-5-甲基吡嗪2,6-二甲基吡嗪2-乙基吡嗪3-乙基-2,5-二甲基吡嗪2-乙基-3,5,6-三甲基吡嗪2,3-二甲基-5-乙基吡嗪2M 25DM 23DM 235TM 2E6M 2356TTM 23DE5M 26DM 2E 3E25DM 2E356TM 23DM5E 1.71 2.56 2.27 2.35 2.35 1.83 11.37 2.35 3.78 5.54 4.05 5.19 94.63>68.0 109.1>82.1 108.9>67.7 123.0>82.2 123.0>82.2 137.0>42.1 150.8>136.0 108.9>82.0 108.9>94.0 137.0>122.0 151.14>136.11 137.0>121.1 94.63>54.1 109.1>68.1 108.9>81.0 123.0>42.0 123.0>107.0 137.0>80.1 150.8>122.5 108.9>67.7/137.0>96.0 151.14>121.0 137.0>80.1 26 33 33 33 29 31 30 31 15 30 30 29 18 18 18 17 19 24 16 19 20 20 20 22
1.3.3 标准溶液的配制
分别精确称取2M、25DM、23DM、235TM、2E6M、2356TTM、23DE5M、26DM、2E、3E25DM、2E356TM、23DM5E标准品适量,加入甲醇溶解定容,配制成质量浓度均为1.0 mg/mL的单个标准品储备液,分别准确量取上述对照品贮备液1.0 mL于100 mL容量瓶中,用蒸馏水稀释定容至刻度,得混合标准品溶液。
1.3.4 色谱及前处理条件优化
考察不同流动相(0.1%甲酸乙腈-0.1%甲酸水、0.2%甲酸乙腈-0.2%甲酸水、0.5%甲酸乙腈-0.5%甲酸水、0.9%甲酸乙腈-0.9%甲酸水)、不同柱温(20 ℃、30 ℃、35 ℃、40 ℃)、不同流动相流速(0.2 mL/min、0.30 mL/min、0.45 mL/min)、不同前处理条件(直接进样、氮吹浓缩)对试验结果的影响。
1.3.5 数据分析
沃特世质谱软件MassLynx采集质谱数据,采用SIMCA 14.1软件基于吡嗪类物质的含量对不同年份白酒样品进行了主成分分析(principal component analysis,PCA)、层次聚类分析(hierarchical cluster analysis,HCA)和偏最小二乘判别分析(partial least squares discrimination analysis,PLS-DA),对实验数据进行统计分析,分别用MeV软件绘制热图和Origin 2021软件绘制柱状图。
2 结果与分析
2.1 色谱条件的优化
2.1.1 流动相的选择
本研究所测定的12种吡嗪类化合物,其中23DM、25DM、26DM为同分异构体,在质谱选择中它们有着相同的母离子和子离子,所以必须要在色谱上实现分离才能准确定量。此外,考虑到吡嗪类化合物为1,4-位含氮的弱碱性化合物,在流动相中加入少量的有机酸可增强其离子化效率,提高分析方法的灵敏度,本研究分别考察不同流动相对23DM、25DM、26DM分离效果的影响,色谱结果见图1。由图1可知,甲酸含量较低时,23DM、25DM的洗脱效果不佳,2E未出峰,甲酸含量为0.9%时,12种吡嗪类化合物的分离效果及响应值较好。因此,本实验选择0.9%甲酸乙腈-0.9%甲酸水系统作为流动相。
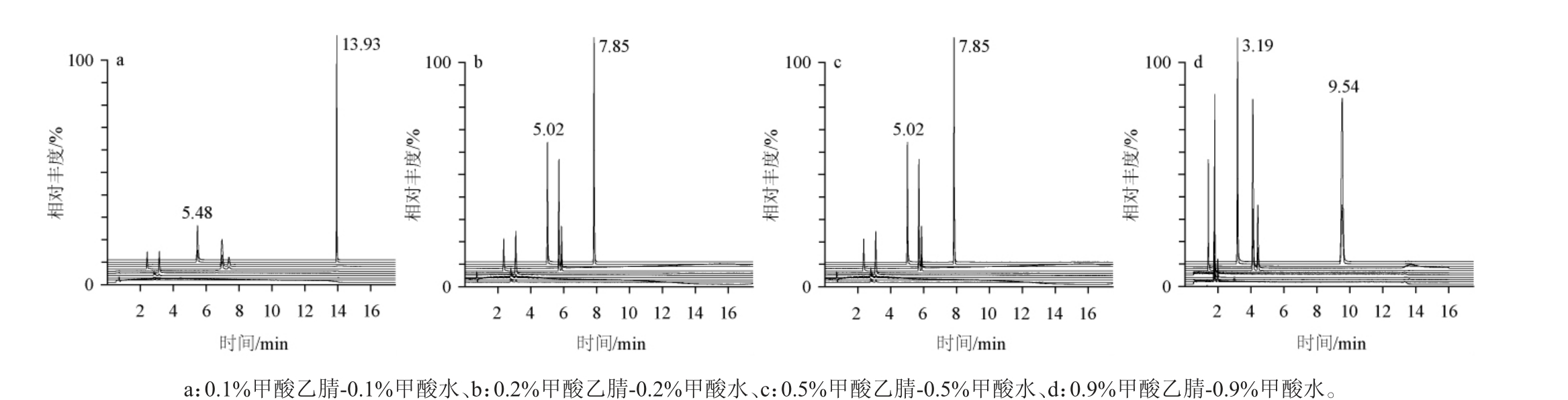
图1 12种吡嗪类化合物在不同流动相体系下的UPLC-MS/MS总离子色谱图
Fig.1 UPLC-MS/MS total ion chromatograms of 12 pyrazine compounds in different mobile phase systems
2.1.2 柱温的选择
色谱柱温度是影响化合物峰型和响应值的重要因素之一,本试验考察不同柱温(20 ℃、30 ℃、35 ℃、40 ℃)对12种吡嗪类化合物响应值的影响,结果见图2。由图2可知,随着色谱柱柱温的升高,吡嗪类化合物的响应值相应增加,当柱温为40 ℃时,12种吡嗪类物质的响应最高,因此试验选40 ℃作为色谱柱温度。
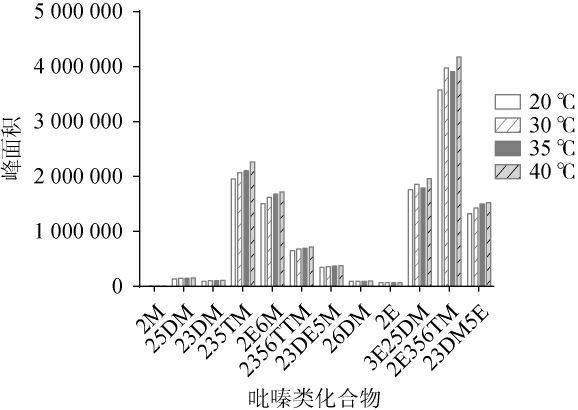
图2 不同柱温对12种吡嗪类化合物测定结果的影响
Fig.2 Effect of different column temperatures on the measurement results of 12 pyrazine compounds
2.1.3 流动相流速的选择
随着流速增大,柱压相应增大,在保证分离效果和压力适中的前提下,应尽可能快的使待检测组分被检出,进而降低分析检测时间,本研究以0.9%甲酸乙腈-0.9%甲酸水系统为流动相,柱温40 ℃,考察不同流速对吡嗪类化合物的分离情况,结果见图3。由图3可知,流速为0.45 mL/min时同分异构体23DM、25DM、26DM的分析效果良好,因此确定最佳流动相流速为0.45 mL/min。
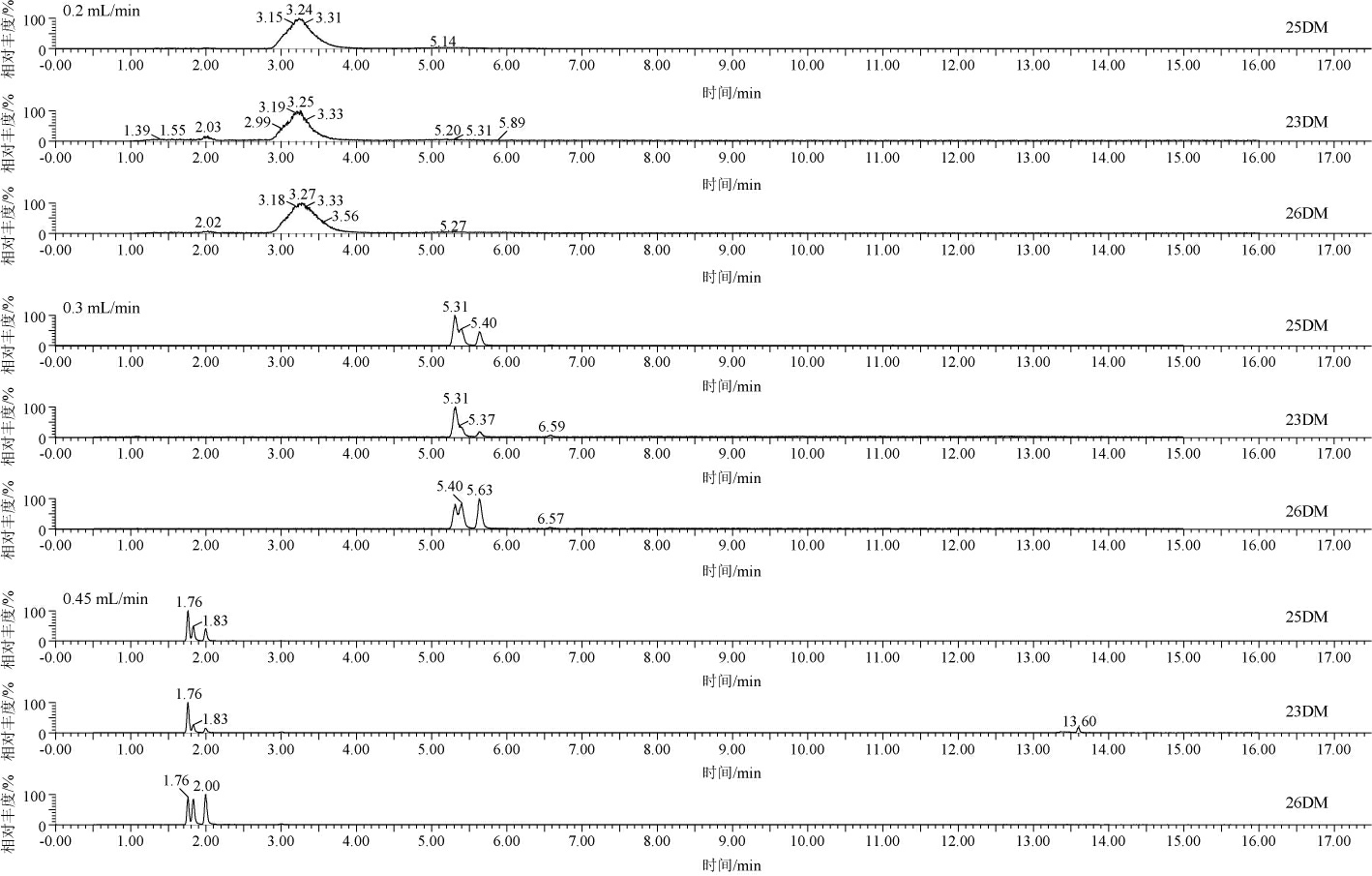
图3 23DM、25DM、26DM在不同流动相流速下的UPLC-MS/MS总离子色谱图
Fig.3 UPLC-MS/MS total ion chromatograms of 23DM, 25DM, 26DM at different mobile phase flow rates
综上,优化的UPLC色谱条件为柱温:40 ℃,梯度洗脱,流动相A为0.9%甲酸水溶液,流动相B为0.9%甲酸乙腈,流速为0.45 mL/min。在此优化条件下,12种吡嗪类化合物的UPLC-MS/MS色谱图见图4。由图4可知,在此优化色谱条件下,12种吡嗪类物质分离良好。
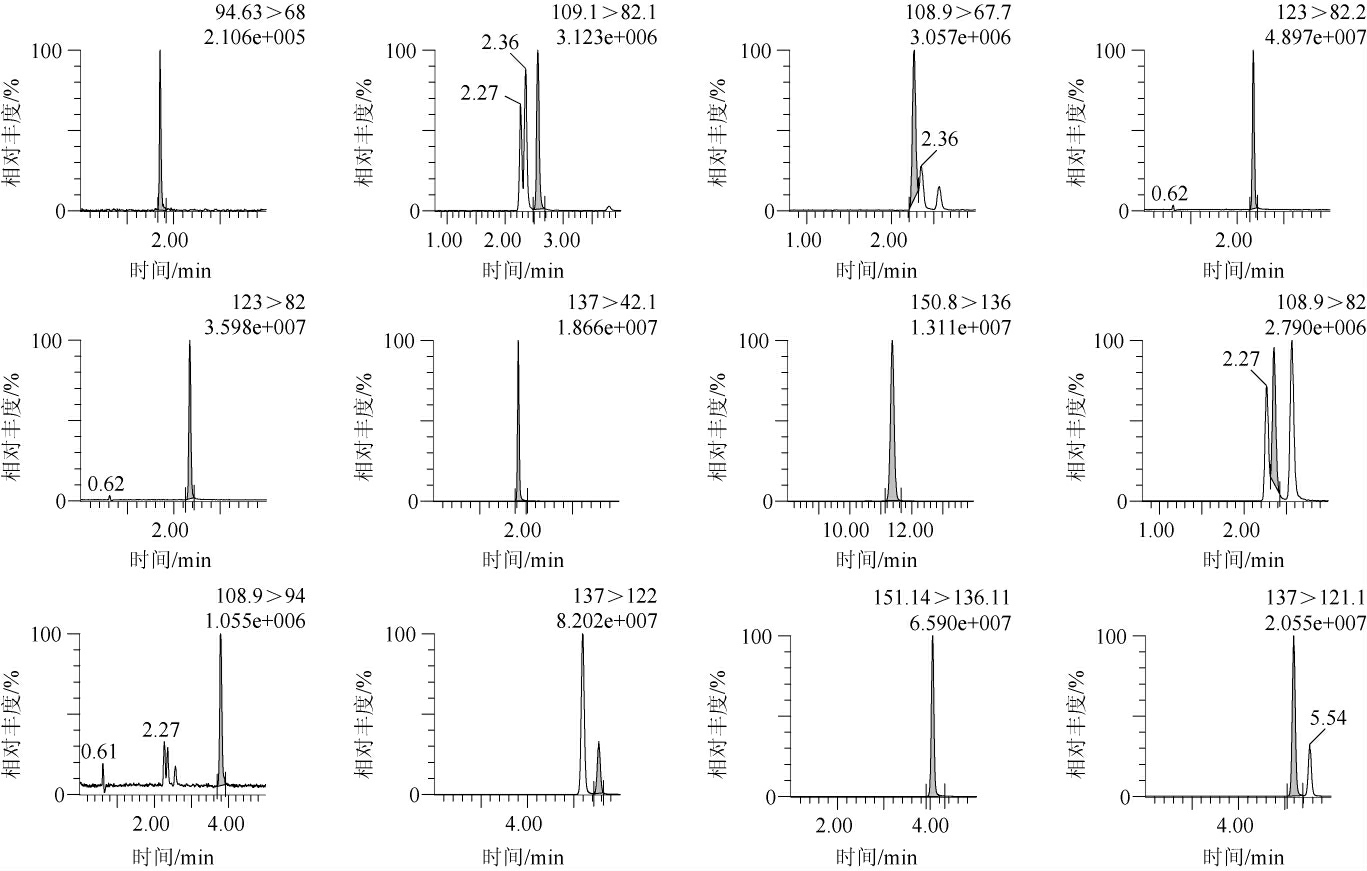
图4 12种吡嗪类化合物的多反应监测质谱图
Fig.4 Multiple reaction monitoring mass spectra of 12 pyrazine compounds
2.2 前处理条件优化
本研究比较了直接进样法和氮吹浓缩的区别,使用直接进样法时,因酱香型白酒中的酸、酯、醇等微量风味物质的干扰,白酒样品中的同分异构体25DM、23DM、26DM不能实现色谱分离,影响定量分析。而氮吹浓缩法对目标组分进行富集,能实现与杂质峰的良好分离,回收率较高,前处理简单。故选择氮吹浓缩法为样品的前处理方法。
2.3 方法学考察
2.3.1 线性关系考察
精确吸取“1.3.3”项下混合标准品溶液,制成系列混合对照品工作溶液,按照“1.3.2”项下色谱条件进样分析,以各对照品的峰面积(Y)与其相应的质量浓度(X)绘制标准曲线。以信噪比(signal-noise ratio,S/N)分别为3和10时各对照品的质量浓度作为检出限(limit of detection,LOD)和定量限(limit of quantitation,LOQ),结果见表3。由表3可知,12种吡嗪类化合物在所测试质量浓度范围内具有良好的线性关系,相关系数(R2)均大于0.99,检出限在0.051~6.00 μg/L,定量限在0.18~21.42 μg/L。
表3 12种吡嗪类化合物标准品回归方程、线性范围、检出限及定量限
Table 3 Regression equation, linear range, limits of detection and limits of quantification of 12 pyrazine compounds standards
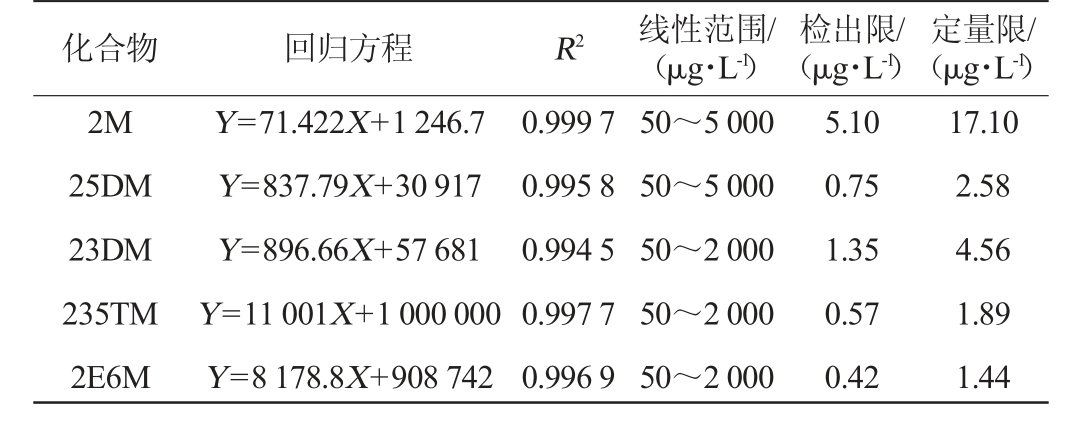
化合物 回归方程 R2 线性范围/(μg·L-1)检出限/(μg·L-1)定量限/(μg·L-1)2M 25DM 23DM 235TM 2E6M Y=71.422X+1 246.7 Y=837.79X+30 917 Y=896.66X+57 681 Y=11 001X+1 000 000 Y=8 178.8X+908 742 0.999 7 0.995 8 0.994 5 0.997 7 0.996 9 50~5 000 50~5 000 50~2 000 50~2 000 50~2 000 5.10 0.75 1.35 0.57 0.42 17.10 2.58 4.56 1.89 1.44
续表
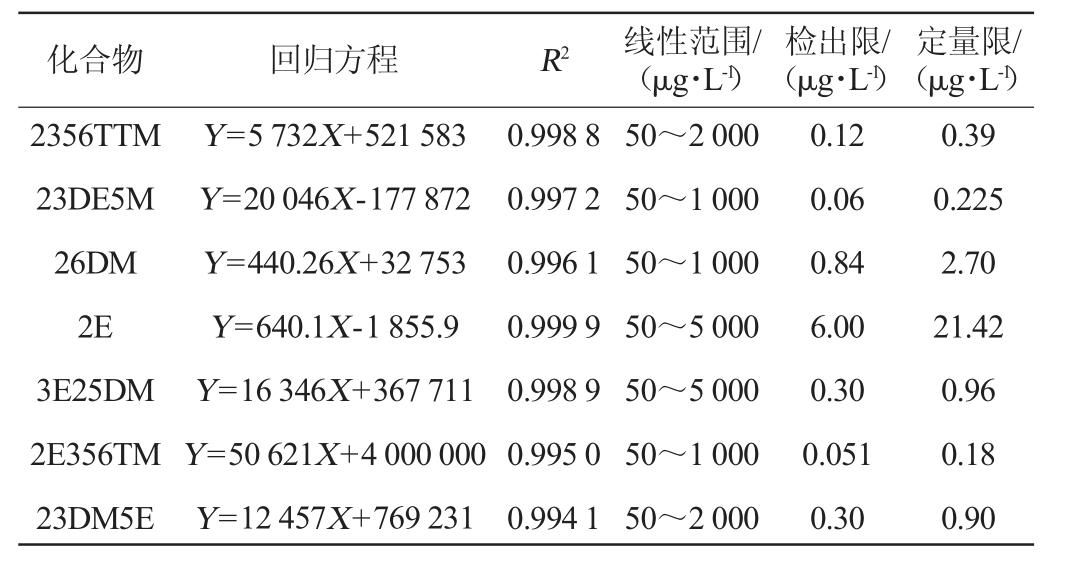
化合物 回归方程 R2 线性范围/(μg·L-1)检出限/(μg·L-1)定量限/(μg·L-1)2356TTM 23DE5M 26DM 2E 3E25DM 2E356TM 23DM5E Y=5 732X+521 583 Y=20 046X-177 872 Y=440.26X+32 753 Y=640.1X-1 855.9 Y=16 346X+367 711 Y=50 621X+4 000 000 Y=12 457X+769 231 0.998 8 0.997 2 0.996 1 0.999 9 0.998 9 0.995 0 0.994 1 50~2 000 50~1 000 50~1 000 50~5 000 50~5 000 50~1 000 50~2 000 0.12 0.06 0.84 6.00 0.30 0.051 0.30 0.39 0.225 2.70 21.42 0.96 0.18 0.90
2.3.2 精密度试验
将100 ng/mL的混合标准品溶液按“1.3.2”确定的色谱条件进样,测定物质的含量并计算日内精密度,日内精密度是通过1 d内不同时段分析6次获得,根据6次试验结果计算相对标准偏差(relative standard deviation,RSD),结果见表4。由表4可知,2M、25DM、23DM、235TM、2E6M、2356TTM、23DE5M、26DM、2E、3E25DM、2E356TM、23DM5E的日内RSD分别为1.05%、1.82%、2.28%、0.67%、2.03%、2.72%、2.36%、0.90%、1.00%、1.63%、2.14%、1.18%,RSD范围均在0.67%~2.72%,均<5%,表明该方法的精密度较高,能满足酱香型白酒中12种吡嗪类化合物的检测需求。
表4 12种吡嗪类化合物的日内精密度试验结果
Table 4 Results of the intra-day precision experiments of 12 pyrazine compounds
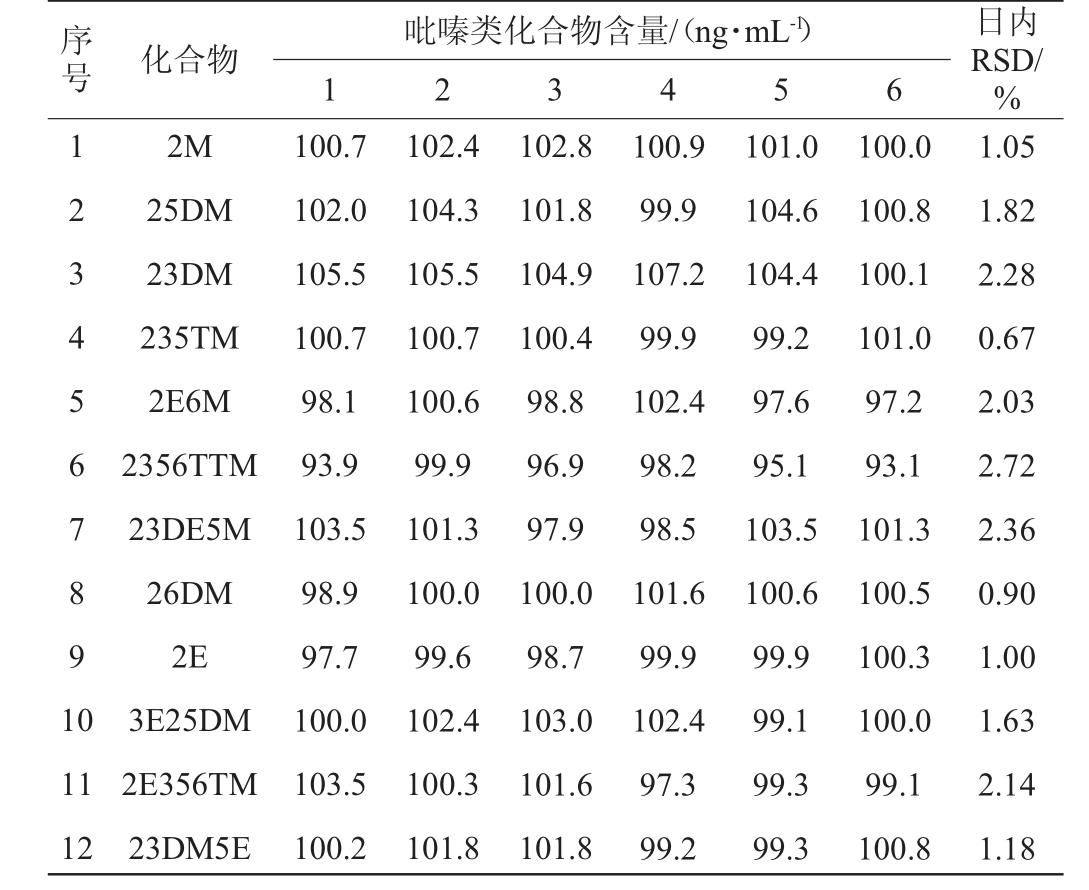
序号 化合物吡嗪类化合物含量/(ng·mL-1)1 2 3 4 5 6日内RSD/%1 2 3 4 5 6 7 8 9 1 0 11 12 2M 25DM 23DM 235TM 2E6M 2356TTM 23DE5M 26DM 2E 3E25DM 2E356TM 23DM5E 100.7 102.0 105.5 100.7 98.1 93.9 103.5 98.9 97.7 100.0 103.5 100.2 102.4 104.3 105.5 100.7 100.6 99.9 101.3 100.0 99.6 102.4 100.3 101.8 102.8 101.8 104.9 100.4 98.8 96.9 97.9 100.0 98.7 103.0 101.6 101.8 100.9 99.9 107.2 99.9 102.4 98.2 98.5 101.6 99.9 102.4 97.3 99.2 101.0 104.6 104.4 99.2 97.6 95.1 103.5 100.6 99.9 99.1 99.3 99.3 100.0 100.8 100.1 101.0 97.2 93.1 101.3 100.5 100.3 100.0 99.1 100.8 1.05 1.82 2.28 0.67 2.03 2.72 2.36 0.90 1.00 1.63 2.14 1.18
2.3.3 加标回收率试验
用无水乙醇配制体积分数为53%的乙醇溶液,作为空白酒样,分别添加0.1 μg/mL、0.2 μg/mL、0.5 μg/mL三个不同水平质量浓度的12种吡嗪类化合物,计算加标回收率,结果见表5。由表5可知,12种吡嗪类物质的平均加标回收率在80.6%~108.7%,RSD为0.49%~4.73%,均<5%,表明该方法的准确度良好,可以满足试验要求。
表5 12种吡嗪类化合物的加标回收率结果
Table 5 Results of the standard recovery rates of 12 pyrazine compounds
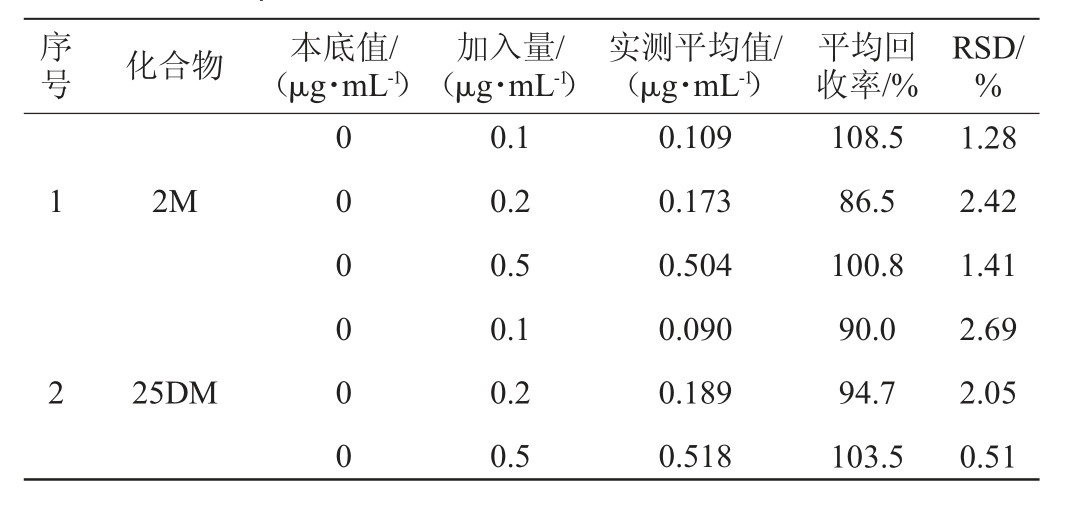
序号 化合物 本底值/(μg·mL-1)加入量/(μg·mL-1)实测平均值/(μg·mL-1)平均回收率/%RSD/%1 2M 2 25DM 0 0 0 0 0 0 0.1 0.2 0.5 0.1 0.2 0.5 0.109 0.173 0.504 0.090 0.189 0.518 108.5 86.5 100.8 90.0 94.7 103.5 1.28 2.42 1.41 2.69 2.05 0.51
续表
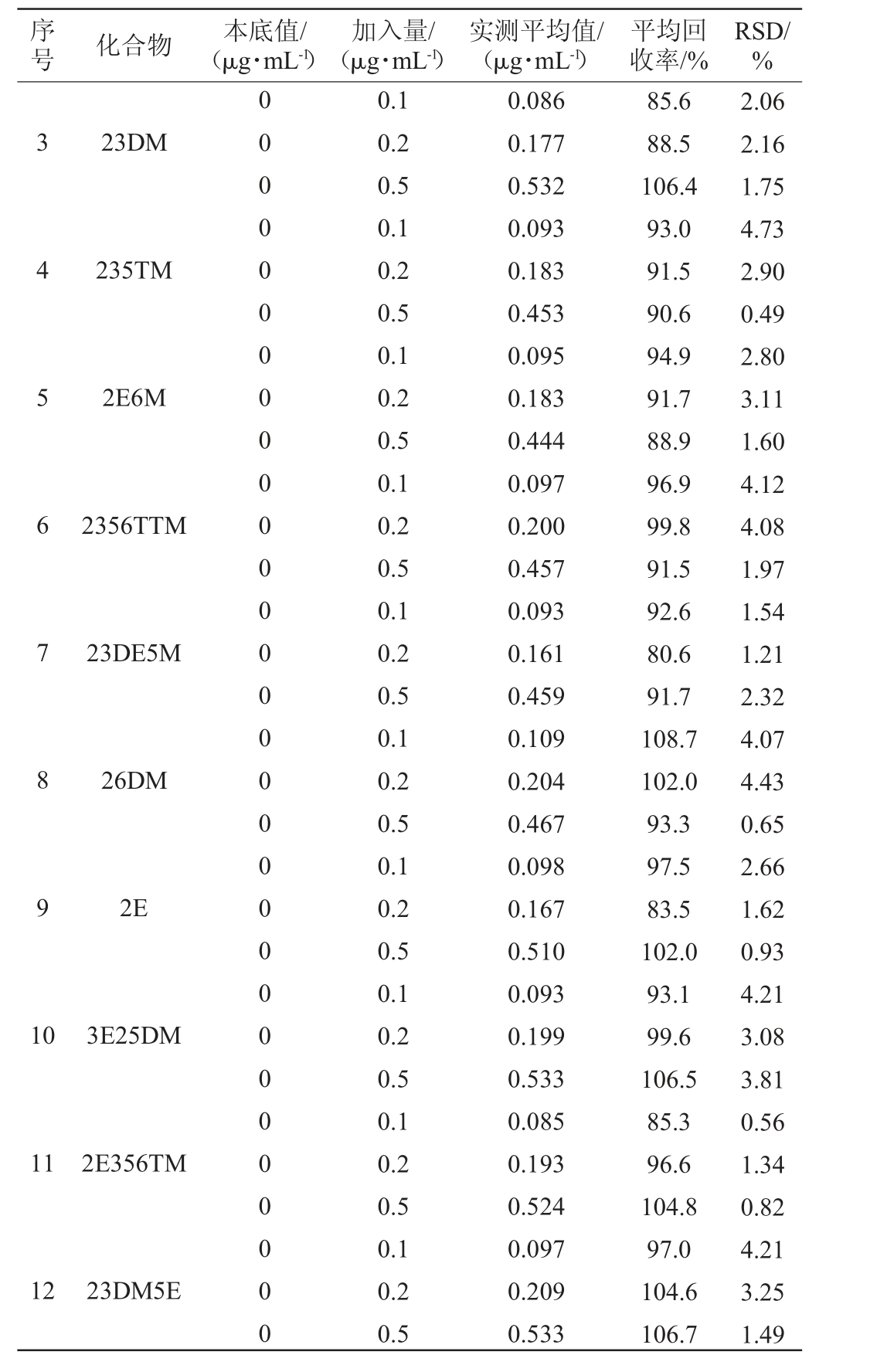
序号 化合物 本底值/(μg·mL-1)加入量/(μg·mL-1)实测平均值/(μg·mL-1)平均回收率/%RSD/%3 4 5 6 7 8 9 1 0 23DM 235TM 2E6M 2356TTM 23DE5M 26DM 2E 3E25DM 11 2E356TM 12 23DM5E 000000000000000000000000000000 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.1 0.2 0.5 0.086 0.177 0.532 0.093 0.183 0.453 0.095 0.183 0.444 0.097 0.200 0.457 0.093 0.161 0.459 0.109 0.204 0.467 0.098 0.167 0.510 0.093 0.199 0.533 0.085 0.193 0.524 0.097 0.209 0.533 85.6 88.5 106.4 93.0 91.5 90.6 94.9 91.7 88.9 96.9 99.8 91.5 92.6 80.6 91.7 108.7 102.0 93.3 97.5 83.5 102.0 93.1 99.6 106.5 85.3 96.6 104.8 97.0 104.6 106.7 2.06 2.16 1.75 4.73 2.90 0.49 2.80 3.11 1.60 4.12 4.08 1.97 1.54 1.21 2.32 4.07 4.43 0.65 2.66 1.62 0.93 4.21 3.08 3.81 0.56 1.34 0.82 4.21 3.25 1.49
2.4 不同年份酱香型白酒样品中吡嗪类物质含量的测定
取不同年份的酱香型白酒样品,按“1.3.1”项下方法制备供试品溶液,并按“1.3.2”色谱条件进样分析测定,记录各待测成分的峰面积,计算酱香型白酒不同年份的样品中2M、25DM、23DM、235TM、2E6M、2356TTM、23DE5M、26DM、2E、3E25DM、2E356TM、23DM5E的含量,结果见表6。
表6 不同年份酱香型白酒样品中12种吡嗪类物质含量的测定结果
Table 6 Determination results of 12 pyrazines in sauce-flavor Baijiu samples of different aging years μg/mL
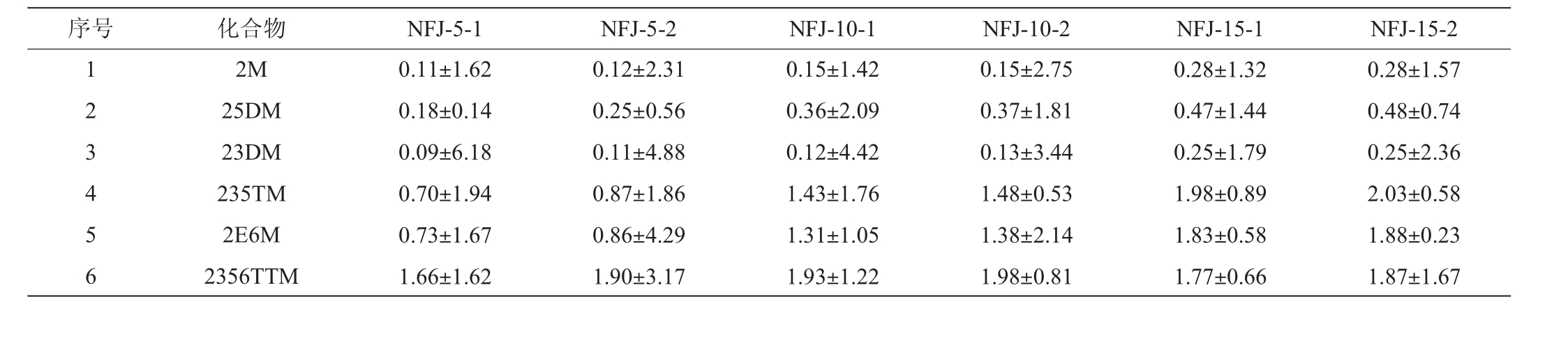
序号 化合物 NFJ-5-1 NFJ-5-2 NFJ-10-1 NFJ-10-2 NFJ-15-1 NFJ-15-2 1 2 3 4 5 6 2M 25DM 23DM 235TM 2E6M 2356TTM 0.11±1.62 0.18±0.14 0.09±6.18 0.70±1.94 0.73±1.67 1.66±1.62 0.12±2.31 0.25±0.56 0.11±4.88 0.87±1.86 0.86±4.29 1.90±3.17 0.15±1.42 0.36±2.09 0.12±4.42 1.43±1.76 1.31±1.05 1.93±1.22 0.15±2.75 0.37±1.81 0.13±3.44 1.48±0.53 1.38±2.14 1.98±0.81 0.28±1.32 0.47±1.44 0.25±1.79 1.98±0.89 1.83±0.58 1.77±0.66 0.28±1.57 0.48±0.74 0.25±2.36 2.03±0.58 1.88±0.23 1.87±1.67
续表
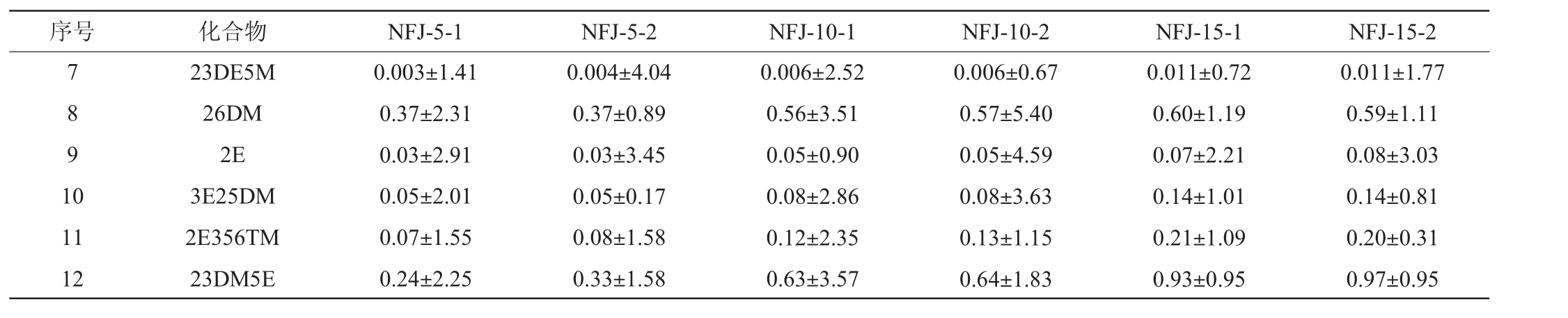
序号 化合物 NFJ-5-1 NFJ-5-2 NFJ-10-1 NFJ-10-2 NFJ-15-1 NFJ-15-2 7 8 9 1 0 11 12 23DE5M 26DM 2E 3E25DM 2E356TM 23DM5E 0.003±1.41 0.37±2.31 0.03±2.91 0.05±2.01 0.07±1.55 0.24±2.25 0.004±4.04 0.37±0.89 0.03±3.45 0.05±0.17 0.08±1.58 0.33±1.58 0.006±2.52 0.56±3.51 0.05±0.90 0.08±2.86 0.12±2.35 0.63±3.57 0.006±0.67 0.57±5.40 0.05±4.59 0.08±3.63 0.13±1.15 0.64±1.83 0.011±0.72 0.60±1.19 0.07±2.21 0.14±1.01 0.21±1.09 0.93±0.95 0.011±1.77 0.59±1.11 0.08±3.03 0.14±0.81 0.20±0.31 0.97±0.95
由表6可知,不同年份的酱香型白酒样品中12种吡嗪类化合物均有不同程度的检出,其中质量浓度最高的是235TM,在酱香型白酒15年份的样品中质量浓度高达2.03 μg/mL。质量浓度最低的是23DE5M,在酱香型白酒15年份的样品中质量浓度为0.011 μg/mL,且在不同年份酱香型白酒中均处于低含量水平。
另外,12种吡嗪类化合物随着酱香型白酒贮存年份的增加,其含量均呈现上升态势,在15年份酱香型白酒中含量达到最高值,如:235TM、2E6M、2356TTM。酱香型白酒中2356TTM和235TM的含量较高为酱香型白酒呈现出来的共性,与前期学者的研究相符合[22-23],结果表明该试验方法的准确度高,可用于测定酱香型白酒中吡嗪化合物含量。
2.5 多元统计分析
2.5.1 12种吡嗪类化合物的化学计量学分析
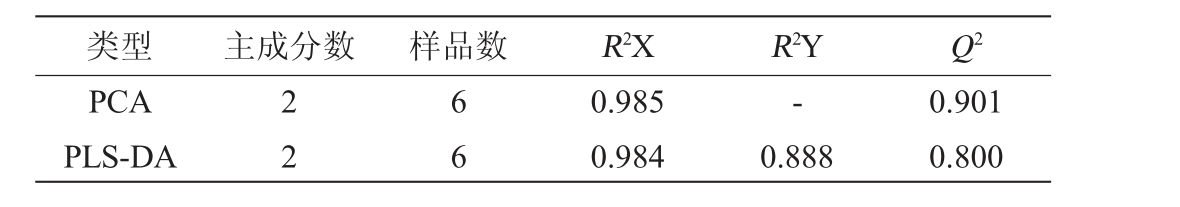
为进一步发掘不同年份酱香型白酒样品中12种吡嗪类物质存在的差异以及使其产生差异的化学成分,采用SIMCA 14.1软件基于吡嗪类物质的含量对不同年份酱香型白酒样品进行了主成分分析(PCA)和偏最小二乘判别分析(PLS-DA)构建鉴别模型并找出关键差异物质[24-26],分析12种吡嗪类物质与酱香型白酒贮存年份的关系,结果见表7和图5。由表7模型数据可知,模型解释能力和预测能力参数均>0.8,说明模型稳定可靠[27]。
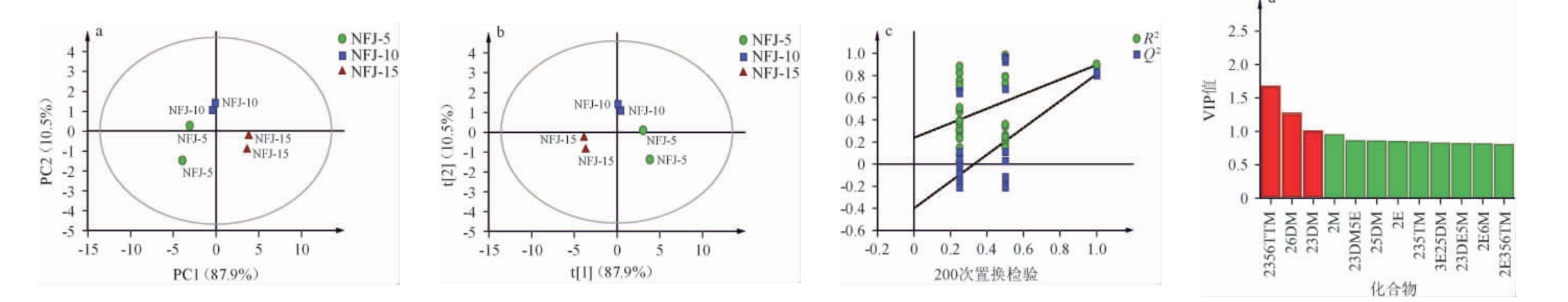
图5 基于12种吡嗪类物质含量不同年份酱香型白酒样品的主成分分析(a)、偏最小二乘判别分析(b)、200次置换检验结果(c)及12种吡嗪类物质的VIP值(d)
Fig.5 Principal component analysis (a), partial least squares-discriminant analysis (b), 200 replacement test results (c) of different aging years of sauce-flavor Baijiu samples based on 12 pyrazines and VIP value (d) of 12 pyrazines
表7 不同年份酱香型白酒样品中吡嗪类物质的模型参数
Table 7 Modeling parameters of pyrazines in sauce-flavor Baijiu samples of different aging years
?
由图5a和图5b可知,不同年份酒整体区分效果明显,其中NFJ-10和NFJ-15聚类效果最好,NFJ-5的样品相对分散,表明年份酒中12种吡嗪类物质含量存在一定的差异,也为年份酒的区分提供一种思路。通过200次置换检验以评估PLS-DA模型是否过度拟合数据,置换测试的R2=0.25<0.3,Q2=-0.404<0,表明PLS-DA模型有效(见图5c),能够同时对不同年份的酱香型白酒区分较好。变量投影重要性(variable important in projection,VIP)越大,说明变量在样品间的差异就越显著,在研究中常以VIP值>1筛选特征性物质[28]。由图5d可知,以12种吡嗪类物质区分的不同年份酒样品中筛选出了2356TTM、26DM和23DM三种特征性物质,根据VIP值大小进行排序,分别为2356TTM>26DM>23DM,结果表明2356TTM、26DM和23DM可能是不同年份酱香型白酒中的差异性指标成分,可以用于区分不同年份的酱香型白酒。
2.5.2 12种吡嗪化合物的聚类分析
为了更加直观地观察不同年份酒中吡嗪类物质的变化规律,对12种吡嗪类化合物含量进行聚类分析[29],结果见图6。图中红色区域代表吡嗪类物质的高表达区,深蓝色区域代表吡嗪类物质的中表达区,蓝色区域代表吡嗪类物质的低表达区。由图6可知,在NFJ-5样品中约11种吡嗪类物质集中于低表达区,NFJ-10中12种吡嗪类物质在3个表达区中均有体现,以中度表达区为主,NFJ-15样品中10种吡嗪物质均集中于高表达区。结合图5和图6,2356TTM和26DM的含量表达规律与其他吡嗪类物质的规律不一致,其他吡嗪类物质随着年份酒的年份增长,其含量呈增加趋势明显,23DM的含量变化在5~10年中趋势相对减缓,与PLS-DA模型中VIP值分析结果一致。
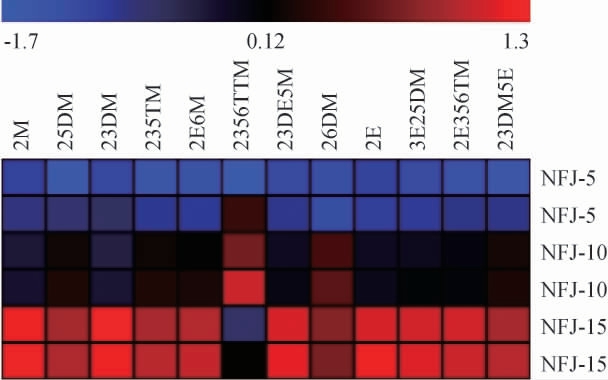
图6 不同年份酱香型白酒样品中12种吡嗪类物质的聚类分析
Fig.6 Clustering analysis of 12 pyrazines in sauce-flavor Baijiu samples of different aging years
3 结论
该研究建立了一种超高效液相色谱-质谱联用法测定酱香型白酒中12种吡嗪类化合物含量的方法,实现了对12种吡嗪类化合物的同时测定,该方法提取步骤简单、方便快速、定性灵敏、定量准确。采用该方法对不同年份酱香型白酒样品中吡嗪类化合物进行跟踪测定,结果表明酱香型白酒中吡嗪类化合物含量的高低与存放年份的长短存在一定的关联性。12种吡嗪类化合物随着酱香型白酒贮存年份的增长,含量分布均呈上升趋势,在15年酱香型白酒中含量达到最高值。此外,通过对测定结果进行多元统计分析发现,12种吡嗪类化合物的含量可以有效区分不同年份的酱香型白酒,2356TTM、26DM和23DM可能为主要差异性指标成分。本研究为快速鉴别不同年份酱香型白酒的方法开发提供理论和相关数据支撑,对建立健全酱香型白酒检测体系,促进酱香型白酒生产数字化发展,加强酱香型白酒深层次研究有着重要意义。
[1]FAN W, QIAN M C.Characterization of aroma compounds of Chinese"Wuliangye"and"Jiannanchun"liquors by aroma extract dilution analysis[J].J Agr Food Chem,2006,54(7):2695-2704.
[2]LIU H L, SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].J Agr Food Chem,2018,66(22):5425-5432.
[3]MU X Q,LU J,GAO M X,et al.Optimization and validation of a headspace solid-phase microextraction with comprehensive two-dimensional gas chromatography time-of-flight mass spectrometric detection for quantification of trace aroma compounds in Chinese liquor(Baijiu)[J].Molecules,2021,26(22):6910.
[4]刘鑫,王耀,庹先国,等.白酒检测技术在生产中的应用研究进展[J].中国酿造,2022,41(3):6-12.
[5]张卫卫,刘建学,韩四海,等.白酒基酒典型风味物质含量的测定方法与差异性研究[J].食品科学,2015,36(24):122-126.
[6]姜晓坤,应铁进.气相色谱-质谱法分析比较传统同山高粱酒及其改良工艺酒样中的香气成分[J].食品工业科技,2016,37(4):87-91.
[7]代汉聪,张宿义,周军,等.低度白酒贮存过程中风味质量变化研究[J].酿酒科技,2020(7):27-32.
[8]王婧,王晓丹,邱树毅,等.酱香型白酒酿造体系风格特征形成探究[J].酿酒,2015,42(4):99-104.
[9]ZHANG Y H,YANG R Y,XIE F W,et al.Control strategies of pyrazines generation from Maillard reaction[J].Trend Food Sci Technol,2021,112:795-807.
[10]DENG S B,CUI H P,HAYAT K,et al.Comparison of pyrazines formation in methio-nine/glucose and corresponding amadori rearrangement product model[J].Food Chem,2022,382,132500.
[11]吴建峰.中国白酒中健康功能性成份四甲基吡嗪的研究综述[J].酿酒,2006,33(6):13-16.
[12]孙宝国,李贺贺,胡萧梅,等.健康白酒的发展趋势[J].中国食品学报,2016,16(8):1-6.
[13]王荣钰,赵金松,苏占元,等.酱香型白酒关键酱香风味物质研究现状[J].酿酒科技,2020(6):81-86.
[14]朱明,丁子元,郑晓卫,等.白酒风味物质成分分析方法及其相关成果研究进展[J].酿酒科技,2022(10):81-87.
[15]徐岩,范文来,葛向阳,等.科学认识中国白酒中的生物活性成分[J].酿酒科技,2013(9):1-6.
[16]范文来,徐岩.白酒功能因子与品质安全问题[J].酿酒科技,2012(3):17-21.
[17]乔慧,高晓娟.GC-NPD快速测定吡嗪类物质方法研究[J].酿酒,2011,38(6):45-46.
[18]梅明明,朱婧,李妍,等.气相色谱-质谱法测定白酒中3种吡嗪类化合物[J].现代预防医学,2015,42(14):2597-2599,2614.
[19]王国明,尹婉嫱,乔阳,等.浓香型“山庄老酒”中吡嗪类物质的分析研究[J].中国酿造,2015(4):146-199.
[20]黄杰,陆玮,汤有宏,等.基于GC-QQQ分析技术测定白酒中四甲基吡嗪的研究[J].食品与发酵科技,2015,51(6):50-52,67.
[21]刘家欢,孙细珍,熊亚青,等.不同轮次酱香型白酒中吡嗪类化合物含量分析[J].食品与发酵科技,2023,59(3):103-110.
[22]王莉,吴建霞,雷良波.气相色谱-质谱-离子扫描联用法快速检测白酒中4种吡嗪类化合物[J].中国酿造,2009,28(3):148-150.
[23]赵应梅,黄家岭,孙棣.GC-MS-SIM 联用法测定白酒中8种吡嗪类化合物[J].酿酒科技,2015(8):151-153.
[24]QIN H,HUO D Q,ZHANG L,et al.Colorimetric artificial nose for identification of Chinese liquor with different geographic origins[J].Food Res Int,2012,45(1):45-51.
[25]黄婷,杨亚娇,刘茗铭,等.基于化学计量学的四川不同产区浓香型原酒判别分析[J].酿酒,2022,49(1):64-70.
[26]马宇.基于风味组学策略研究酱香型白酒关键成分及其呈香呈味特性[D].贵阳:贵州大学,2019.
[27]徐春晖,王远兴.基于GC-MS结合化学计量学方法鉴别3种江西名茶[J].食品科学,2020,41(20):141-150.
[28]孙细珍,张帆,杜佳炜,等.基于毛细管气相色谱法和主成分分析的白酒真假酒判别分析[J].酿酒,2021,48(1):42-50.
[29]张琴,董晓庆,林欣,等.基于UPLC-MS/MS的不同产地蜂糖李果实初生代谢差异分析[J].食品科学,2023,44(8):284-292.